Содержание
- 2. Понятие об алкинах Алкины – углеводороды, содержащие в молекуле одну тройную связь между атомами углерода, а
- 3. Номенклатура алкинов. (Согласно международной номенклатуре названия ацетиленовых углеводородов производят от соответствующего алкана с заменой суффикса –ан
- 4. Гомологический ряд алкинов C2H2 C3H4 C4H6 C5H8 C6H10 C7H12 Этин или ацетилен Пропин Бутин Пентин Гексин
- 5. Изомерия алкинов Структурная изомерия 1. Изомерия положения тройной связи (начиная с С4Н6): СН ≡С−СН2−СН3 СН3−С≡С−СН3 бутин-1
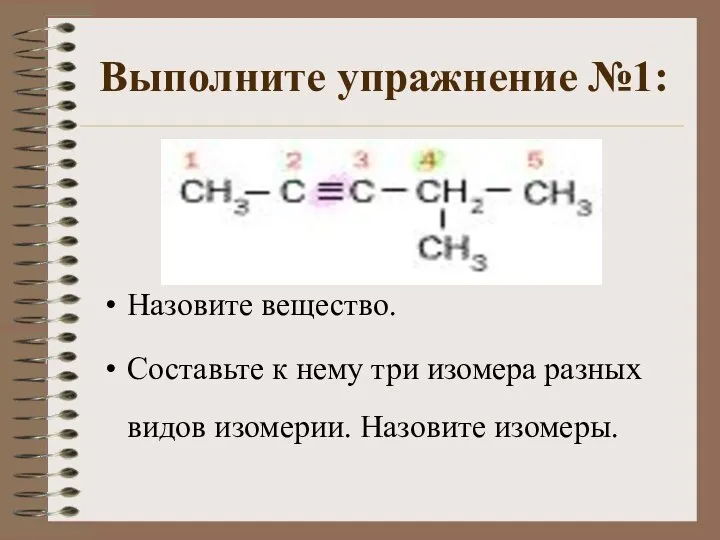
- 6. Выполните упражнение №1: Назовите вещество. Составьте к нему три изомера разных видов изомерии. Назовите изомеры.
- 7. Физические свойства Температуры кипения и плавления алкинов, так же как и алкенов, закономерно повышаются при увеличении
- 8. Ацетилен получают в промышленности двумя способами: 1. Термический крекинг метана: 1500°С 2СН4 ⎯⎯→ С2Н2 + 3Н2
- 9. Химические свойства алкинов Химические свойства ацетилена и его гомологов в основном определяются наличием в их молекулах
- 10. Реакции присоединения 1. Галогенирование Обесцвечивание бромной воды является качественной реакцией на все непредельные углеводороды
- 11. 2. Гидрогалогенирование. 3. Гидрирование. 4. Гидратация. HgSO4 Н−C≡C−H + H2O ⎯→ [H−C=C−H] ⎯→ CH3−C−H ⏐ ⏐
- 12. Окисление Ацетилен и его гомологи окисляются перманганатом калия с расщеплением тройной связи и образованием карбоновых кислот:
- 13. Горение ацетилена При сгорании (полном окислении) ацетилена выделяется большое количества тепла: HC≡CH + 2О2 ⎯→ 2СО2
- 14. Реакции замещения При взаимодействии ацетилена (или R−C≡C−H) с аммиачными растворами оксида серебра выпадают осадки нерастворимых ацетиленидов:
- 15. Реакция полимеризации 1. Димеризация под действием водного раствора CuCl и NH4Cl: НC≡CH + НC≡CH ⎯→ Н2C=CH−C≡CH
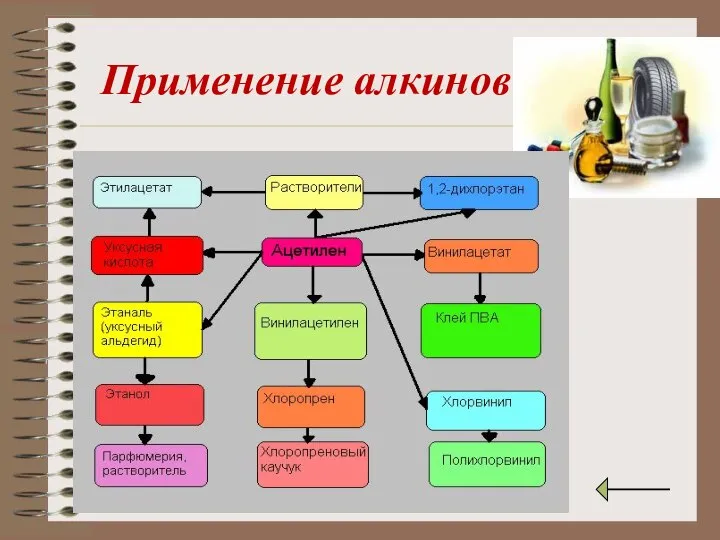
- 16. Применение алкинов
- 18. Скачать презентацию








![2. Гидрогалогенирование. 3. Гидрирование. 4. Гидратация. HgSO4 Н−C≡C−H + H2O ⎯→ [H−C=C−H]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1072202/slide-10.jpg)




 Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Водные биоресурсы и аквакультура. Расчеты в объемном анализе
Водные биоресурсы и аквакультура. Расчеты в объемном анализе Термохимия
Термохимия Исследование снега на общую химическую токсичность методом биотестирования Автор: Милюта Юлия, Тюменская область, Тюменский рай
Исследование снега на общую химическую токсичность методом биотестирования Автор: Милюта Юлия, Тюменская область, Тюменский рай Топливоснабжение источников децентрализованного теплоэнергоснабжения
Топливоснабжение источников децентрализованного теплоэнергоснабжения Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена
Ключевые реакции и регуляторные ферменты начальных этапов углеводного обмена Исследование химического состава разных сортов картофеля
Исследование химического состава разных сортов картофеля Знаки химических элементов. Периодическая система
Знаки химических элементов. Периодическая система Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение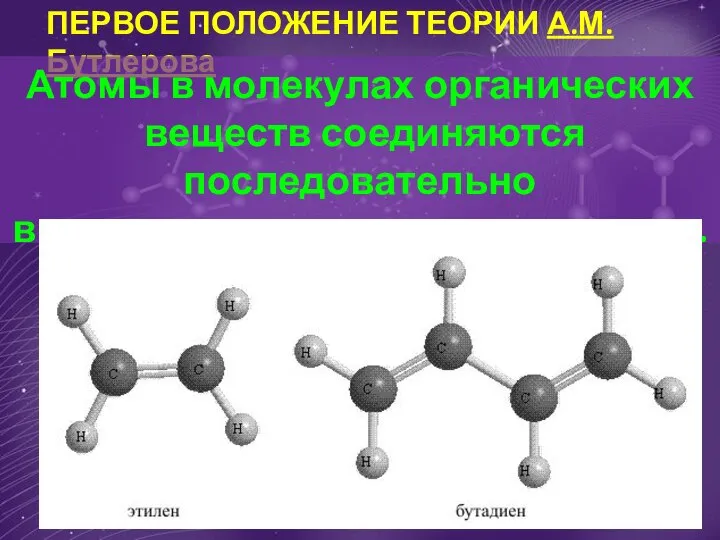 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Презентация на тему Спирты
Презентация на тему Спирты  Окислительно-восстновительные реакции
Окислительно-восстновительные реакции Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции
Реакционная система. Схема химической реакции. Закон сохранения массы веществ в химической реакции Презентация на тему Химические средства гигиены и косметика
Презентация на тему Химические средства гигиены и косметика  РАСЧЕТЫ по химическим уравнениям
РАСЧЕТЫ по химическим уравнениям Алкены (непредельные углеводороды)
Алкены (непредельные углеводороды) Полимеры. Пластмассы
Полимеры. Пластмассы Переработка каменного угля. Коксование
Переработка каменного угля. Коксование Презентация по Химии "Быль о каучуке"
Презентация по Химии "Быль о каучуке"  Химические свойства и применение этилена
Химические свойства и применение этилена Интегративный подход к обучению на уроках химии
Интегративный подход к обучению на уроках химии Фосфор - светоносный
Фосфор - светоносный Приключение кислорода
Приключение кислорода Щелочно-земельные металлы и магний
Щелочно-земельные металлы и магний Типы химических реакций
Типы химических реакций Гидролиз солей
Гидролиз солей Знакомство с химией
Знакомство с химией Навчальний проект Дослідження зміни концентрації CO2 у класній кімнаті під час занять
Навчальний проект Дослідження зміни концентрації CO2 у класній кімнаті під час занять