Содержание
- 3. КИСЛОТЫ Тема урока:
- 4. ЦЕЛИ УРОКА: дать определение кислотам, рассмотреть состав кислот, классифицировать кислоты, ознакомиться с формулами и названиями основных
- 5. Кислоты в животном мире Тропический паук педипальпида стреляет во врагов струйкой жидкости, содержащей 84% уксусной кислоты.
- 6. Кислоты в растительном мире Мухоморы в качестве ядовитых токсинов «используют» иботеновую кислоту. Это вещество так ядовито,
- 7. Томаты содержат яблочную, лимонную, щавелевую кислоты
- 8. Аскорбиновая кислота витамин С
- 9. Кислоты в организме человека Если ты проглотил аскорбинку, Твой организм получил витаминку. Она закрывает болезням врата
- 10. Соляная кислота, находящаяся в желудке, помогает переваривать пищу. Молочная кислота образуется в мышцах при физической нагрузке.
- 11. Кислоты применяются в медицине. Аскорбиновая, фолиевая, липоевая, ацетил- салициловая и другие
- 12. Кислоты применяются в кулинарии. Уксусная и лимонная кислоты.
- 13. Прочитайте формулы кислот. HCl, H2SO4, H3PO4 Кислоты HR – это сложные вещества, состоящие из ионов водорода
- 14. ОРГАНИЧЕСКИЕ – ЛИМОННАЯ, ЯБЛОЧНАЯ, УКСУСНАЯ, ЩАВЕЛЕВАЯ, МУРАВЬИНАЯ. 1. По происхождению КЛАССИФИКАЦИЯ КИСЛОТ
- 15. НЕОРГАНИЧЕСКИЕ- СЕРНАЯ, СОЛЯНАЯ, ПЛАВИКОВАЯ, ФОСФОРНАЯ, АЗОТНАЯ.
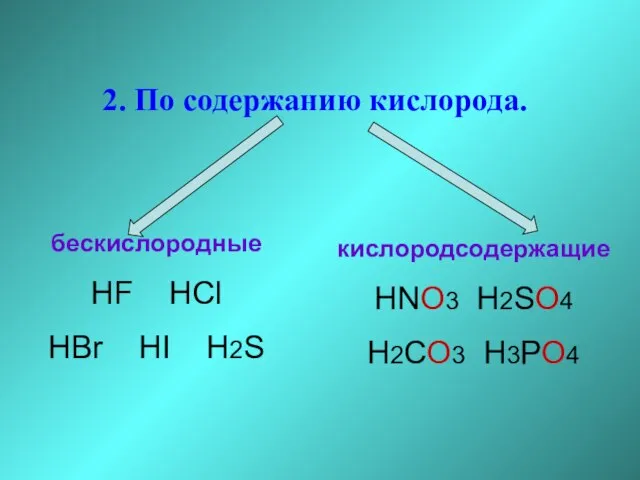
- 16. 2. По содержанию кислорода. бескислородные HF HCl HBr HI H2S кислородсодержащие HNO3 H2SO4 H2CO3 H3PO4
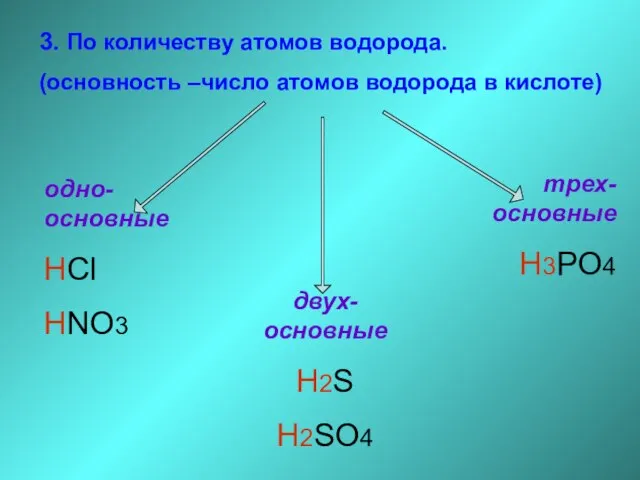
- 17. 3. По количеству атомов водорода. (основность –число атомов водорода в кислоте) одно-основные HCl HNO3 двух-основные H2S
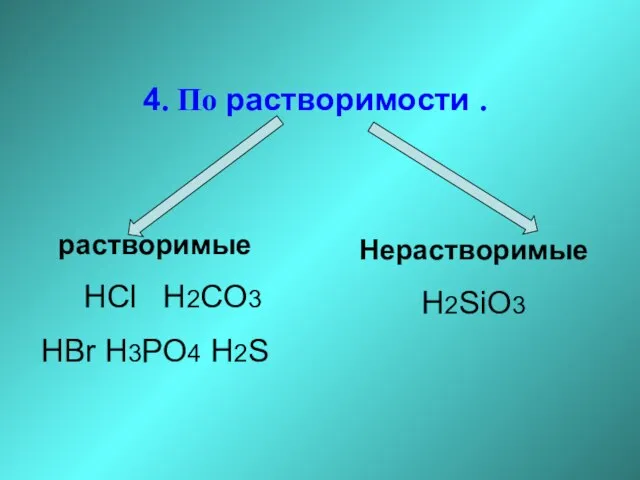
- 18. 4. По растворимости . растворимые HCl H2CO3 HBr H3PO4 H2S Нерастворимые H2SiO3
- 19. 4. По агрегатному состоянию и вкусу Жидкие ( HCI, H2SO4) Твердые (H3PO4, H2SiO3) Кислые( большинство) Сладкие(салициловая
- 20. Правило разбавления кислот (сначала вода, потом - кислота, иначе случится большая беда)
- 21. Лабораторная работа. Поместите по очереди индикаторные бумажки ( лакмус, фенолфталеин, метилоранж) в растворы кислот HCI, H2SO4
- 22. ДЕЙСТВИЕ КИСЛОТ НА ИНДИКАТОРЫ Вывод: в растворах кислот индикаторы изменяют свой цвет одинаково ( определяют ионы
- 23. Действие какого индикатора наблюдаем? Кислота вода щелочь Универсальный индикатор
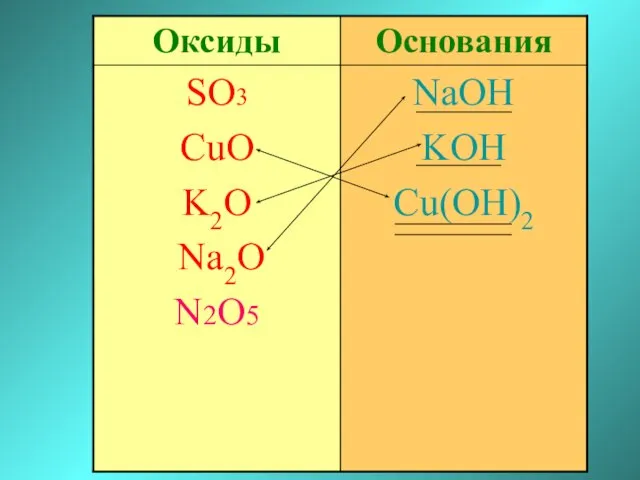
- 24. Составление формулы оксида соответствующего кислоте. Кислота +5 HNO3 Азотная кислота Оксид +5 -2 N O Оксид
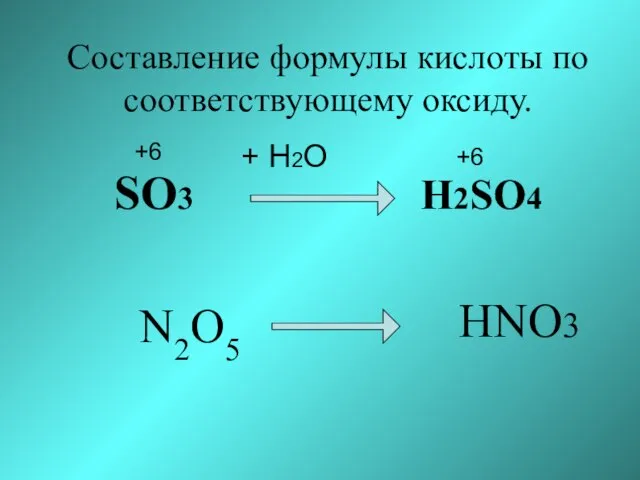
- 25. Составление формулы кислоты по соответствующему оксиду. SO3 H2SO4 + H2O +6 +6 N2O5 HNO3
- 26. Уксусная кислота(древесная кислота) H2SO4 ( купоросное масло) HCl (соляной спирт) HNO3 (селитряная водка) H2CO3 (содовая вода)
- 27. Тест по теме «КИСЛОТЫ»
- 28. 1. Выберите группу веществ, в которой указаны только формулы кислот. а) НСL, H2 O, H2 CO3
- 29. 2. Выберите группу, в которой указаны формулы только кислородсодержащих кислот а)НСL, Н2 SО4 , НNO3 б)Н2
- 30. 3. Выберите группу, в которой указаны формулы только одноосновных кислот а) НСL, НNO3, НFа б) Н2
- 31. 4. Под действием растворов кислот лакмус синий становится: а) малиновым б) не изменяет окраску в) красным
- 32. 5. «Купоросным маслом» называют: а)Соляную кислоту HСL б)Азотную кислоту HNO3 в)Фосфорную кислоту H3PO4 г)Серную кислоту H2SO4
- 33. 6. При разбавлении кислоты: а)Воду приливают к кислоте б)Кислоту приливают к воде в)Воду и кислоту смешивают
- 34. 7.Формула оксида, соответствующего H2SO4? SO2 2) SO3 3)SiO2 4)CO2 8.Формула кислоты, соответствующей N2O3? 1) HNO3 2)
- 36. Скачать презентацию




























 Азотная кислота
Азотная кислота Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Игра Что? Где? Когда?. Химия
Игра Что? Где? Когда?. Химия Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Индиго-краситель
Индиго-краситель Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Макро- и микромир
Макро- и микромир Коррозия металлов
Коррозия металлов Сказка о братьях карбонатах
Сказка о братьях карбонатах Взаимодействие атомов элементов-неметаллов между собой
Взаимодействие атомов элементов-неметаллов между собой Полиамиды (ПА)
Полиамиды (ПА) Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Способы выражения концентраций растворов
Способы выражения концентраций растворов Кислородсодержащие органические соединения
Кислородсодержащие органические соединения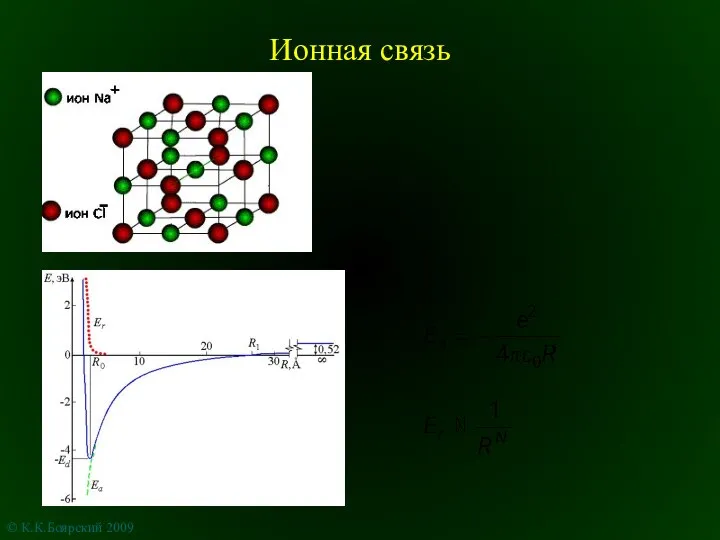 Ионная связь
Ионная связь Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Карбоновые кислоты, их строение, номенклатура, получение и свойства
Карбоновые кислоты, их строение, номенклатура, получение и свойства Уравнение состояния идеального газа
Уравнение состояния идеального газа Шаблон для презентации по химии
Шаблон для презентации по химии Перициклические реакции
Перициклические реакции Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Катализ в нефтепереработке
Катализ в нефтепереработке Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Жиры
Жиры Скорость химических реакций
Скорость химических реакций 1666603286718__4v20ts
1666603286718__4v20ts Основы МКТ
Основы МКТ