Содержание
- 2. Аминокислоты Пептиды
- 3. Аминокислоты – основные структурные единицы, из которых построены молекулы белковых веществ. АМК - бифункциональные соединения, содержащие
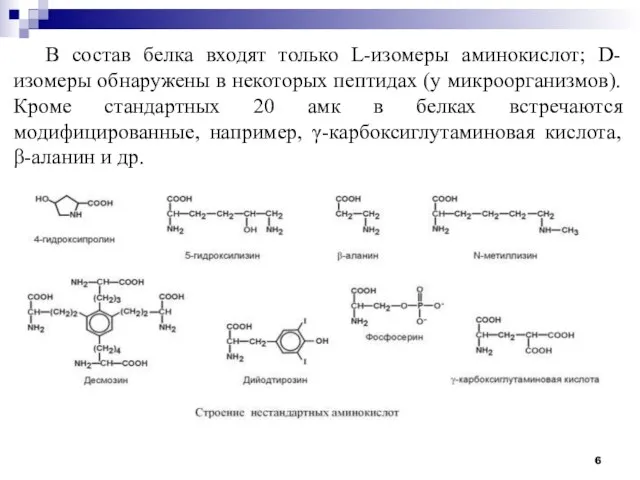
- 6. В состав белка входят только L-изомеры аминокислот; D-изомеры обнаружены в некоторых пептидах (у микроорганизмов). Кроме стандартных
- 7. Кислотно-основные свойства АМК Все амк в растворах существуют в виде биполярного иона (цвиттер-иона), эти вещества амфолиты.
- 8. В воде амк растворяются лучше, чем в других менее полярных растворителях. В водных растворах амк обладают
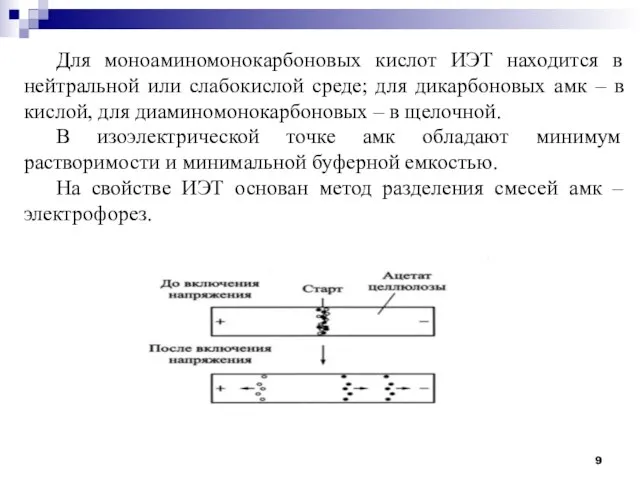
- 9. Для моноаминомонокарбоновых кислот ИЭТ находится в нейтральной или слабокислой среде; для дикарбоновых амк – в кислой,
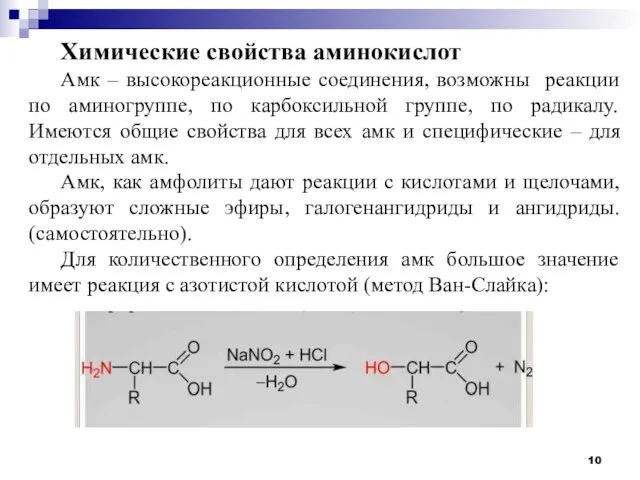
- 10. Химические свойства аминокислот Амк – высокореакционные соединения, возможны реакции по аминогруппе, по карбоксильной группе, по радикалу.
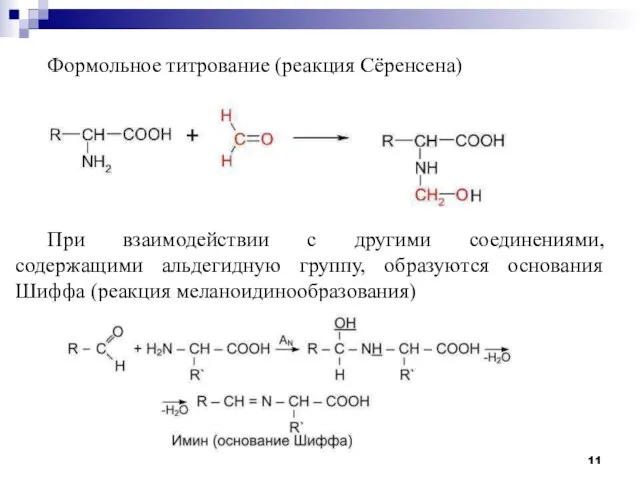
- 11. Формольное титрование (реакция Сёренсена) При взаимодействии с другими соединениями, содержащими альдегидную группу, образуются основания Шиффа (реакция
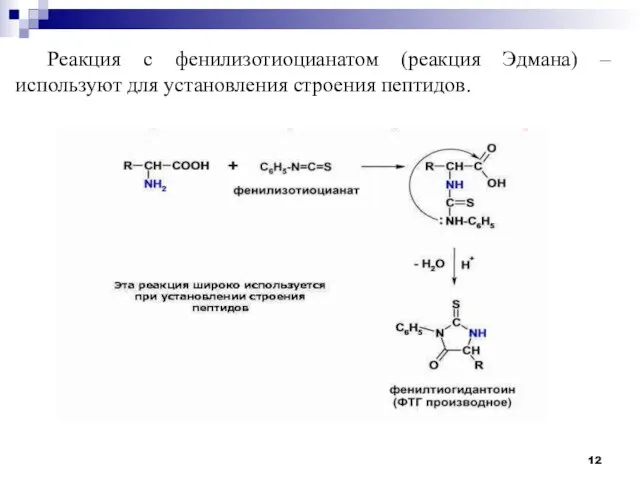
- 12. Реакция с фенилизотиоцианатом (реакция Эдмана) – используют для установления строения пептидов.
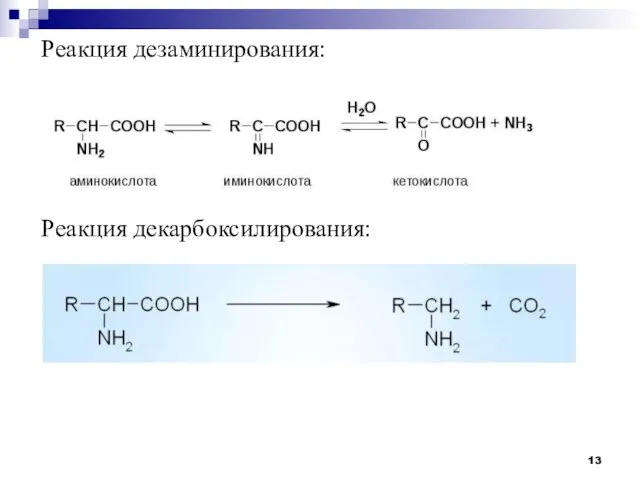
- 13. Реакция дезаминирования: Реакция декарбоксилирования:
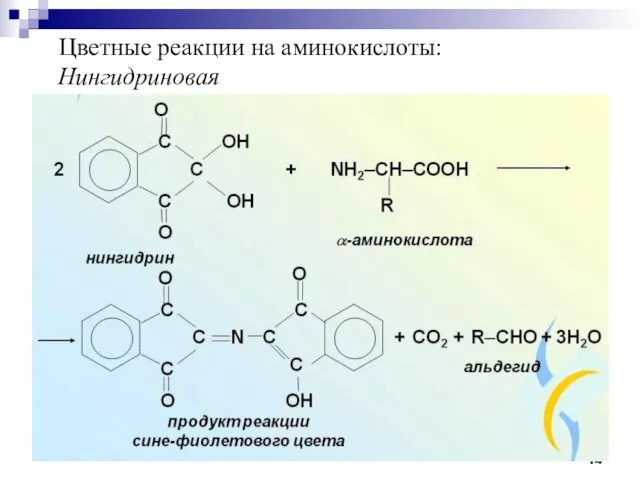
- 14. Цветные реакции на аминокислоты: Нингидриновая
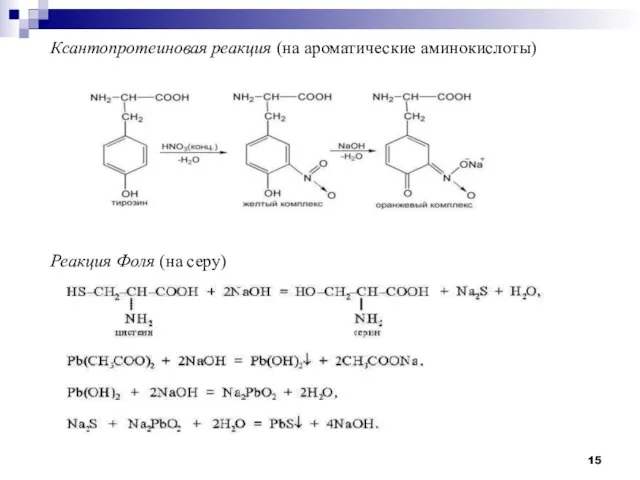
- 15. Ксантопротеиновая реакция (на ароматические аминокислоты) Реакция Фоля (на серу)
- 16. Реакция Адамкевича (на триптофан) при добавлении к раствору концентрированных уксусной и серной кислот образуется фиолетово-красное кольцо.
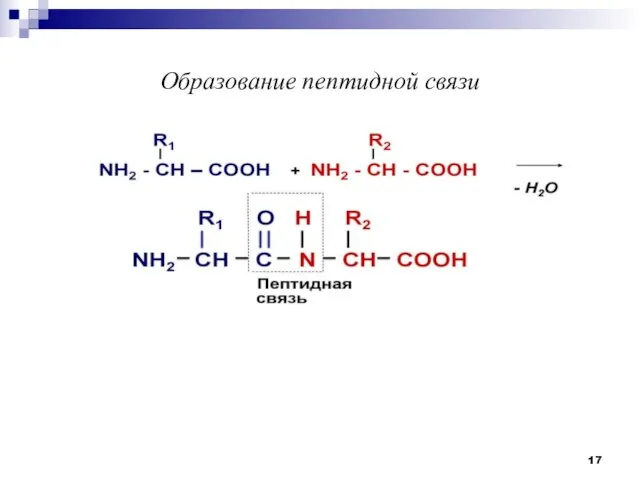
- 17. Образование пептидной связи
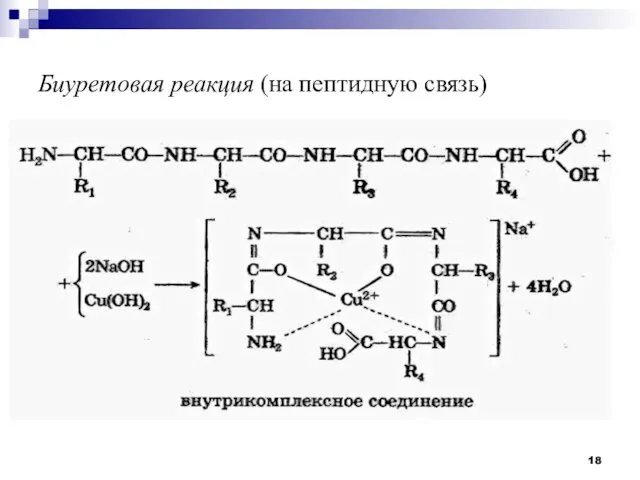
- 18. Биуретовая реакция (на пептидную связь)
- 19. Биологическое значение аминокислот Незаменимые амк – не могут быть синтезированы в организме человека и обязательно должны
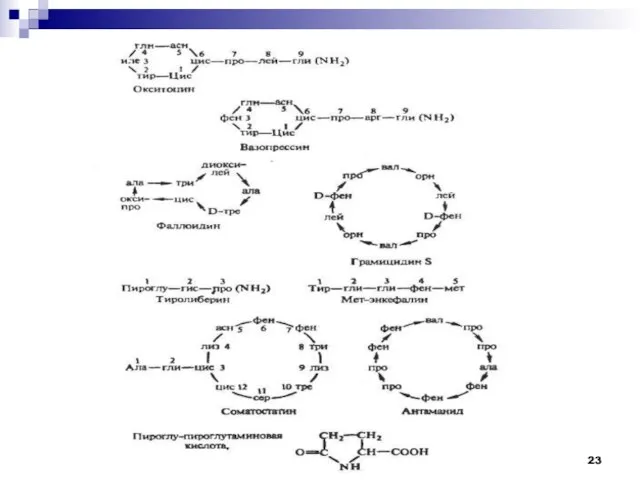
- 20. Пептиды – это низкомолекулярные органические соединения, в которых аминокислоты связываются между собой пептидной или амидной связью
- 21. Глутатион – состоит из глутаминовой кислоты, цистеина и глицина, легко переходит из восстановленной в окисленную (S-S)
- 22. Еще один важный дипептид - карнозин Препятствует накоплению и устраняет продукты перекисного окисления липидов, участвует в
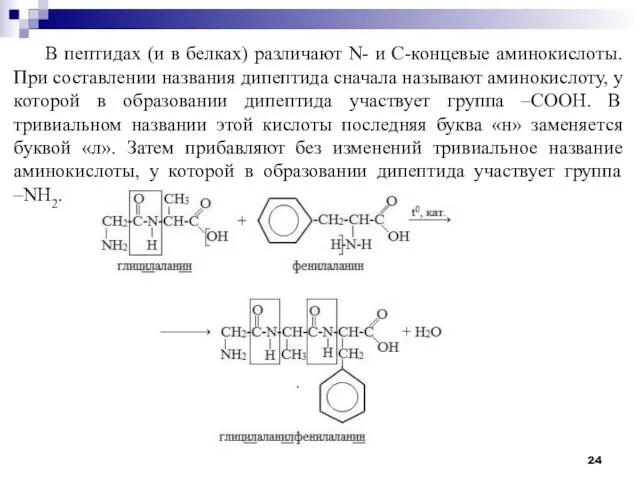
- 24. В пептидах (и в белках) различают N- и C-концевые аминокислоты. При составлении названия дипептида сначала называют
- 26. Скачать презентацию











 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества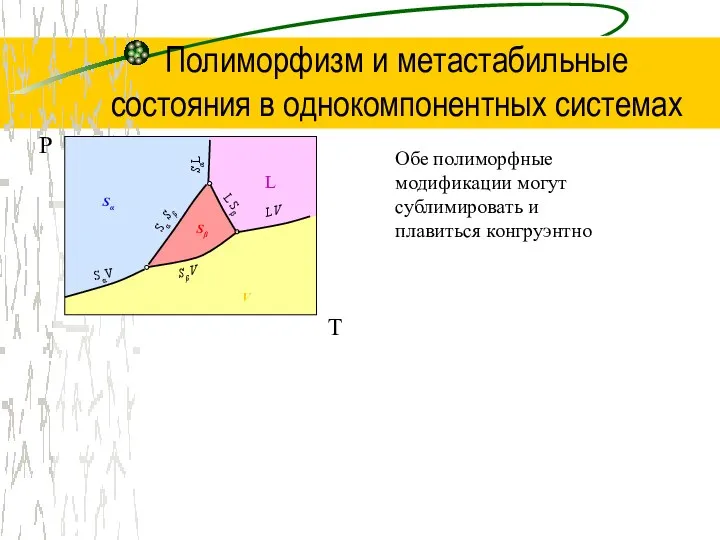 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі