Слайд 2Цели урока
создание условий для:
- формирования у учащихся знаний о разновидностях органических веществ,

их строении на примере аминов, аминокислот и белков; о значении органических веществ в жизнедеятельности человеческого организма
- формирование навыков применять правила систематической международной номенклатуры как средства различения и идентификации веществ по их составу и строению
- формирование личностных результатов – готовности и способности к образованию и самообразованию в течение всей жизни
- формирование метапредметных результатов – умение самостоятельно формулировать цели деятельности, продуктивно общаться и взаимодействовать, готовность к самостоятельной информационно-познавательной деятельности, умение излагать свои мысли.
Слайд 3Амины
Производные аммиака, в молекуле которого один или несколько атомов водорода замещены на

углеводородные радикалы
Слайд 4
У первичных аминов азот связан только с одним углеводородным радикалом
У вторичных аминов

азот связан с двумя радикалами
У третичных аминов азот связан с тремя радикалами
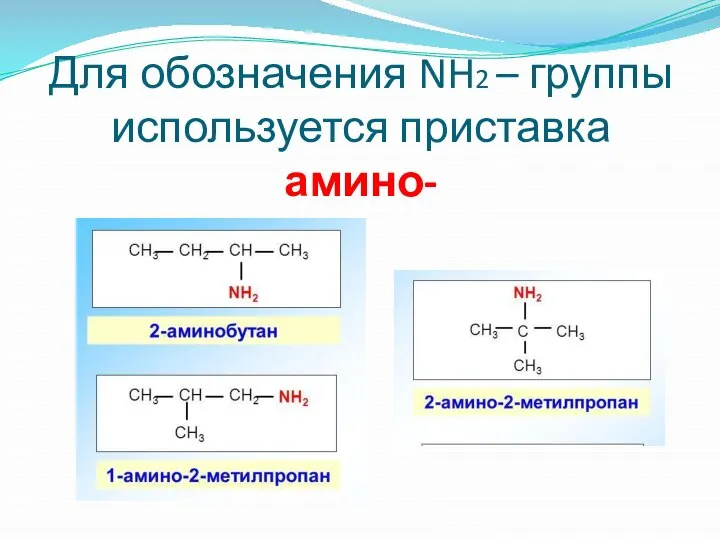
Слайд 5Для обозначения NH2 – группы используется приставка
амино-
Слайд 6Вторичные и третичные амины называют используя рациональную номенклатуру: в алфавитном порядке перечисляются
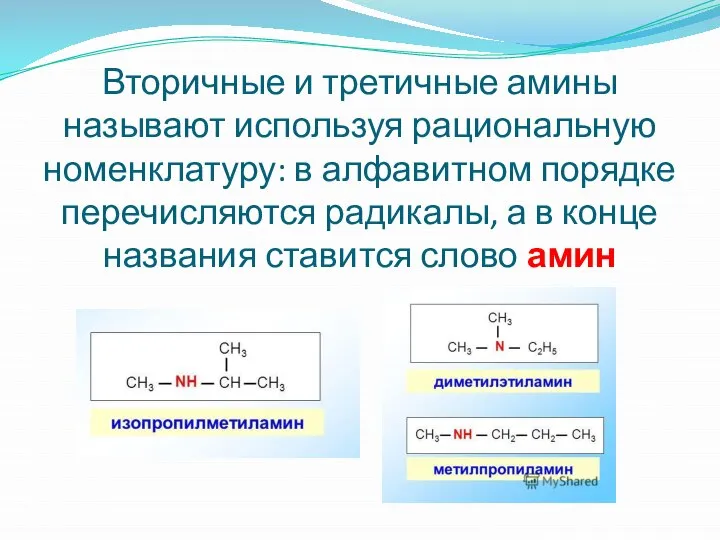
радикалы, а в конце названия ставится слово амин
Слайд 7Физические свойства
Первые амины – газы с характерным запахом, хорошо растворимы в воде.
Первичные

и вторичные амины менее летучие, чем третичные, и лучше растворимы.
Слайд 9Качественная реакция на амины
Разрушение азотистой кислотой первичных аминов:

Слайд 13Аминокислоты
Производные карбоновых кислот, содержащие в своем составе одну или несколько аминогрупп

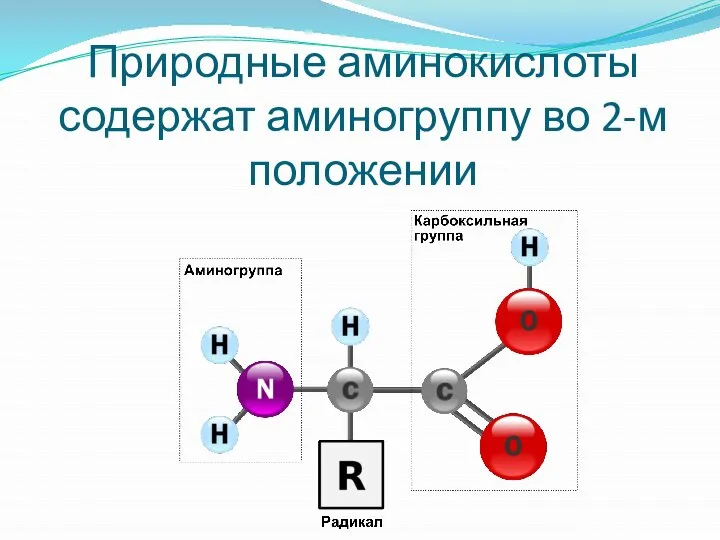
Слайд 14Природные аминокислоты содержат аминогруппу во 2-м положении
Слайд 15В названии аминокислот указывается положение и название аминогруппы, а затем карбоновая кислота

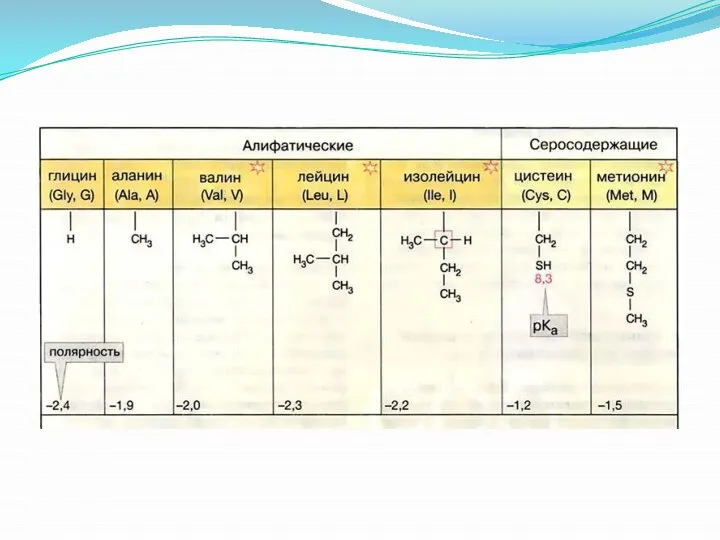
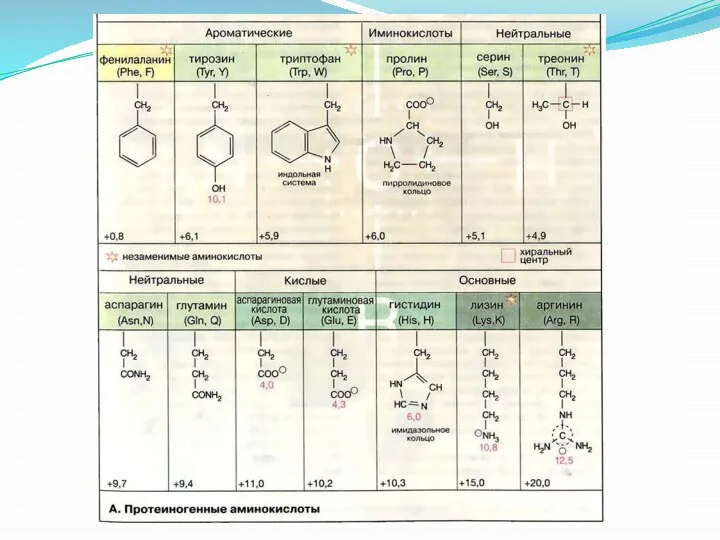
Слайд 16Из белков выделено 20 аминокислот:

Слайд 19Химические свойства
Аминокислоты – амфотерные вещества

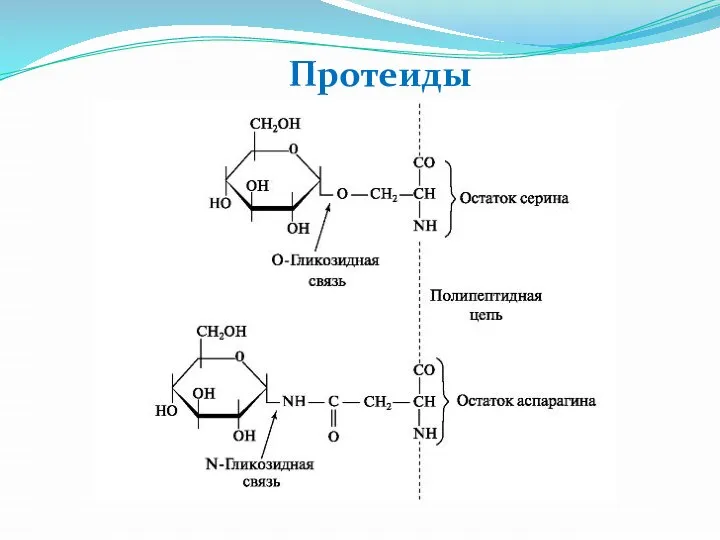
Слайд 20Белки
Биологические полимеры, состоящие из остатков аминокислот

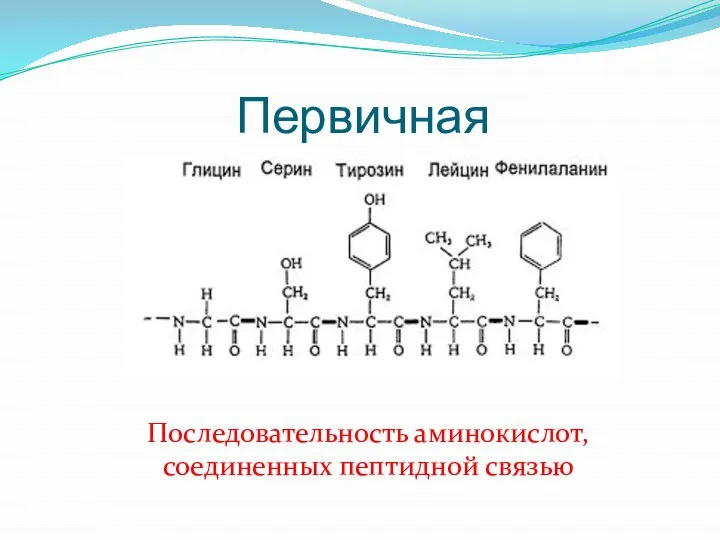
Слайд 25Первичная
Последовательность аминокислот, соединенных пептидной связью
Слайд 26Вторичная
Образована одной полипептидной цепью в результате возникновения водородных связей между карбоксильными группами
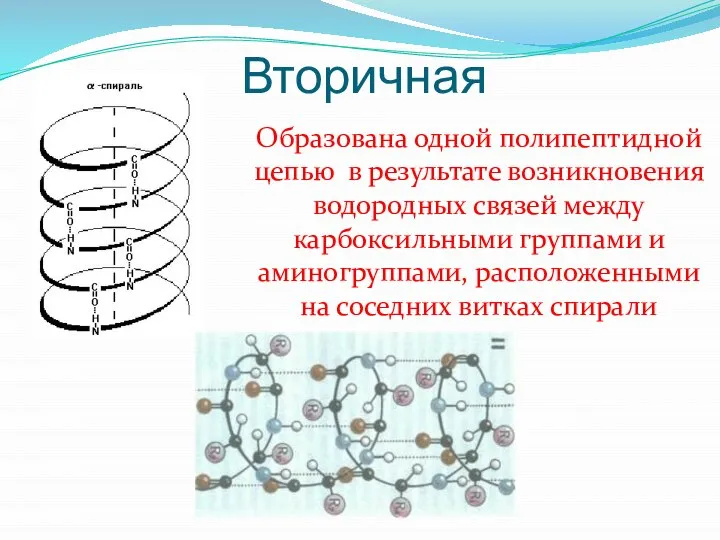
и аминогруппами, расположенными на соседних витках спирали
Слайд 27Третичная
Образована полипептидными цепочками, по-разному расположенными в пространстве за счет водородных связей, ионного

и гидрофобного взаимодействия
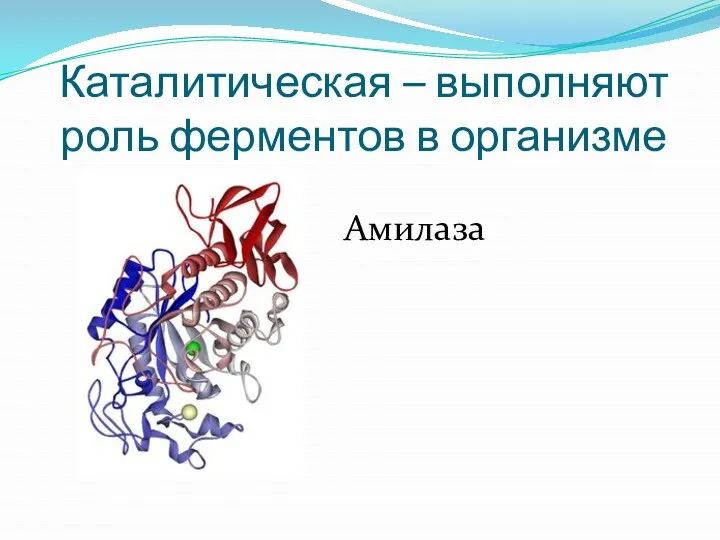
Слайд 30Каталитическая – выполняют роль ферментов в организме
Амилаза
Слайд 31Защитная – выполняют роль антител в организме

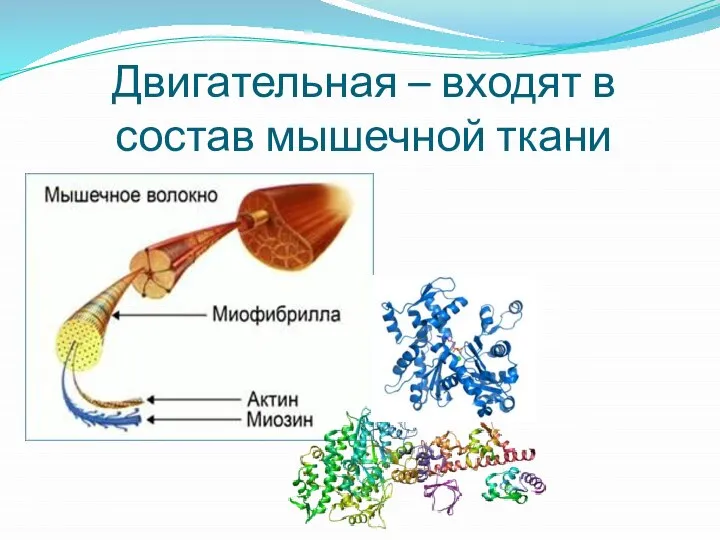
Слайд 32Двигательная – входят в состав мышечной ткани
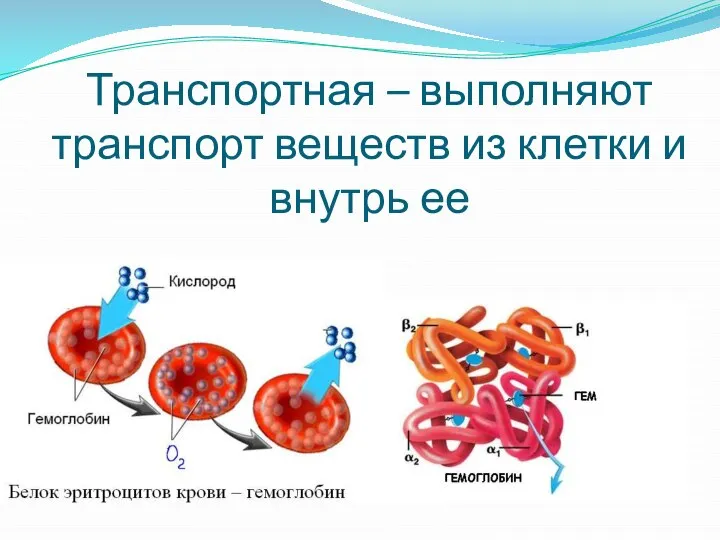
Слайд 33Транспортная – выполняют транспорт веществ из клетки и внутрь ее
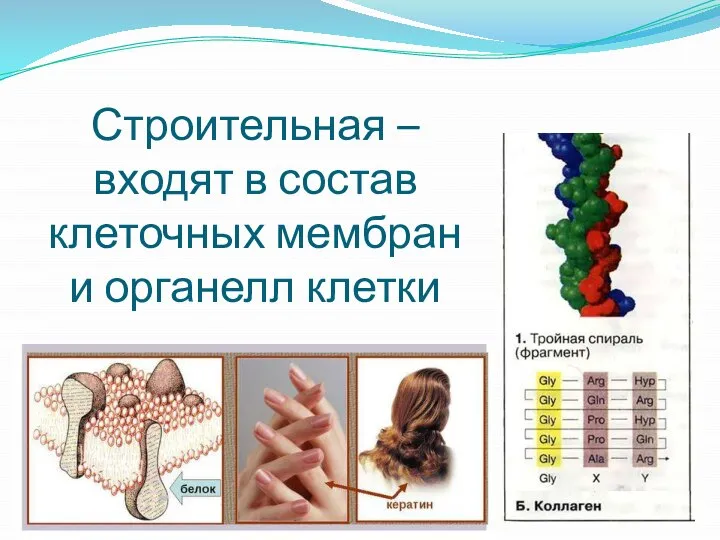
Слайд 34Строительная – входят в состав клеточных мембран и органелл клетки
Слайд 35Энергетическая – при расщеплении
1 г белка выделяется 17,6 кДж энергии
(4
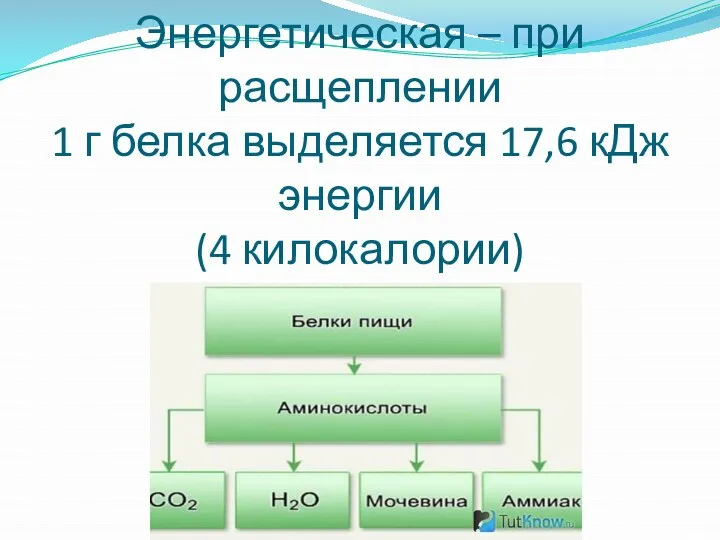
килокалории)
Слайд 42Биуретовая реакция
Качественная реакция на пептидные связи
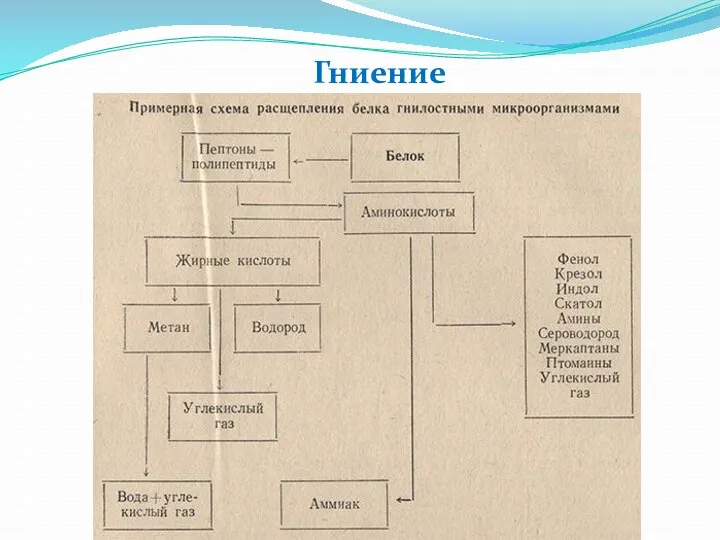
Белок
Гидроксид меди (II)
Внутрикомплексное соединение

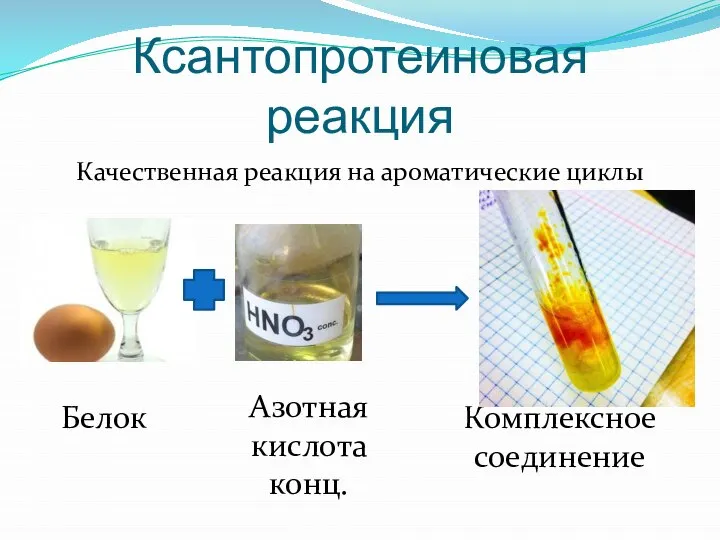
Слайд 43Ксантопротеиновая реакция
Качественная реакция на ароматические циклы
Белок
Азотная кислота конц.
Комплексное соединение
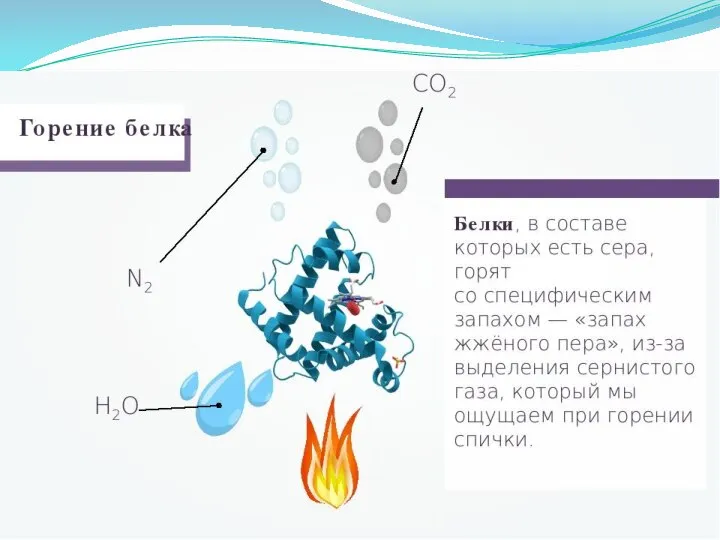
Слайд 44Реакция на серу (Фоля)
Белок
Нитрат свинца
Плюмбат серы





































 Щелочные металлы
Щелочные металлы Основы химической термодинамики. Основные понятия химической термодинамики. Лекция 1
Основы химической термодинамики. Основные понятия химической термодинамики. Лекция 1 Введение в дисциплину Процессы и аппараты химической технологии
Введение в дисциплину Процессы и аппараты химической технологии Химия и косметика
Химия и косметика Классификация веществ
Классификация веществ Аммиак. Соли аммония
Аммиак. Соли аммония Лекарственные средства – производные пиримидин 2,4,6-триона
Лекарственные средства – производные пиримидин 2,4,6-триона Спирты (10 класс)
Спирты (10 класс) Галогены. Их значение в жизни человека
Галогены. Их значение в жизни человека 1bb1fde703934b8cb10cb70170970502
1bb1fde703934b8cb10cb70170970502 Валентность химических элементов
Валентность химических элементов Коррозия металлов
Коррозия металлов Введение в органическую химию
Введение в органическую химию Химическая связь
Химическая связь Биосенсоры. Основные принципы (лекция 2)
Биосенсоры. Основные принципы (лекция 2) Химическая реакция в потоке в одномерном случае. Уравнение неразрывности
Химическая реакция в потоке в одномерном случае. Уравнение неразрывности бирюза
бирюза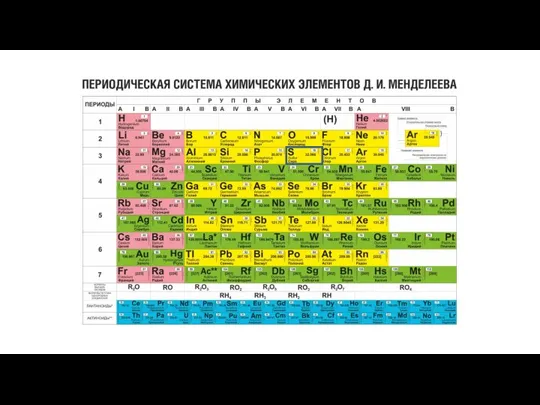 Периодическая система химических элементов Д.И. Меделеева
Периодическая система химических элементов Д.И. Меделеева Spectroscopy. U.V. Lect.2
Spectroscopy. U.V. Lect.2 История и методология химии
История и методология химии Полимеры
Полимеры Карбоновые кислоты. Д.И. Менделеев
Карбоновые кислоты. Д.И. Менделеев Разработка электронных образовательных ресурсов в естественнонаучном образовании бакалавров направления Химия
Разработка электронных образовательных ресурсов в естественнонаучном образовании бакалавров направления Химия Синтез макромолекул
Синтез макромолекул Углерод
Углерод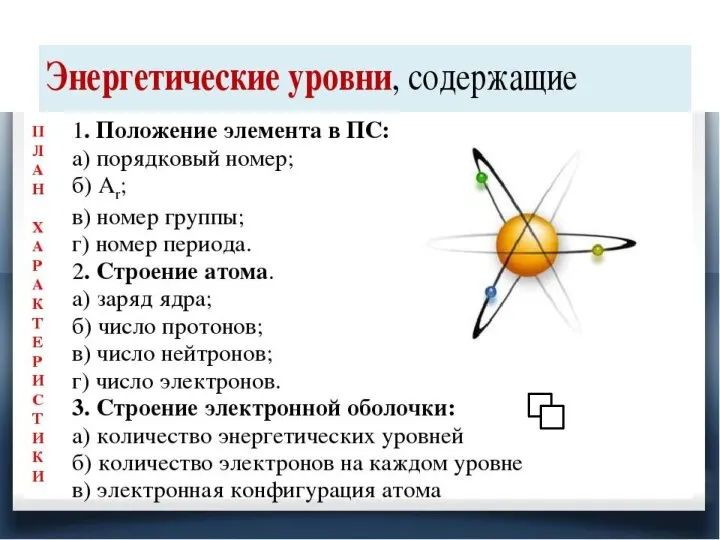 Закономерности изменения свойств атомов химических элементов
Закономерности изменения свойств атомов химических элементов Свойства кислорода. Оксиды
Свойства кислорода. Оксиды Презентация на тему Свойства простых веществ
Презентация на тему Свойства простых веществ