Слайд 2Молекулярная формула
Электронная формула
Вид химической связи
Тип кристаллической решетки
Dвозд. =
Растворимость в воде ……
Запах ……

Слайд 3Химические свойства
N-3H3 - восстановитель
t
NH3 →
NH3 + O2 → N2 +
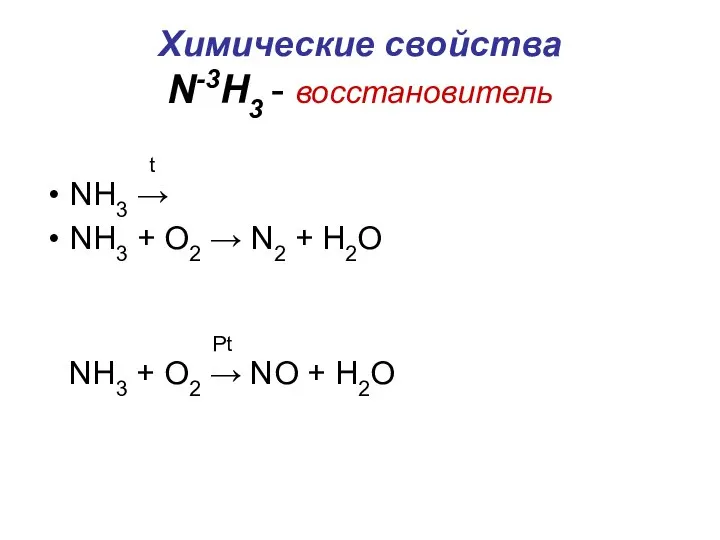
H2O
Pt
NH3 + O2 → NO + H2O
Слайд 4Взаимодействие с водой
NH3 + HOH ↔
H: N-δ: Н + Н+δ:О-δ: Н→
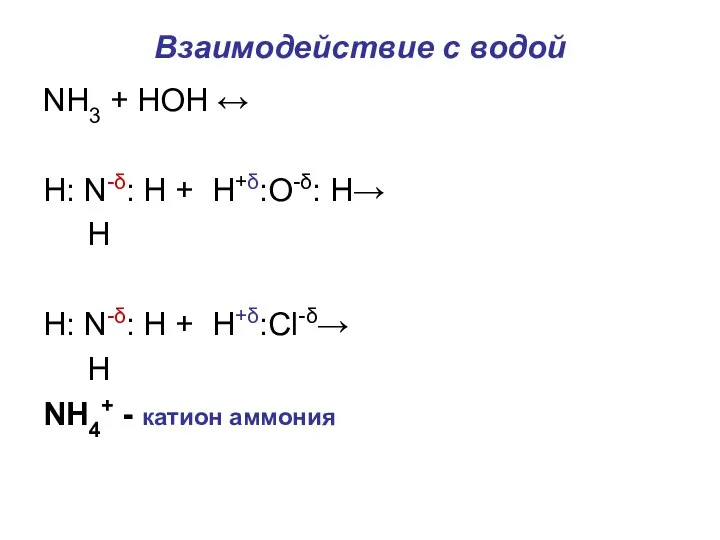
Н
H: N-δ: Н + Н+δ:Cl-δ→
Н
NH4+ - катион аммония
Слайд 5Получение аммиака в лаборатории
NH4Cl + Ca(OH)2 = CaCl2 + NH3↑+ H2O
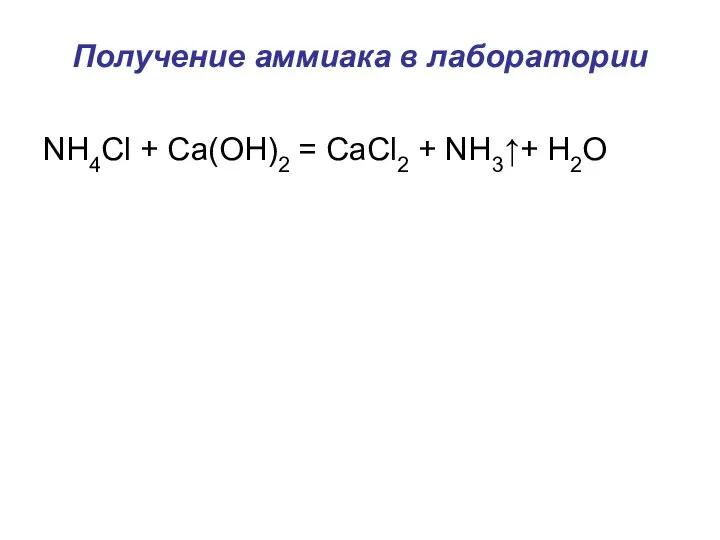
Слайд 6Соли аммония- сложные вещества, состоящие из ………………..
Закончите уравнение реакции
NH3 + H2SO4

=
Напишите уравнения реакций получения нитрата аммония
А)
Б)
Слайд 7Используя таблицу растворимости, сделайте вывод, как ведут себя соли аммония в воде
Общие

свойства солей:
а) взаимодействие с кислотами
(NH4)2CO3 + HCl =
б) взаимодействие с солями
(NH4)2SO4 + BaCl2 =
в ) взаимодействие с щелочами
NH4Cl + NaOH =
г) термическое разложение
NH4Cl → NH3↑+ HCl
Слайд 8Качественная реакция
NH4+ + OH- = NH3↑+ H2О

Слайд 9Проверь свои знания:
Предложите вещества, соответствующие данной схеме и осуществите превращения
N0 ↔

N-3 → N+2 → N+4
Запишите молекулярные и ионные уравнения реакций следующих превращений:
NH3 → NH4Cl → NH4NO3 → NH3
Какие свойства гидрокарбоната аммония используются при добавлении его в тесто при выпечке кондитерских изделий? Запишите уравнение реакции
Слайд 10Задача:
Вычислите массу и объем (н.у.) аммиака, который получится при взаимодействии 20г хлорида

аммония с 7,4г гидроксида кальция.









 Металлы и их соединения
Металлы и их соединения Кислоты. Химический диктант. 8 класс
Кислоты. Химический диктант. 8 класс Соли
Соли Массовая доля элемента в веществе
Массовая доля элемента в веществе Природные источники углеводорода
Природные источники углеводорода Протравка стекла с помощью ионного обмена
Протравка стекла с помощью ионного обмена Свойство металлов и сплавов
Свойство металлов и сплавов Дисперсные системы
Дисперсные системы Диены. Понятие о диенах
Диены. Понятие о диенах Аппаратурное оформление процесса гидроочистки нефтяных фракций
Аппаратурное оформление процесса гидроочистки нефтяных фракций Презентация для заочников
Презентация для заочников Электролиз и его применение
Электролиз и его применение Генетические ряды металлов и неметаллов
Генетические ряды металлов и неметаллов Классификация реагентов и реакции в органической химии
Классификация реагентов и реакции в органической химии Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Железо
Железо Среды для культивирования эмбрионов-история разработки и составы
Среды для культивирования эмбрионов-история разработки и составы Массовая доля элемента в веществе
Массовая доля элемента в веществе Полисахариды
Полисахариды 9-14 Реакции в растворах электролитов
9-14 Реакции в растворах электролитов Физические и фазовые состояния полимеров
Физические и фазовые состояния полимеров Алкены
Алкены 8-11 2 валентность
8-11 2 валентность Бериллий (Beryllium) Be
Бериллий (Beryllium) Be Арены. Бензол
Арены. Бензол Презентация на тему Металлы в организме человека
Презентация на тему Металлы в организме человека  Количество вещества. Моль
Количество вещества. Моль Изомерия
Изомерия