Содержание
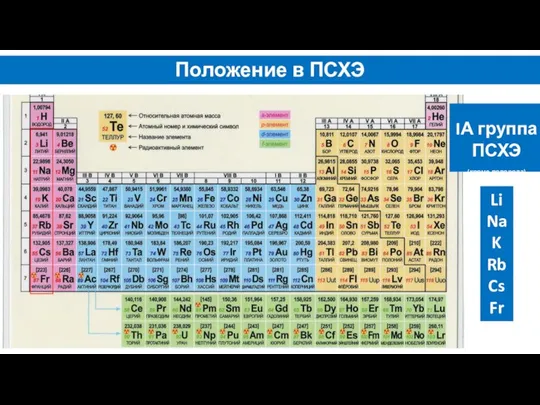
- 2. Положение в ПСХЭ IА группа ПСХЭ (кроме водорода) Li Na K Rb Cs Fr
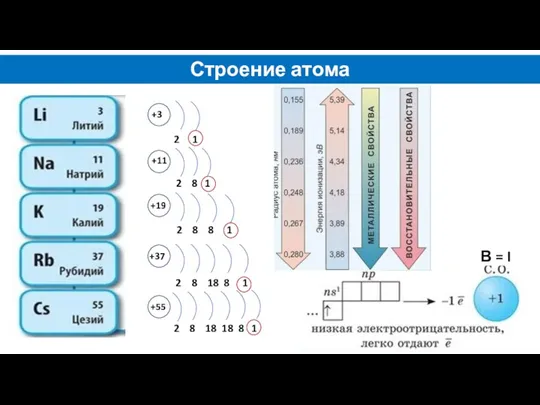
- 3. Строение атома +3 +11 +19 +37 +55 В = I 2 1 2 8 1 2
- 4. Щелочные металлы в природе (только в виде соединений)
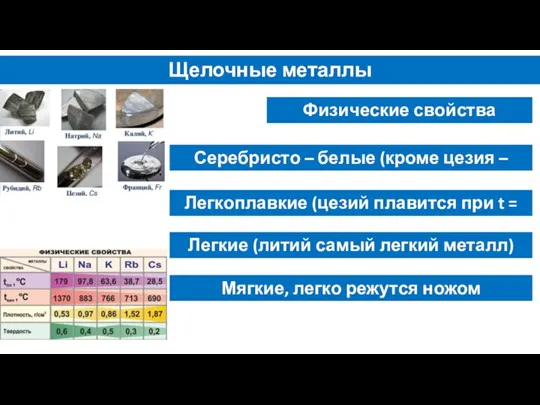
- 5. Щелочные металлы Серебристо – белые (кроме цезия – желтый) Легкоплавкие (цезий плавится при t = 290С)
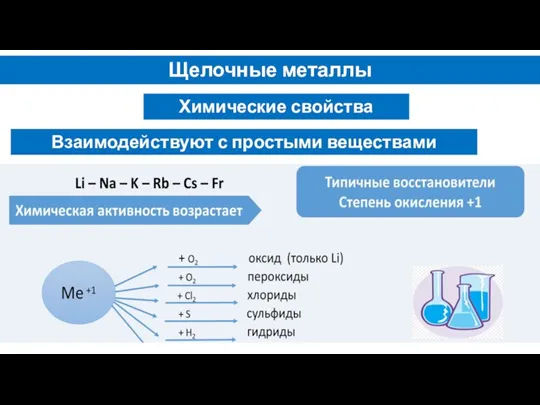
- 6. Щелочные металлы Химические свойства Взаимодействуют с простыми веществами
- 7. Щелочные металлы 4Li + O2 = 2Li2O 2Na + O2 = Na2O2 2Na + Cl2 =
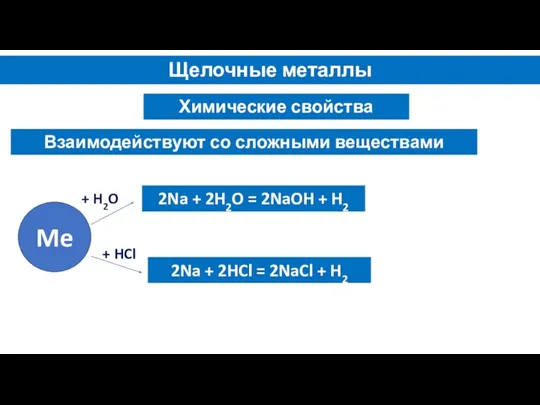
- 8. Щелочные металлы Химические свойства Взаимодействуют со сложными веществами Me + H2O + HCl 2Na + 2H2O
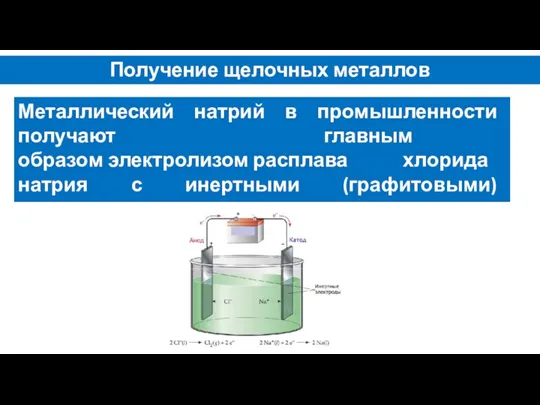
- 9. Получение щелочных металлов Металлический натрий в промышленности получают главным образом электролизом расплава хлорида натрия с инертными
- 10. Качественный анализ катионы щелочных металлов окрашивают пламя в характерные цвета Соли лития придают пламени карминово-красный цвет,
- 12. Скачать презентацию



 Ароматические углеводороды. Строение молекулы бензола. Физические свойства
Ароматические углеводороды. Строение молекулы бензола. Физические свойства Молекулярно-массовое распределение
Молекулярно-массовое распределение Изомерия. Виды изомерии
Изомерия. Виды изомерии Презентация на тему Ионные уравнения
Презентация на тему Ионные уравнения  Основания, состав и классификация
Основания, состав и классификация Типы кристаллических решеток. Тест
Типы кристаллических решеток. Тест СПИРТЫ, ФЕНОЛЫ
СПИРТЫ, ФЕНОЛЫ Химические методы анализа. Аналитические методы контроля в техносферной безопасности. Лекция 6
Химические методы анализа. Аналитические методы контроля в техносферной безопасности. Лекция 6 Теория электролитической диссоциации
Теория электролитической диссоциации Реакции ионного обмена составление ионных уравнений
Реакции ионного обмена составление ионных уравнений 01. Химический состав
01. Химический состав Алканы. Задания
Алканы. Задания Спирты. Непредельные спирты
Спирты. Непредельные спирты История развития химии
История развития химии Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Цинк (Zn). Свойства
Цинк (Zn). Свойства Предельные одноатомные спирты
Предельные одноатомные спирты Физическая химия растворов электролитов
Физическая химия растворов электролитов Основания. 8 класс
Основания. 8 класс Kristālisku vielu uzbūve
Kristālisku vielu uzbūve Соединения серы
Соединения серы Строение атома. Химия, 8 класс
Строение атома. Химия, 8 класс Органическая химия. Йенс Якоб Берцелиус (1779 - 1848)
Органическая химия. Йенс Якоб Берцелиус (1779 - 1848) Типы химических реакций. Класс оксиды
Типы химических реакций. Класс оксиды Формы существования химических элементов. Формы существования химических элементов
Формы существования химических элементов. Формы существования химических элементов lektsia_7
lektsia_7 Предмет органической химии
Предмет органической химии Хром. Месторождения
Хром. Месторождения