Содержание
- 2. Открытие азота 12 сентября 1772 года — Даниель Резерфорд 1771 - 1773 гг. — Г. Кавендиш
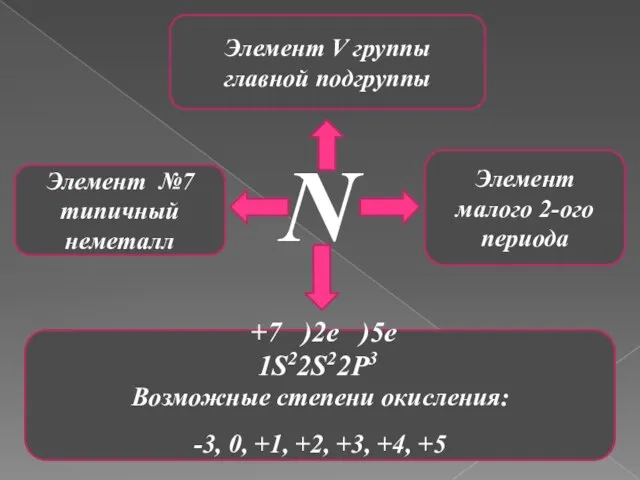
- 3. N Элемент V группы главной подгруппы Элемент №7 типичный неметалл Элемент малого 2-ого периода +7 )2e
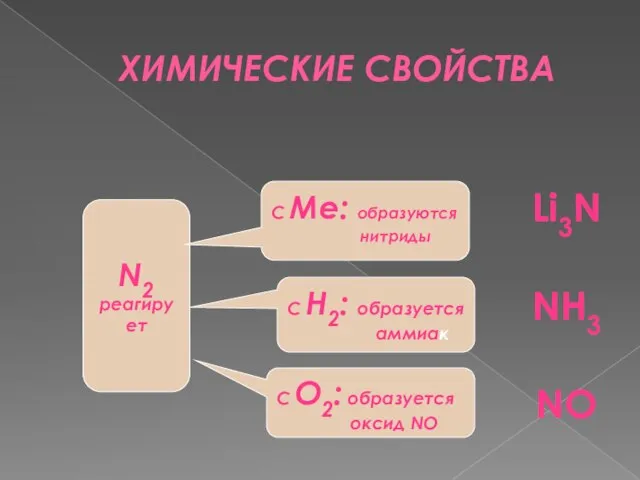
- 4. ХИМИЧЕСКИЕ СВОЙСТВА N2 реагирует С Ме: образуются нитриды С Н2: образуется аммиак С О2: образуется оксид
- 5. ФИЗИЧЕСКИЕ СВОЙСТВА N2 Газ без вкуса, цвета, запаха. Плохо растворим в воде. Легче воздуха.
- 6. Азот присутствует во всех живых организмах (1-3% на сухую массу), являясь важнейшим биогенным элементом. Он входит
- 7. Нахождение в природе По распространенности в земной коре азот занимает 17-е место, на его долю приходится
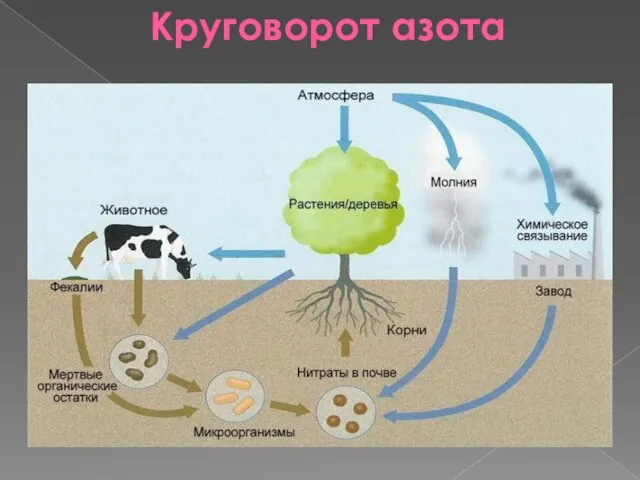
- 8. Круговорот азота
- 9. Поставщик связанного азота в природе Главный поставщик связанного азота в природе — бактерии: благодаря им связывается
- 10. Некоторое количество азота переводится в связанное состояние во время грозы Электрический разряд нагревает атмосферу вокруг себя,
- 11. Получение азота в промышленности: фракционная перегонка жидкого воздуха ОАО «Невинномысский Азот" Завод по производству азота из
- 12. Получение азота в лаборатории (разложением солей аммония) 1. Разложением нитрита аммония NH4NO2=N2 + 2H2O 2. Разложением
- 13. N2 Жидкий азот в медицине Синтез аммиака Производство удобрений Синтез азотной кислоты Создание инертной среды
- 14. В косметологии Для создания инертной среды при опытах Как хладагент Для синтеза аммиака Применение N 2
- 15. Применение соединений азота производство минеральных удобрений производство взрывчатых веществ производство лекарственных препаратов
- 17. Скачать презентацию











 Минерал Александрит
Минерал Александрит Soft Matter. Emulsions
Soft Matter. Emulsions Химические свойства металлов. Электрохимический ряд напряжения металлов
Химические свойства металлов. Электрохимический ряд напряжения металлов Фторсодержащие полимеры
Фторсодержащие полимеры Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Относительная атомная масса
Относительная атомная масса Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Химия в косметике
Химия в косметике Простые вещества – неметаллы. Получение и химические свойства неметаллов
Простые вещества – неметаллы. Получение и химические свойства неметаллов Диффузия золота и свинца
Диффузия золота и свинца Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Основные классы неорганических соединений (урок - семинар)
Основные классы неорганических соединений (урок - семинар) Основы квантовой химии
Основы квантовой химии Презентация на тему Азотная кислота и ее соли (9 класс)
Презентация на тему Азотная кислота и ее соли (9 класс)  Подготовка к олимпиаде по химии. Некоторые идеи составления и решения нестандартны задач
Подготовка к олимпиаде по химии. Некоторые идеи составления и решения нестандартны задач Скорость протекания химических реакций
Скорость протекания химических реакций Белки-1 2020
Белки-1 2020 Рука руку моет. Механизм двух реакций
Рука руку моет. Механизм двух реакций Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Энергетические уровни
Энергетические уровни Карбоновые кислоты
Карбоновые кислоты Химияның негізгі түсініктері мен зандары
Химияның негізгі түсініктері мен зандары Химия в быту
Химия в быту Основания. Щелочи – растворимые основания
Основания. Щелочи – растворимые основания Химические методы. Золь-гель метод
Химические методы. Золь-гель метод Многоатомные спирты
Многоатомные спирты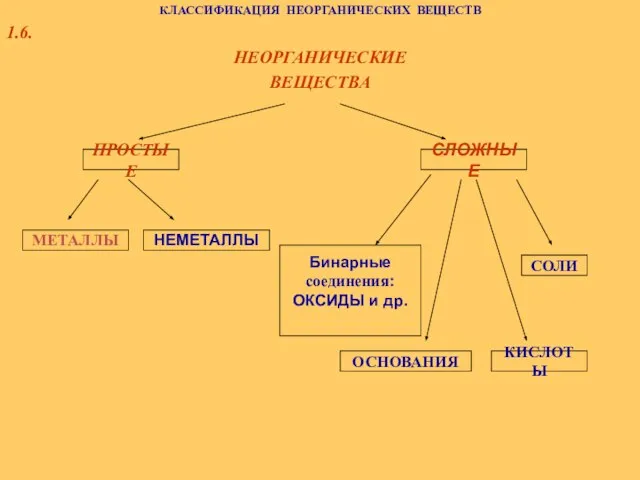 Классификация неорганических веществ
Классификация неорганических веществ