Содержание
- 4. Напишите уравнения реакций между: а) калием и хлором, б) натрием и йодом, в) литием и водой.
- 5. 1. Оксиды щелочных металлов а) физические свойства: б) химические свойства:
- 6. Составьте уравнения реакций оксида калия с водой, оксида натрия с оксидом фосфора(V) К2O + H2O =
- 7. 2. Гидроксиды щелочных металлов а) физические свойства: б) химические свойства: 1) С кислотами: NaOH + HCl
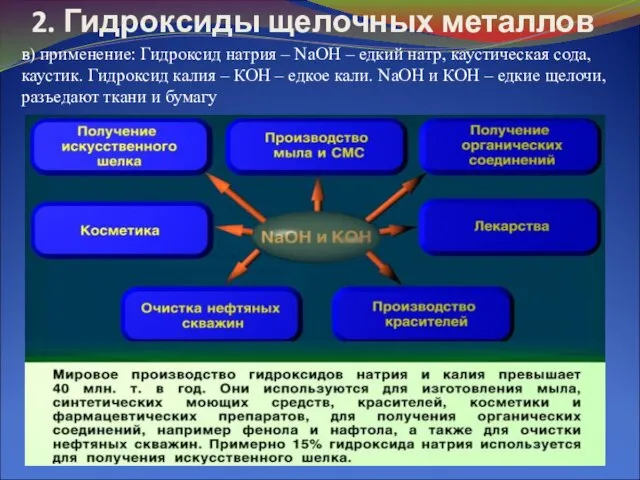
- 8. 2. Гидроксиды щелочных металлов в) применение: Гидроксид натрия – NaOH – едкий натр, каустическая сода, каустик.
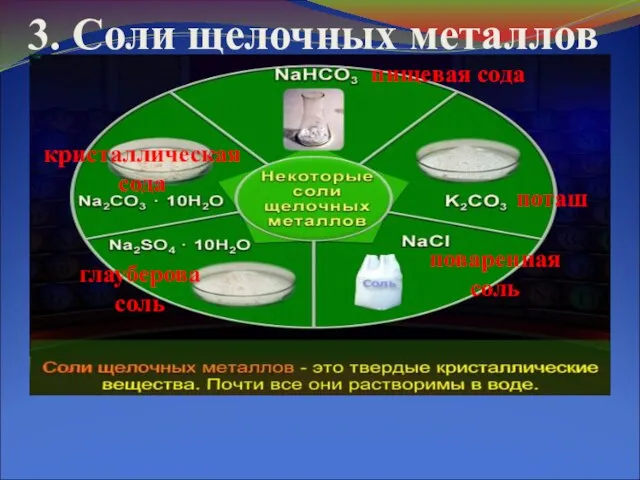
- 9. 3. Соли щелочных металлов пищевая сода поташ поваренная соль глауберова соль кристаллическая сода
- 10. 4. Значение соединений щелочных металлов в жизнедеятельности организмов Ионы натрия и калия играют большую биологическую роль:
- 11. Задание 1 Взрослый человек должен в сутки потреблять с пищей 3,5г ионов калия. Задача. В 100г
- 13. Скачать презентацию







 Метаболизм азота
Метаболизм азота Важнейшие классы неорганических соединений. Соли
Важнейшие классы неорганических соединений. Соли Термохимия. Задания
Термохимия. Задания Кислоты. Классификация. Номенклатура
Кислоты. Классификация. Номенклатура 9-12 Гидролиз солей -
9-12 Гидролиз солей - Получение метанола из синтез-газа
Получение метанола из синтез-газа Предмет органической химии
Предмет органической химии Альдегиды и кетоны
Альдегиды и кетоны Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие
Железоуглеродистые сплавы. Диаграмма равновесного состояния железо-цементит. Фазы и структурные составляющие Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Альдегиды и кетоны
Альдегиды и кетоны Сахароза (С12Н22О11)
Сахароза (С12Н22О11) Классификация реакций в органической химии
Классификация реакций в органической химии Комплексные соединения
Комплексные соединения Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация 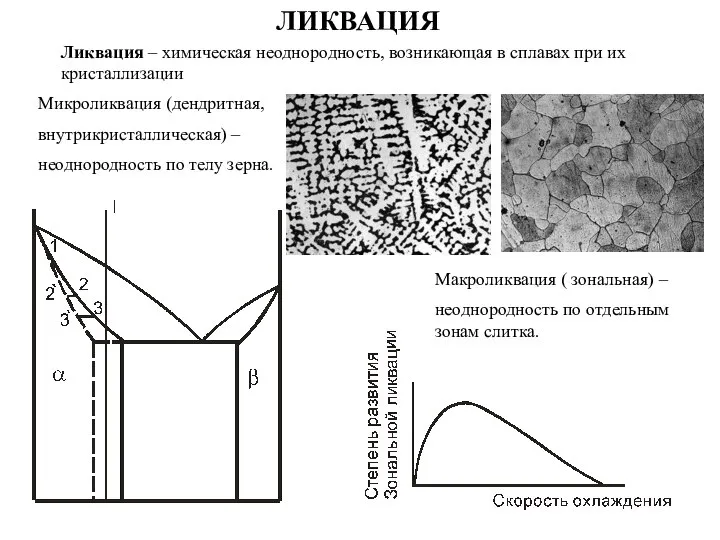 Ликвация. Микроликвация
Ликвация. Микроликвация Синтез-газ
Синтез-газ Реакции замещения
Реакции замещения Синтез 7,7 - дихлоробицикло [4.1.0] гептана
Синтез 7,7 - дихлоробицикло [4.1.0] гептана Углерод и его аллотропные модификации. Органическая химия - химия углерода
Углерод и его аллотропные модификации. Органическая химия - химия углерода Использование элементов модульной технологии на уроках химии
Использование элементов модульной технологии на уроках химии Физические свойства водорода
Физические свойства водорода Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алюминий
Алюминий Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация по Химии "Ковалентная химическая связь"
Презентация по Химии "Ковалентная химическая связь"  Презентация на тему Изотопы
Презентация на тему Изотопы  Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса
Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса