Содержание
- 2. Диаграммы плавкости – это зависимость температуры плавления от состава. При описании равновесий типа «твердое тело –
- 3. Кривые охлаждения (р = const) Кривая охлаждения чистого расплавленного вещества На участке 1–2 происходит охлаждение жидкости,
- 4. Вид диаграмм определяется взаимной нерастворимостью компонентов в жидком и твердом состоянии Все диаграммы плавкости можно разделить
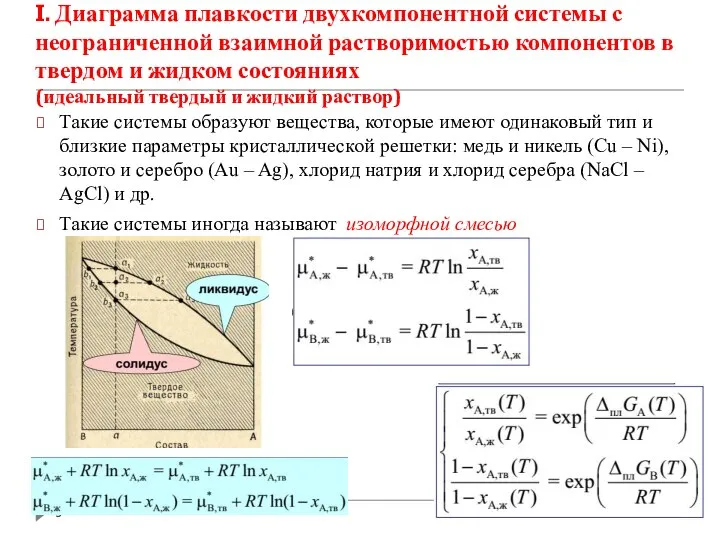
- 5. I. Диаграмма плавкости двухкомпонентной системы с неограниченной взаимной растворимостью компонентов в твердом и жидком состояниях (идеальный
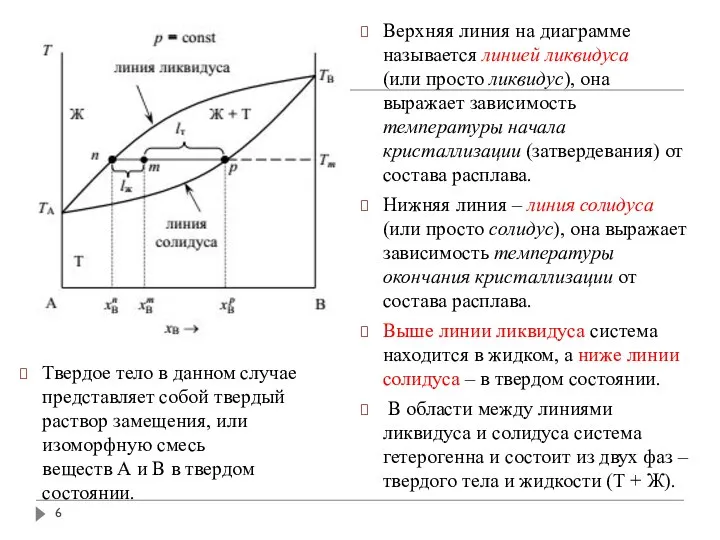
- 6. Твердое тело в данном случае представляет собой твердый раствор замещения, или изоморфную смесь веществ А и
- 7. Температуры начала и окончания кристаллизации зависят от состава расплава, при этом состав выпадающих кристаллов не совпадает
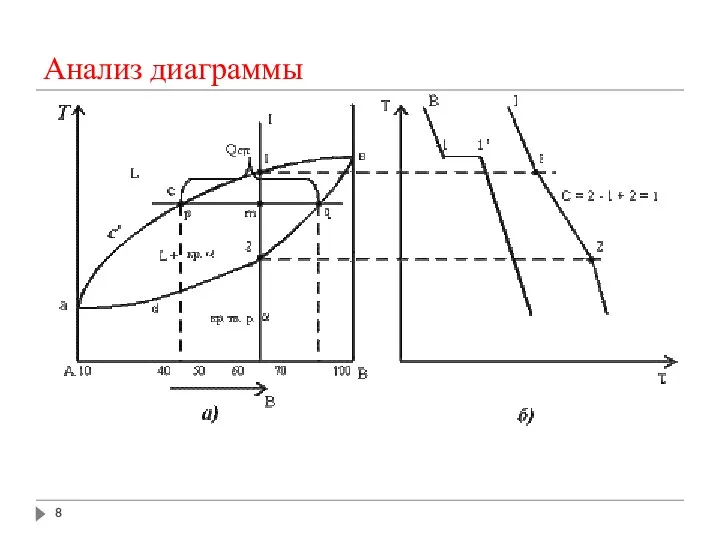
- 8. Анализ диаграммы
- 9. 1. Количество компонентов: К = 2 (компоненты А и В). 2. Число фаз: f = 2
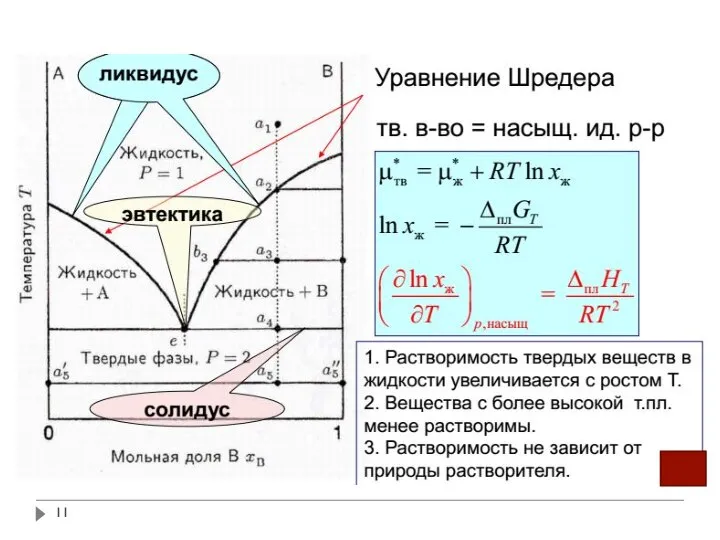
- 10. Диаграмма плавкости вухкомпонентной системы эвтектического типа Такие системы образуют вещества, сильно различающиеся по структуре либо по
- 12. 2) эвтектический расплав имеет состав, промежуточный между составами чистых компонентов. При температуре эвтектики в системе протекает
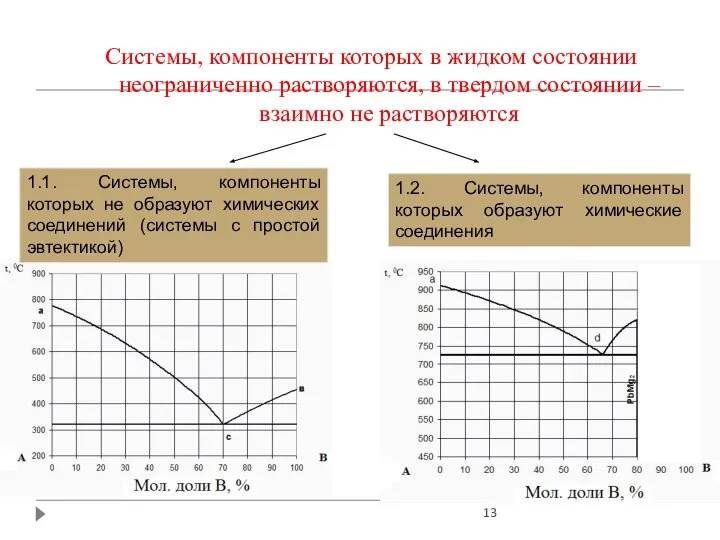
- 13. Системы, компоненты которых в жидком состоянии неограниченно растворяются, в твердом состоянии – взаимно не растворяются 1.1.
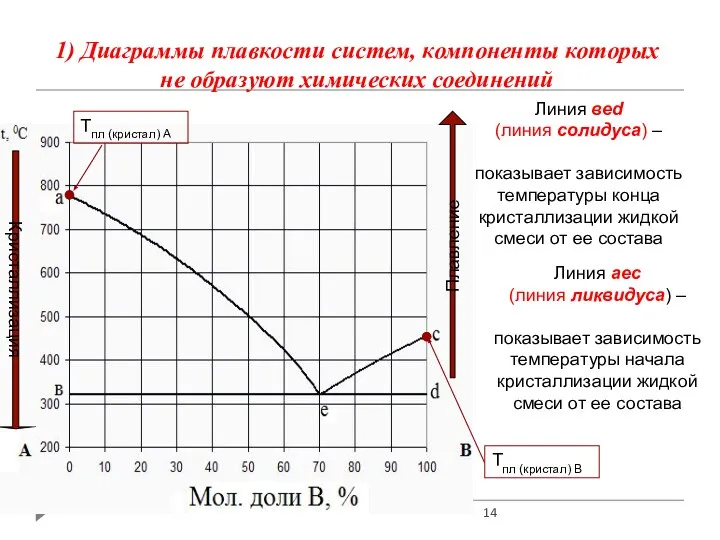
- 14. 1) Диаграммы плавкости систем, компоненты которых не образуют химических соединений Линия аес (линия ликвидуса) – показывает
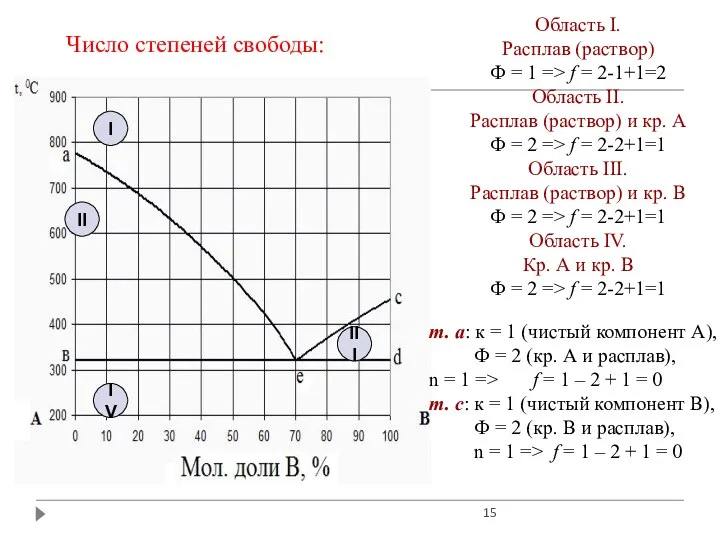
- 15. Область I. Расплав (раствор) Ф = 1 => f = 2-1+1=2 Область II. Расплав (раствор) и
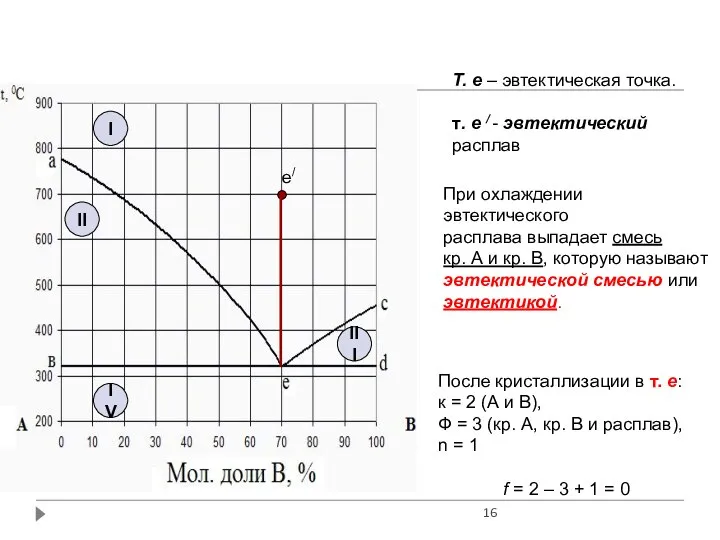
- 16. I II III IV Т. е – эвтектическая точка. т. е / - эвтектический расплав При
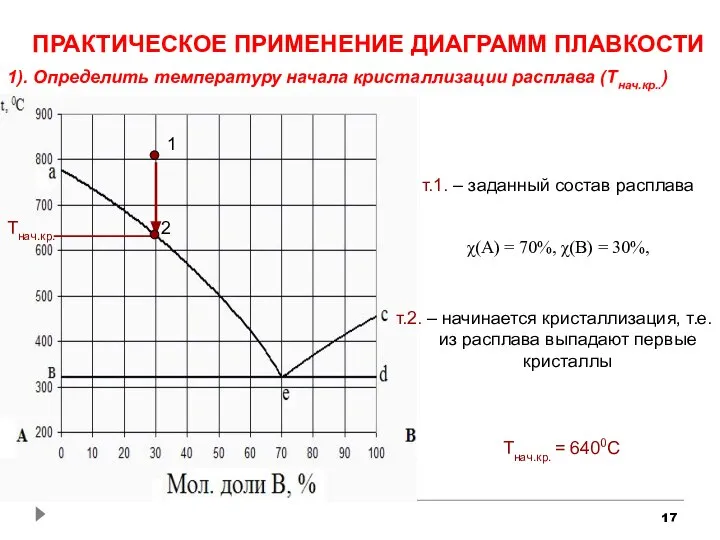
- 17. ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ ДИАГРАММ ПЛАВКОСТИ 1). Определить температуру начала кристаллизации расплава (Тнач.кр..) т.1. – заданный состав расплава
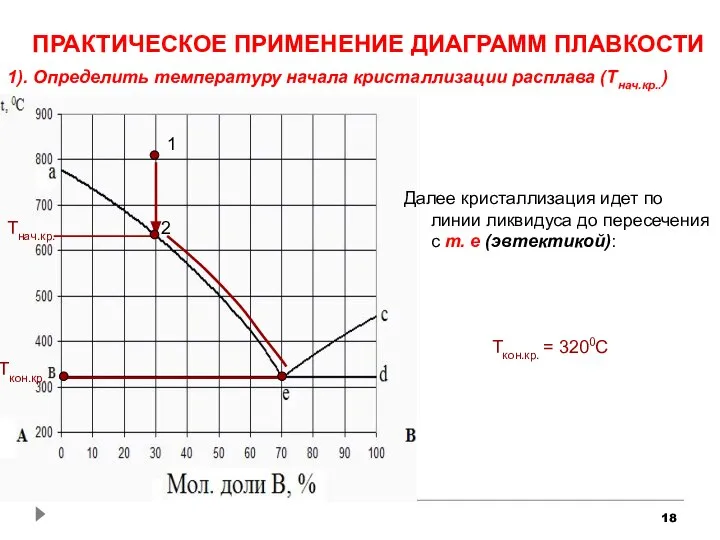
- 18. ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ ДИАГРАММ ПЛАВКОСТИ 1). Определить температуру начала кристаллизации расплава (Тнач.кр..) Далее кристаллизация идет по линии
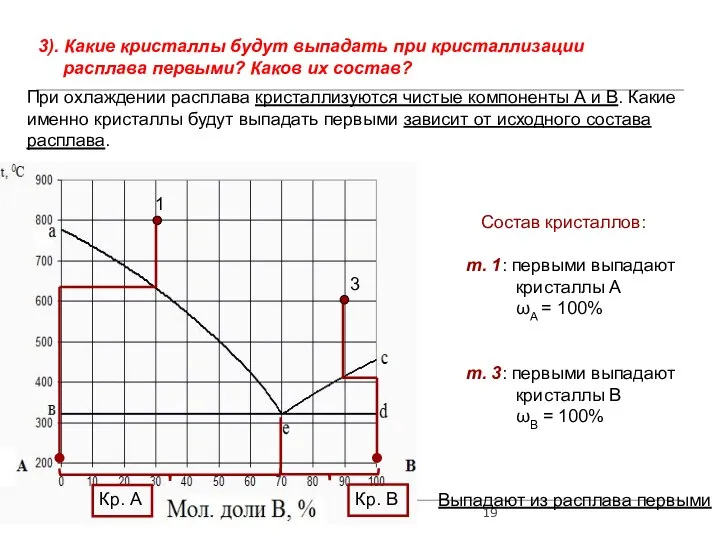
- 19. 3). Какие кристаллы будут выпадать при кристаллизации расплава первыми? Каков их состав? При охлаждении расплава кристаллизуются
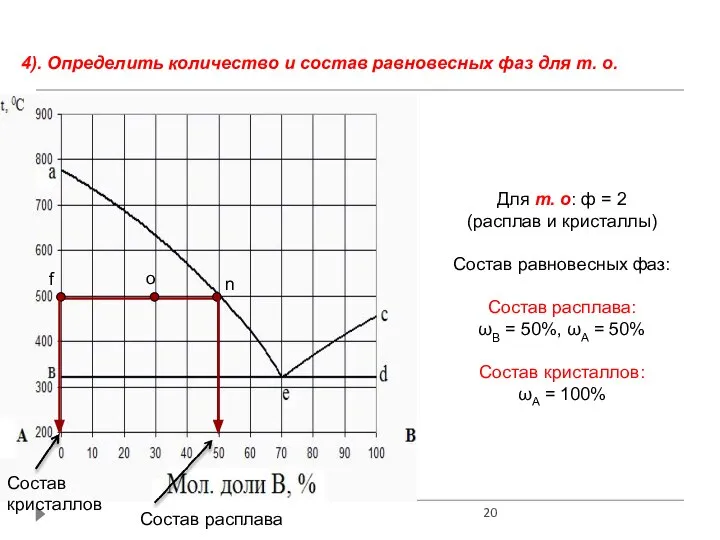
- 20. 4). Определить количество и состав равновесных фаз для т. о. Для т. о: ф = 2
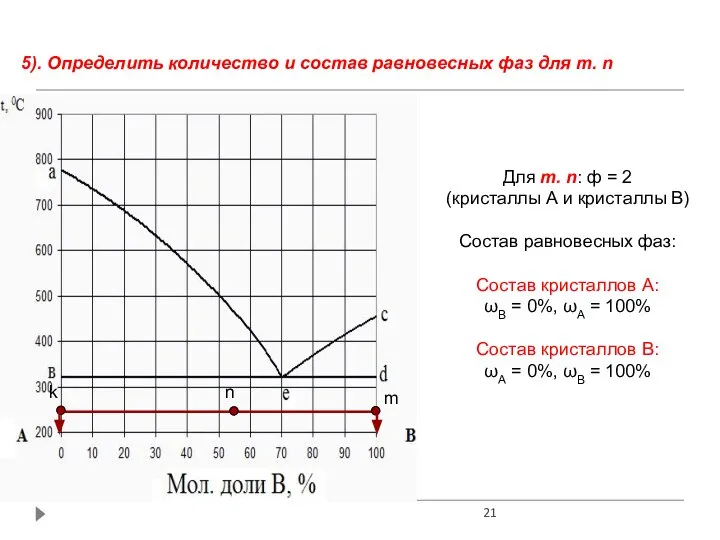
- 21. 5). Определить количество и состав равновесных фаз для т. n Для т. n: ф = 2
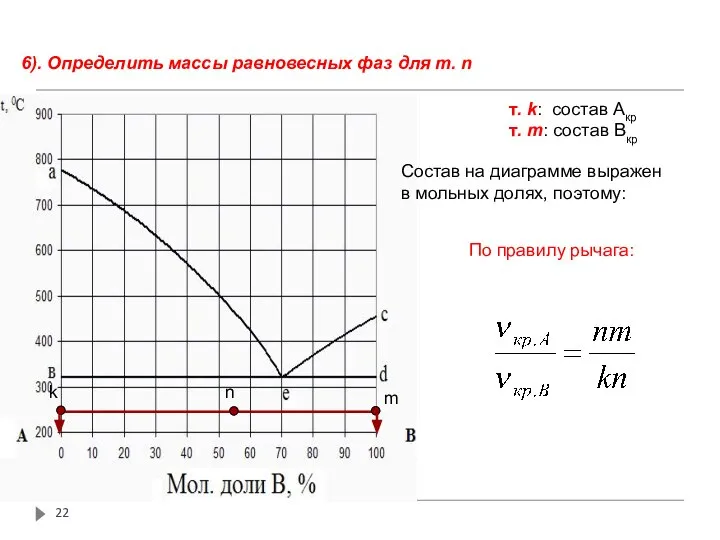
- 22. 6). Определить массы равновесных фаз для т. n т. k: состав Акр т. m: состав Вкр
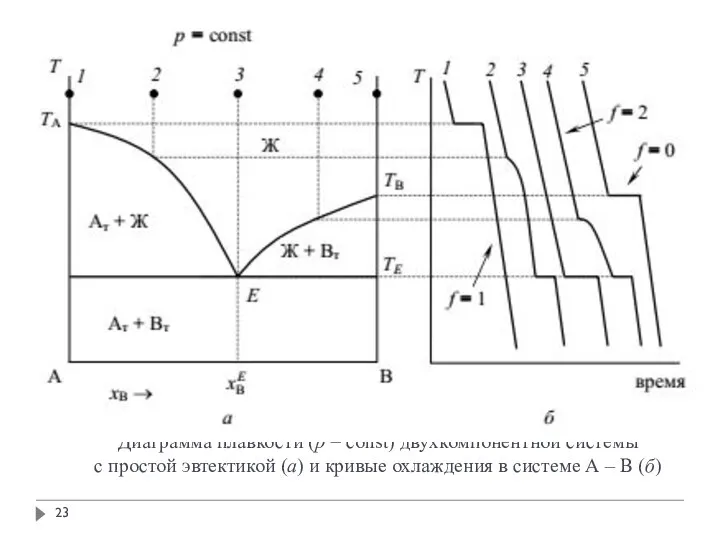
- 23. Диаграмма плавкости (p = const) двухкомпонентной системы с простой эвтектикой (а) и кривые охлаждения в системе
- 24. Анализ диаграммы состояния Особенностью диаграммы плавкости систем эвтектического типа является то, что кривая охлаждения смеси состава
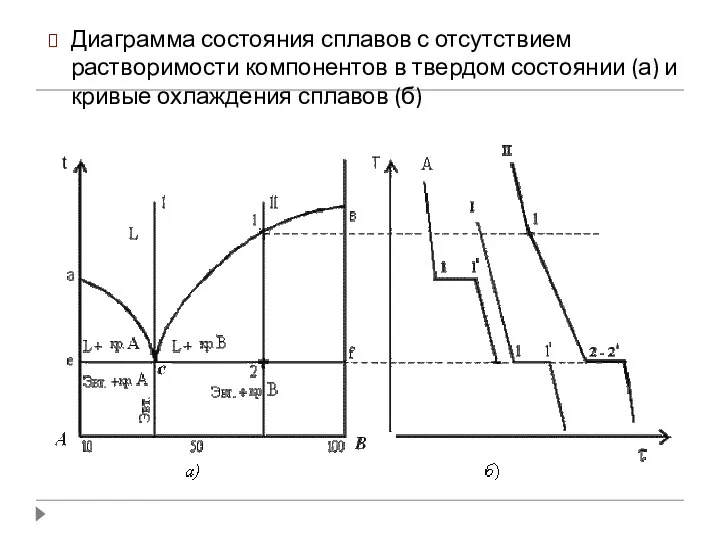
- 25. Диаграмма состояния сплавов с отсутствием растворимости компонентов в твердом состоянии (а) и кривые охлаждения сплавов (б)
- 26. Анализ диаграммы состояния 1. Количество компонентов: К = 2 (компоненты А и В); 2. Число фаз:
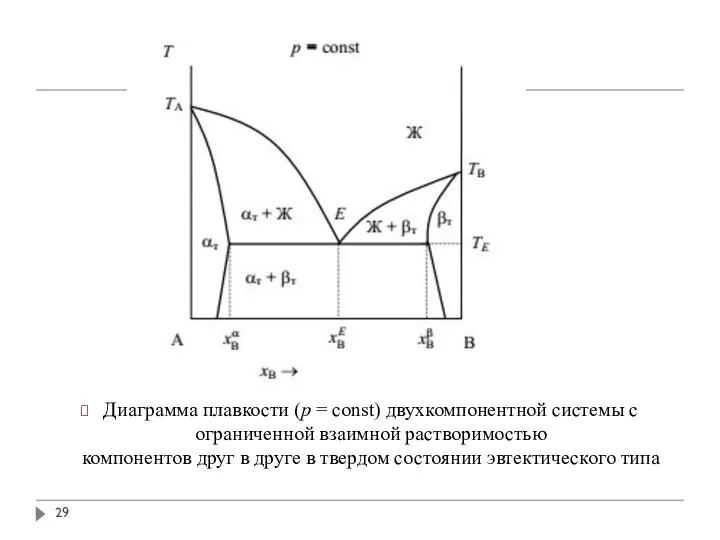
- 27. Диаграмма плавкости (p = const) двухкомпонентной системы с ограниченной взаимной растворимостью компонентов друг в друге в
- 28. В области под горизонтальной частью солидуса в равновесии находятся две твердые фазы – твердые растворы αт
- 29. Диаграмма плавкости (p = const) двухкомпонентной системы с ограниченной взаимной растворимостью компонентов друг в друге в
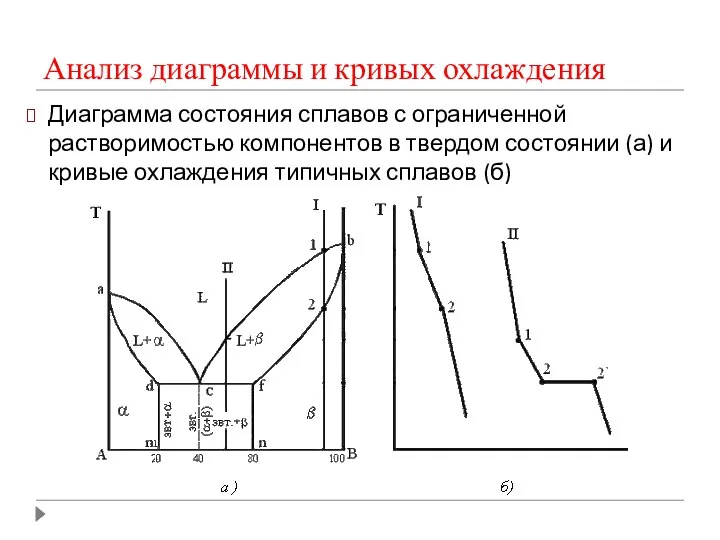
- 30. Анализ диаграммы и кривых охлаждения Диаграмма состояния сплавов с ограниченной растворимостью компонентов в твердом состоянии (а)
- 31. Анализ диаграммы состояния: Диаграмма состояния и кривые охлаждения типичных сплавов системы представлены на рис. 1. Количество
- 32. Диаграмма плавкости двухкомпонентной системы перитектического типа Другим видом трехфазного равновесия, наблюдаемого в двухкомпонентных системах, компоненты которых
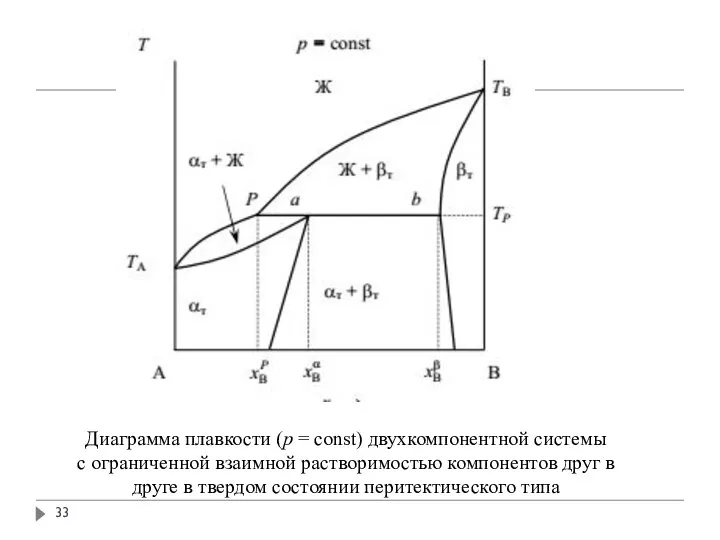
- 33. Диаграмма плавкости (p = const) двухкомпонентной системы с ограниченной взаимной растворимостью компонентов друг в друге в
- 34. В данном случае, как и при эвтектическом равновесии, в системе в равновесии находятся две твердые фазы
- 35. При температуре перитектики ТР в системе протекает так называемая перитектическая реакция: которая идет слева направо при
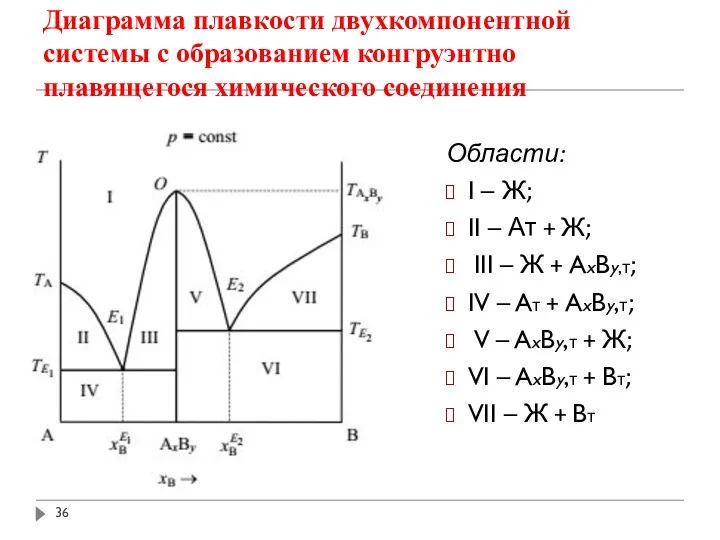
- 36. Диаграмма плавкости двухкомпонентной системы с образованием конгруэнтно плавящегося химического соединения Области: I – Ж; II –
- 37. Диаграмма плавкости системы, состоящей из двух компонентов А и В, образующих химическое содинение AxBy, не способное
- 38. В системе наблюдается два эвтектических равновесия при ТE1 и ТE2 с эвтектическими расплавами состава соответственно. Как
- 39. Само химическое соединение AxBy обозначается на диаграмме вертикальной линией. В системе может образовываться не одно, а
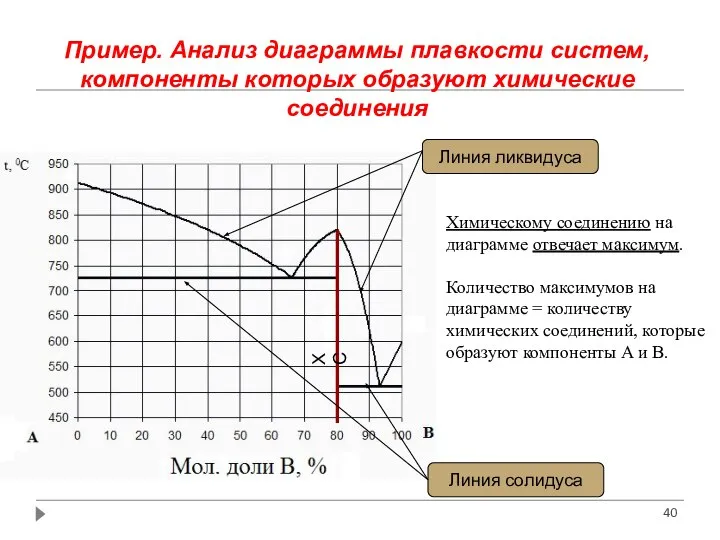
- 40. Пример. Анализ диаграммы плавкости систем, компоненты которых образуют химические соединения Химическому соединению на диаграмме отвечает максимум.
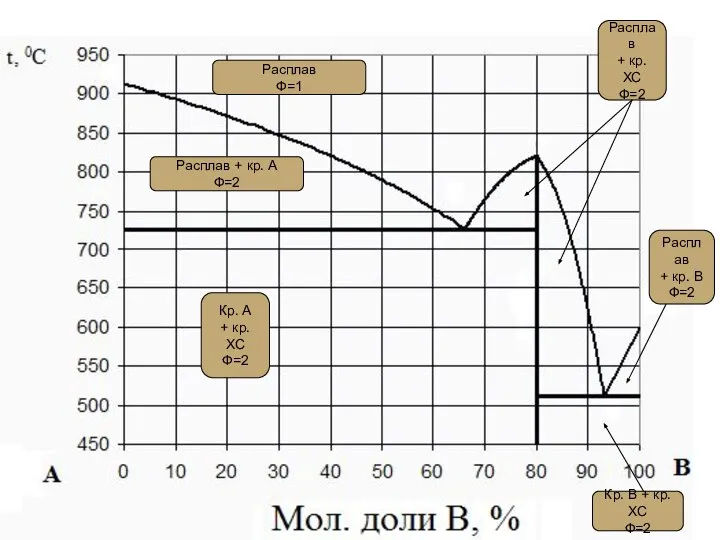
- 41. Расплав Ф=1 Расплав + кр. А Ф=2 Кр. А + кр. ХС Ф=2
- 42. ХС ХС
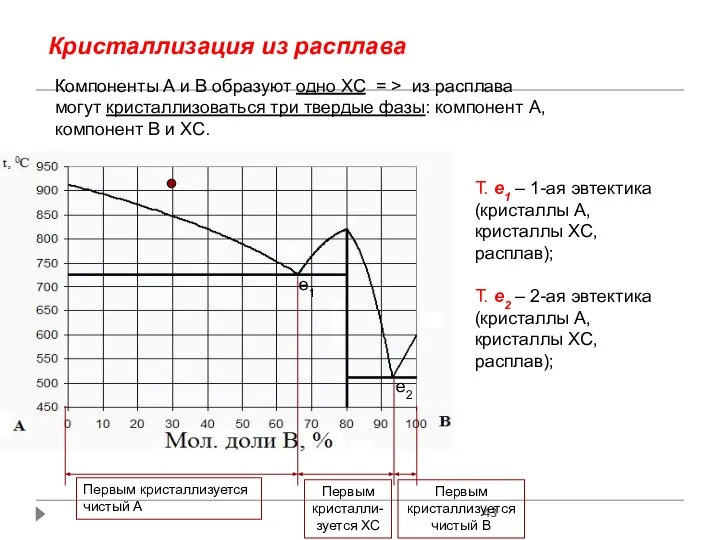
- 43. Кристаллизация из расплава Компоненты А и В образуют одно ХС = > из расплава могут кристаллизоваться
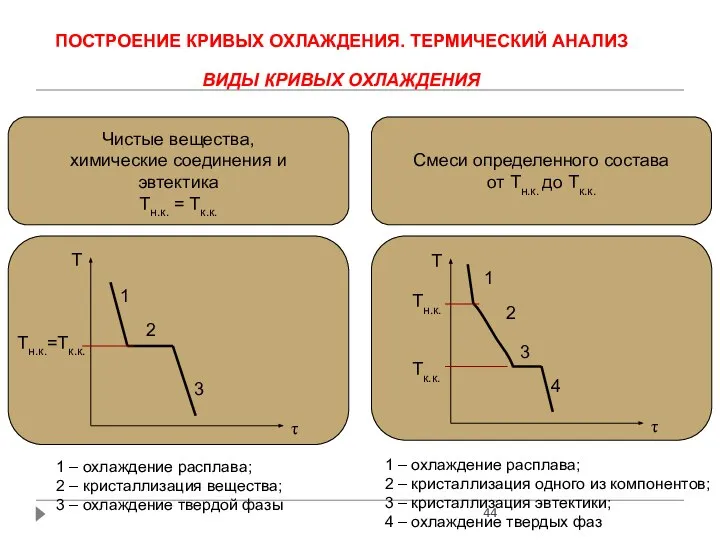
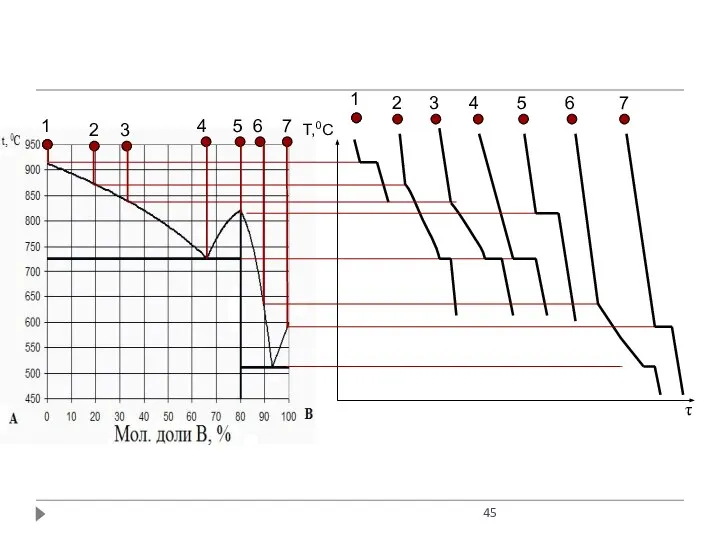
- 44. ПОСТРОЕНИЕ КРИВЫХ ОХЛАЖДЕНИЯ. ТЕРМИЧЕСКИЙ АНАЛИЗ ВИДЫ КРИВЫХ ОХЛАЖДЕНИЯ Чистые вещества, химические соединения и эвтектика Тн.к. =
- 45. Т,0С τ
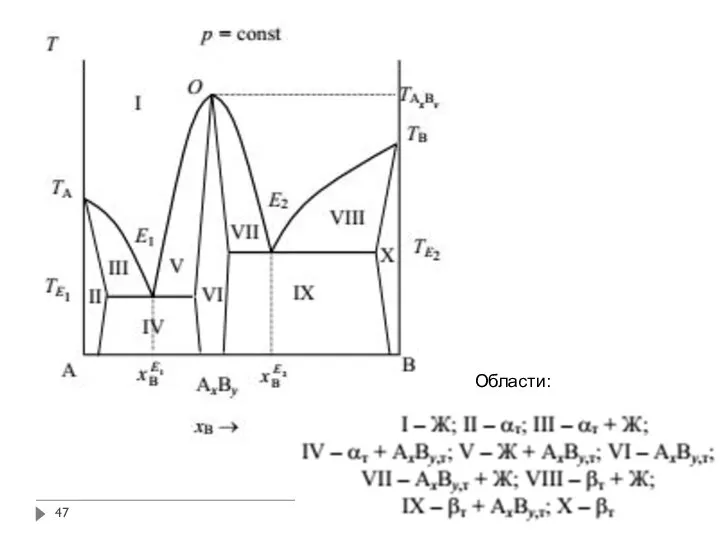
- 46. Диаграмма плавкости (p = const) двухкомпонентной системы с образованием в ней химического соединения, плавящегося конгруэнтно (без
- 47. Области:
- 48. В этом случае на диаграмме состояние соединение AxBy, обладающее ненулевой областью гомогенности изображается в виде поля
- 50. Диаграмма плавкости двухкомпонентной системы с образованием инконгруэнтно плавящегося химического соединения Неустойчивые химические соединения плавятся инконгруэнтно, т.
- 51. Связь между свойствами сплавов и типом диаграммы состояния При образовании механических смесей свойства изменяются по линейному
- 52. При образовании твердых растворов с ограниченной растворимостью свойства в интервале концентраций, отвечающих однофазным твердым растворам, изменяются
- 53. Термины и определения при анализе двухкомпонентных диаграмм Компонент — составная часть, в данном случае химический элемент,
- 54. Раствор твердый — однофазный в твердом состоянии сплав, в котором соотношение компонент может быть переменным и
- 56. Скачать презентацию



























 Химическая связь 8 класс - Презентация_
Химическая связь 8 класс - Презентация_ Углеводороды в природе
Углеводороды в природе Способы получения металлов
Способы получения металлов Производство нитрата аммония (лекция 16)
Производство нитрата аммония (лекция 16) Железо от начала времен до конца средних веков
Железо от начала времен до конца средних веков Введение в материаловедение
Введение в материаловедение Презентация на тему Арены (10 класс)
Презентация на тему Арены (10 класс)  Презентация на тему Уголь
Презентация на тему Уголь  Презентация на тему Вещества в твоей жизни
Презентация на тему Вещества в твоей жизни  Закономерности изменения окислительно-востановительных свойств соединений в периодах и группах
Закономерности изменения окислительно-востановительных свойств соединений в периодах и группах Алканы
Алканы Физические свойства водорода
Физические свойства водорода Изотерма адсорбции. Связь изотермы, изопикны и изостеры адсорбции. Закон Генри. Лекция 6
Изотерма адсорбции. Связь изотермы, изопикны и изостеры адсорбции. Закон Генри. Лекция 6 Лаборатория мечты
Лаборатория мечты Основания. Классификация
Основания. Классификация Презентация на тему Халькогены
Презентация на тему Халькогены  4 Минеральные удобрения (1)
4 Минеральные удобрения (1) Презентация на тему Химия и повседневная жизнь человека
Презентация на тему Химия и повседневная жизнь человека  Мышьяк
Мышьяк Problem-solving. Test: real-time polymerase chain reaction
Problem-solving. Test: real-time polymerase chain reaction Лекарственные растения содержащие флавоноиды
Лекарственные растения содержащие флавоноиды Валентность. Определение валентности элемента в оксиде
Валентность. Определение валентности элемента в оксиде Минералы
Минералы Заманауи косметика биотехнологиясы
Заманауи косметика биотехнологиясы Сера и ее соединения
Сера и ее соединения Трансляция. Активирование аминокислоты
Трансляция. Активирование аминокислоты Углеводороды
Углеводороды Знаки химических элементов. Периодическая система
Знаки химических элементов. Периодическая система