Слайд 2 Галагеноалканы – это предельные алимфатические соединения, в молекулах которых присутствует атом

галогена.
Слайд 4Галогенопроизводные алканов
H3C-CH2 бромэтан
Br
Cl
CH 2- хлорпропан
H3C CH3
CH3
H3C-C-CH3
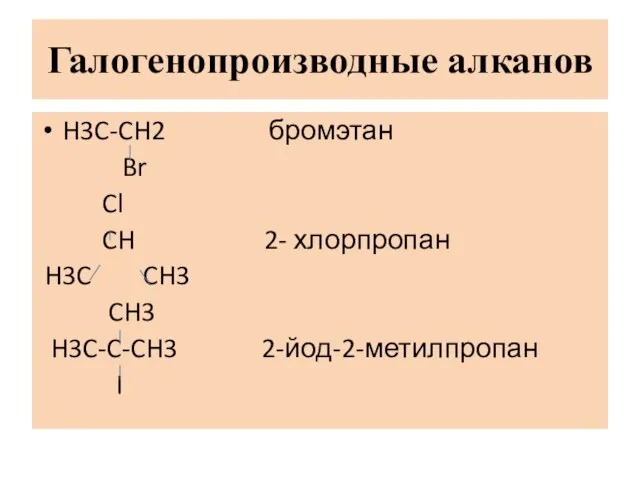
2-йод-2-метилпропан
I
Слайд 5Характеристика связей C–Halв молекулах галогеналканов
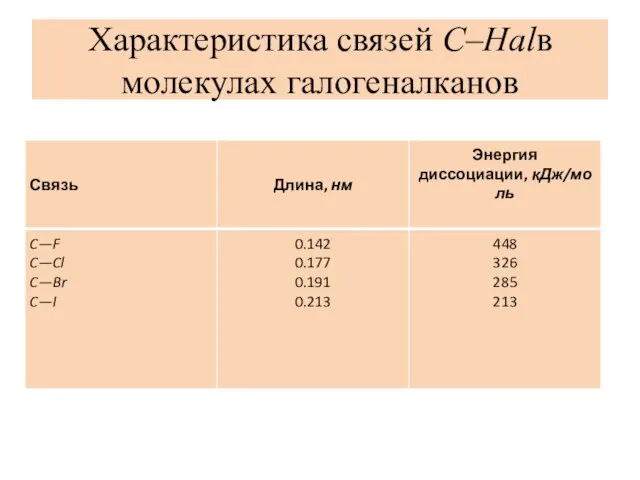
Слайд 6 В зависимости от числа атомов галогена и от их природы галогеналканы

можно разделить на:
моногалогеналканы, содержащие один атом галогена, и
ди-, три- и полигалогеналканы, в молекулах которых несколько атомов галогена.
Моногалогеналканы классифицируют на первичные, вторичные и третичные в зависимости от природы атома углерода, у которого находится галоген.
Среди дигалогеналканов выделяют геминальные, в которых атомы галогена находятся у одного атома углерода, ивицинальныес расположением атомов галогена у соседних углеродных атомов
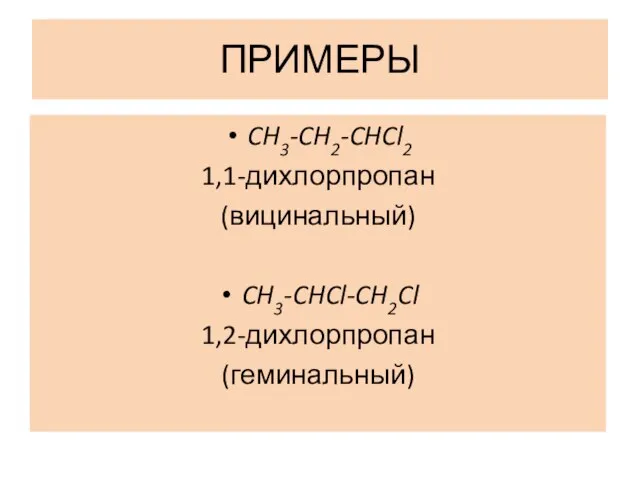
Слайд 7ПРИМЕРЫ
CH3-CH2-CHCl2
1,1-дихлорпропан
(вицинальный)
CH3-CHCl-CH2Cl
1,2-дихлорпропан
(геминальный)
Слайд 8Физические свойства
1. Летучесть. Молекулы фтор-, хлоралканов полярны, т.к. электроотрицательность галогенов и

углерода:
Связи С—F и С—Сl сильно полярны, что приводит к притяжению между диполями соседних молекул:
2. Температуры кипения фтор- и хлоралканов близки к температурам кипения углеводородов с такой же молекулярной массой. Молекулы бром- и иодалканов малополярны. Атом брома имеет такую же массу, как шесть групп —СН2—, но размеры молекулы бромалкана гораздо меньше, чем молекулы алкана равной массы. Меньший размер молекул приводит к уменьшению взаимодействия между ними и к более низкой температуре кипения.
Температура кипения бром- и иодалканов значительно ниже температуры кипения алканов с той же молекулярной массой
3. Растворимость. Галогенопроизводные плохо растворимы в воде.
4. Запах. Галогеналканы имеют сладковатый запах (немного тошнотворный).
5. Плотность. Хлоралканы легче воды, а бром- и иодалканы — тяжелее.
Слайд 9Химические свойства галогеналканов
Реакция замещения:
C2H3Cl + 2NH3 → C2H3NH2 + NH4HCl
хлорэтан
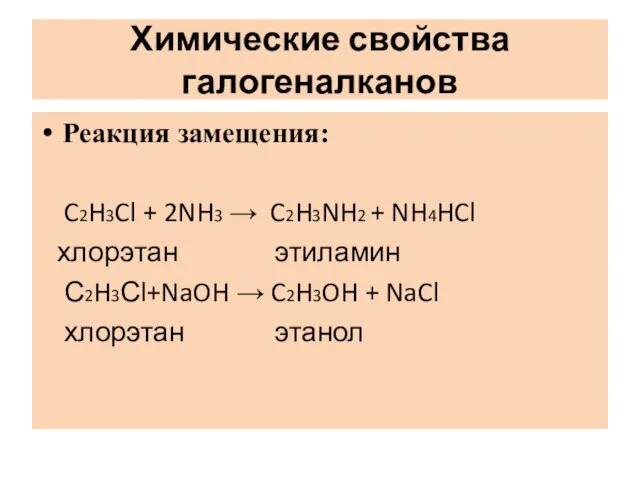
этиламин
С2H3Сl+NaOH → C2H3OH + NaCl
хлорэтан этанол
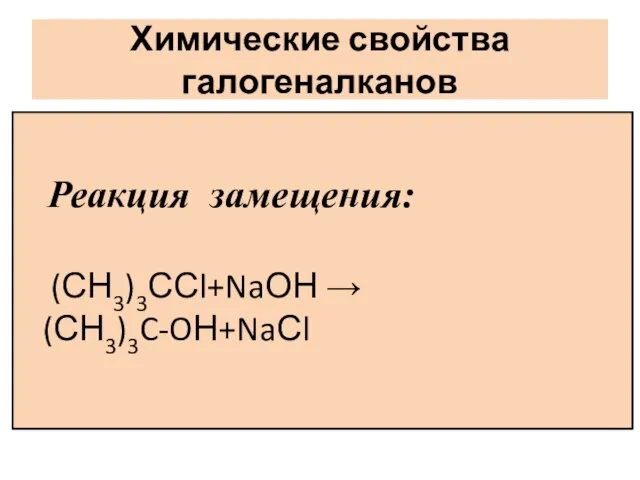
Слайд 10Химические свойства галогеналканов
Реакция замещения:
(СН3)3ССl+NaОН →(СН3)3C-OН+NaСl
Слайд 11Химические свойства галогеналканов
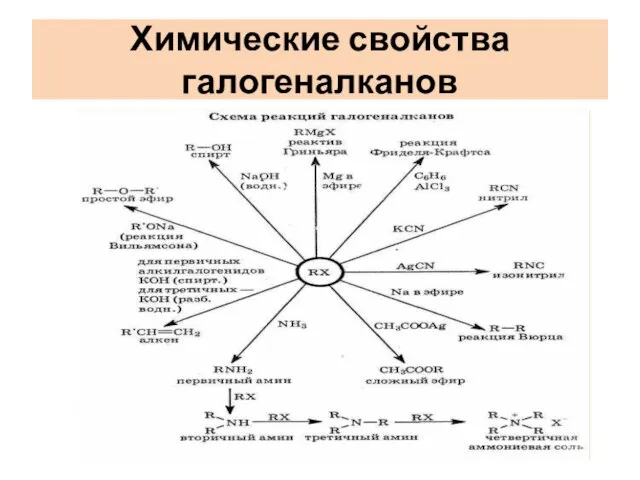
Слайд 12Получение моногалогеналканов
Присоединение галогеноводородов к алкенам.
R-CH=CH2+HCl→R-CHCl-CH3
Реакции спиртов с галогеноводородами.
R-OH+H-Cl→R-Cl+H2O
Взаимодействие галогенидов фосфора или тионилхлорида со

спиртами.
3R-OH+PCl3→3R-Cl+H3PO3
Слайд 13Получение дигалогеналканов
Присоединение галогеноводородов к алкинам.
R-C≡CH+2HCl→R-CCl2-CH3
Взаимодействие альдегидов и кетонов с PCl5, PBr5 или SF4. Реакция идёт при нагревании.
R—CHO +

PCl5 → R—CHCl2 + POCl3
Присоединение галогенов к алкенам
R-CH=CH2 + Cl2 → R-CHCl-CHCl
Раскрытие циклических простых эфиров (например, ТГФ) при реакции с NaI в среде H3PO4+P2O5.
C4H8O + HI → I-CH2CH2CH2CH2-I
При 180 °C ТГФ с хлороводородом даёт 1,4-дихлорбутан
Слайд 14Применение галогеналканов
Галогеналканы используются:
как растворители для жиров и масел;
2) в качестве хладагентов (например,

дихлорметан CCl2H2);
3) при тушении пожаров (например, CBr2ClF — дибромфторхлорметан).













 Химические формулы
Химические формулы 9-8 кислоты в свете ТЭД (1)
9-8 кислоты в свете ТЭД (1) Спирты
Спирты Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот
Адсорбционно-десорбционные взаимодействия фосфатов кальция и аминокислот Соли как производные кислот и оснований
Соли как производные кислот и оснований Интерактивная интеллектуальная игра Юный химик
Интерактивная интеллектуальная игра Юный химик Класс оксиды
Класс оксиды Обобщение знаний об углеводородах
Обобщение знаний об углеводородах ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов
ЕГЭ по химии: документы, регламентирующие структуру и содержание контрольных измерительных материалов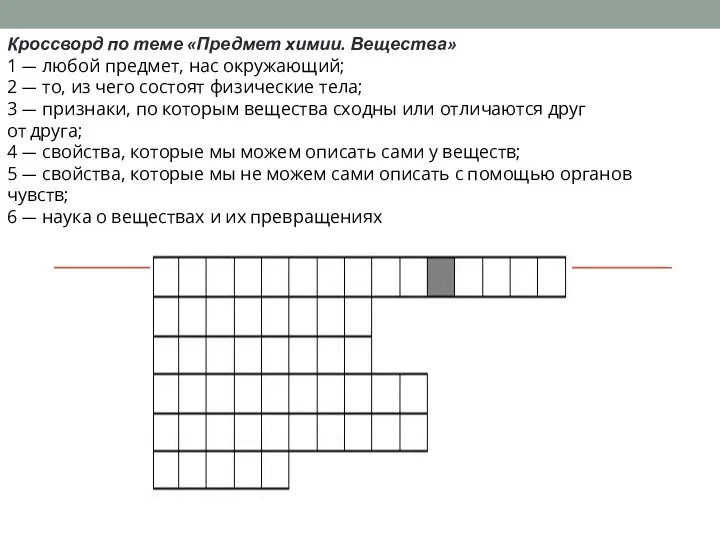 Предмет химии. Вещества
Предмет химии. Вещества 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Общая характеристика оксидов
Общая характеристика оксидов Золото
Золото Органическая химия. Ароматические углеводороды
Органическая химия. Ароматические углеводороды Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Нефть и её переработка
Нефть и её переработка Оксид кремния
Оксид кремния Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Презентация на тему Соединения серы
Презентация на тему Соединения серы  Свойства солей, оксидов, оснований
Свойства солей, оксидов, оснований Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Техника титрования и лабораторная посуда
Техника титрования и лабораторная посуда Уровень С1 в ГИА
Уровень С1 в ГИА Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Азотсодержащие гетероциклические соединения пиррол
Азотсодержащие гетероциклические соединения пиррол Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19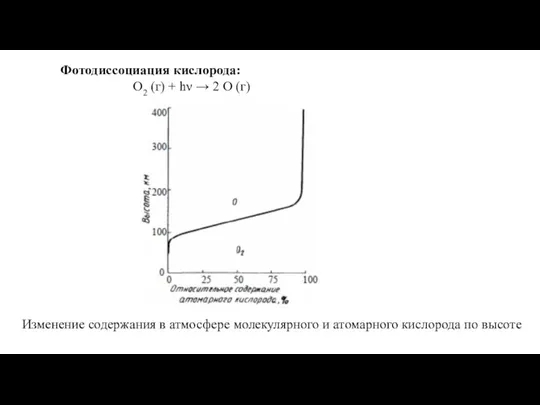 Фотодиссоциация кислорода
Фотодиссоциация кислорода