Содержание
- 2. Составьте уравнения полуреакций окисления и восстановления, определите окислитель и восстановитель в реакции: 1 вариант – взаимодействия
- 3. Методом электронного баланса расставьте коэффициенты в схеме реакции: 1 вариант – BaSO4 + C → BaS
- 4. ЧТО ОБЪЕДИНЯЕТ ? Нанесение металлических покрытий на различные поверхности
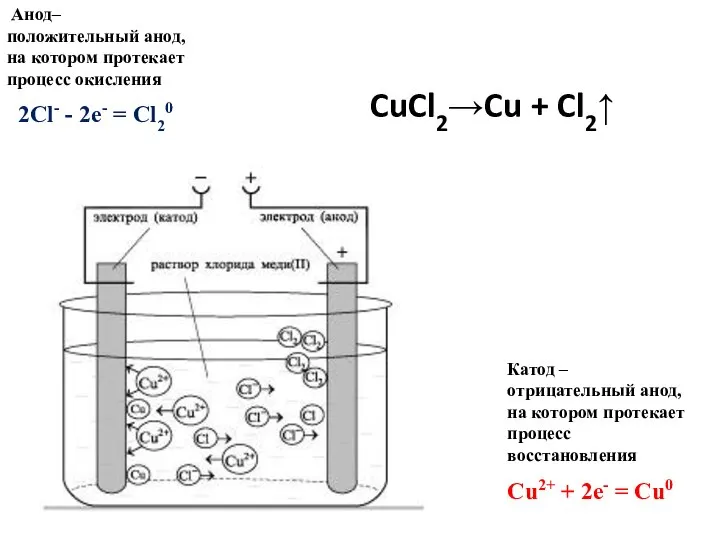
- 5. Как это происходит? Какой химический процесс лежит в основе? ЭЛЕКТРОЛИЗ
- 6. Катод – отрицательный анод, на котором протекает процесс восстановления Анод– положительный анод, на котором протекает процесс
- 11. Скачать презентацию






 Аномальные свойства воды
Аномальные свойства воды 5 Нефть. Нефтепереработка. Конверсия метана
5 Нефть. Нефтепереработка. Конверсия метана Полимеры
Полимеры Скорость химической реакции
Скорость химической реакции Анализ образца доломита методами аналитической химии
Анализ образца доломита методами аналитической химии Презентация на тему Войди в природу другом
Презентация на тему Войди в природу другом  Металлургия в химии
Металлургия в химии Ртуть. Правила работы со ртутью
Ртуть. Правила работы со ртутью Важнейшие породообразующие минералы
Важнейшие породообразующие минералы Простые вещества – неметаллы. Получение и химические свойства неметаллов
Простые вещества – неметаллы. Получение и химические свойства неметаллов Особо чистые вещества. Занятие13
Особо чистые вещества. Занятие13 Свойства воды. Физические свойства
Свойства воды. Физические свойства Химический элемент калий
Химический элемент калий Строение вещества
Строение вещества Влияние кислотности среды на свойство белка
Влияние кислотности среды на свойство белка Prezentatsia1_1
Prezentatsia1_1 Оксиды и гидроксиды металлов
Оксиды и гидроксиды металлов Окислительно-восстановительные реакции. 8 класс
Окислительно-восстановительные реакции. 8 класс Синтетические органические соединения
Синтетические органические соединения Строение атома. Строение электронных оболочек атомов
Строение атома. Строение электронных оболочек атомов Металлическая связь_1
Металлическая связь_1 Аппаратура ионообменных процессов
Аппаратура ионообменных процессов Соли (8 класс)
Соли (8 класс) 3bc28ca0711047a6880d20a6763f17db
3bc28ca0711047a6880d20a6763f17db Арены. Ароматические углеводороды
Арены. Ароматические углеводороды Аминокислоты. Свойства. Промышленные способы получения
Аминокислоты. Свойства. Промышленные способы получения Подготовка к контрольной работе по теме «Изменения, происходящие с веществами
Подготовка к контрольной работе по теме «Изменения, происходящие с веществами Итоговая консультация. Формульный диктант
Итоговая консультация. Формульный диктант