Содержание
- 2. Оксид фосфора (V). Фосфорная кислота и ее соли
- 3. Белый, рыхлый гигроскопичный порошок. Оксид фосфора(V) P2O5 образуется при горении фосфора на воздухе: 4Р + 5О2
- 4. Химические свойства оксида фосфора (V): P2O5 – типичный кислотный оксид. 1) При взаимодействии с водой образует
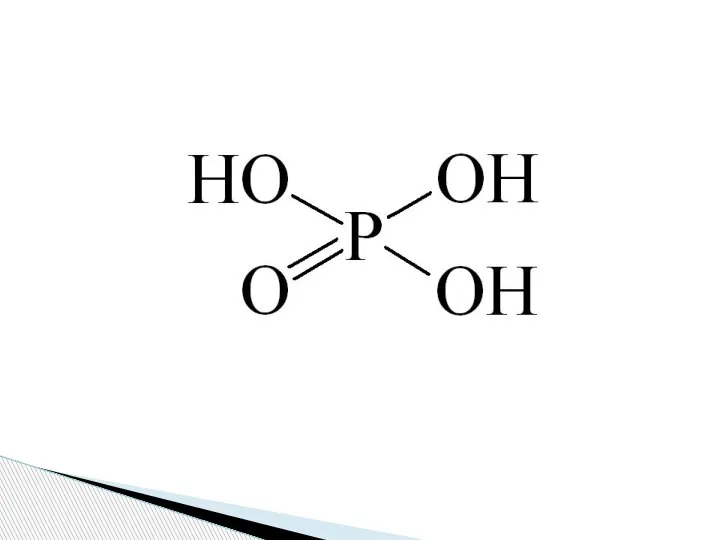
- 5. H3PO4 - бесцветное твердое кристаллическое вещество. Температура плавления +42ºС, хорошо растворяется в воде. Фосфорная кислота -
- 7. Химические свойства H3PO4 Фосфорная кислота вступает во многие реакции, характерные для кислот: 1). С металлами, стоящими
- 8. Фосфорную кислоту используют: в производстве фосфорных удобрений; в производстве кормовых добавок для животноводства; в производстве моющих
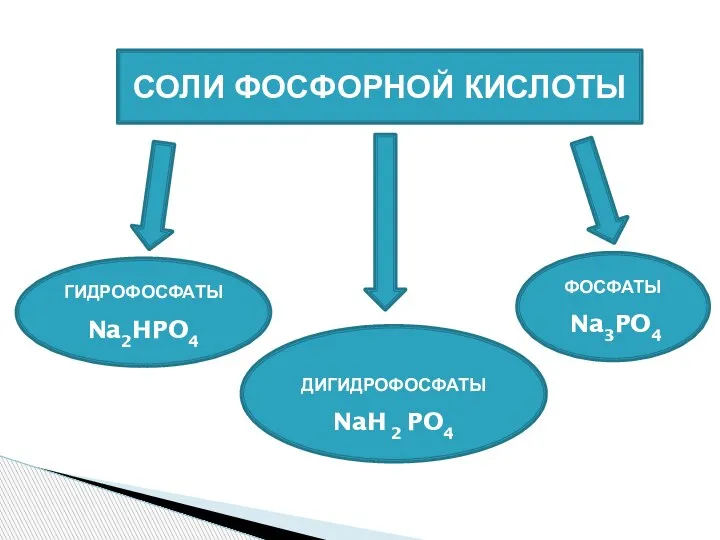
- 9. СОЛИ ФОСФОРНОЙ КИСЛОТЫ ГИДРОФОСФАТЫ Na2HPO4 ДИГИДРОФОСФАТЫ NaH 2 PO4 ФОСФАТЫ Na3PO4
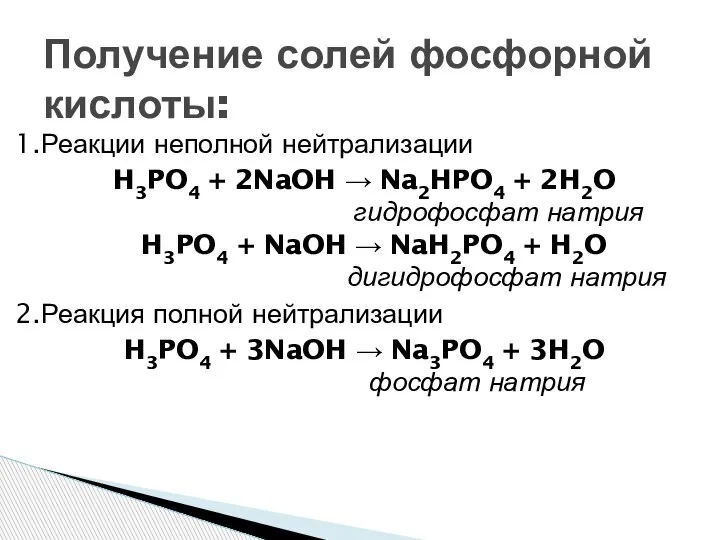
- 10. Получение солей фосфорной кислоты: 1.Реакции неполной нейтрализации H3PO4 + 2NaOH → Na2HPO4 + 2H2O гидрофосфат натрия
- 11. Соли фосфорной кислоты – кристаллические вещества. Средние соли, или фосфаты (например, Са3(РО4)2), нерастворимы в воде, кроме
- 12. Фосфат кальция Фосфат калия Фосфат аммония Фосфат серебра
- 14. Скачать презентацию








 Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием
Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием Основные понятия химической термодинамики
Основные понятия химической термодинамики Биологическая роль III(A) группы
Биологическая роль III(A) группы Органические вещества
Органические вещества Презентация на тему Кристаллические решетки
Презентация на тему Кристаллические решетки  Адсорбция твёрдыми адсорбентами
Адсорбция твёрдыми адсорбентами Фторсодержащие полимеры
Фторсодержащие полимеры Презентация на тему Волокна
Презентация на тему Волокна  Презентация на тему Путешествие по континенту Химия
Презентация на тему Путешествие по континенту Химия  Соли в природе и их значение
Соли в природе и их значение Задача №3: Трансмутация. Команда: Карбораны
Задача №3: Трансмутация. Команда: Карбораны Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Металлическая химическая связь
Металлическая химическая связь Карбид кремния
Карбид кремния Кетоновые тела
Кетоновые тела Химия в еде
Химия в еде Степени окисления
Степени окисления Алкины
Алкины Презентация на тему Коррозия
Презентация на тему Коррозия  Ренгеноструктурный и рентгеноспектральный анализы
Ренгеноструктурный и рентгеноспектральный анализы Ароматические углеводороды
Ароматические углеводороды Алканы
Алканы Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов
Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Физическая химия, термодинамика
Физическая химия, термодинамика Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 valentnost
valentnost