Слайд 2
ГІДРОЛІЗ - це реакція обміну між деякими солями і водою приводить

до утворення слабкого електроліту.
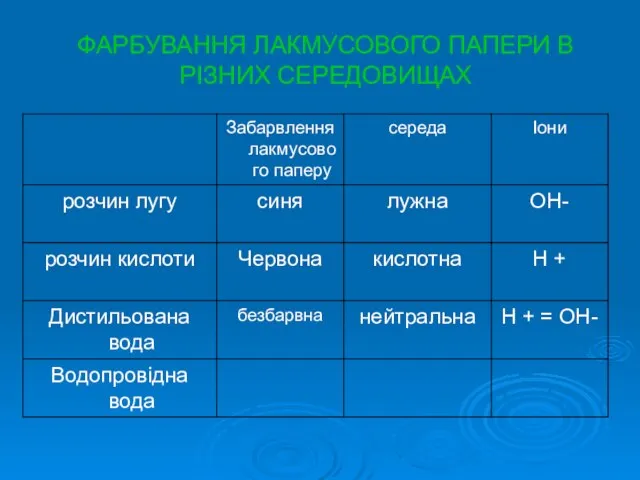
Слайд 4ФАРБУВАННЯ ЛАКМУСОВОГО ПАПЕРИ В РІЗНИХ СЕРЕДОВИЩАХ
Слайд 5Тема: Гідроліз солей
Мета: вивчити сутність гідролізу солей у водних розчинах . завдання:

сформулювати визначення поняття « гідроліз » навчитися пояснювати хімічні процеси, що протікають у водних розчинах солей записувати рівняння реакцій гідролізу пророкувати і пояснювати зміна кислотності середовища і утворення кислих і основних солей у цьому процесі познайомитися з роллю гідролізу солей в природі, господарської діяльності та повсякденному житті людини .
Слайд 6« ГІДРОЛІЗ » - від грецького « гідро » - вода «

лізіс » - розкладання
Слайд 7Забарвлення лакмоіда в розчинах солей :
хлориду алюмінію
AlCl3 карбонату натрію
Na2CO3
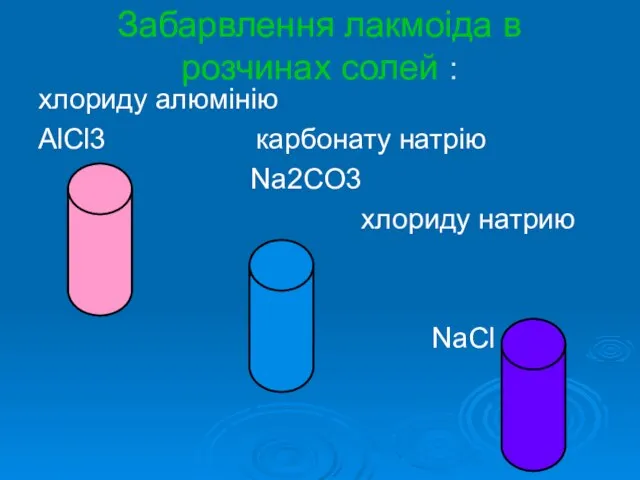
хлориду натрию
NaCl
Слайд 8Механізм гідролізу хлориду алюмінію
H2O H+ + OH-
AlCl3 Al3+ + 3Cl-
Al3+ +3Cl-
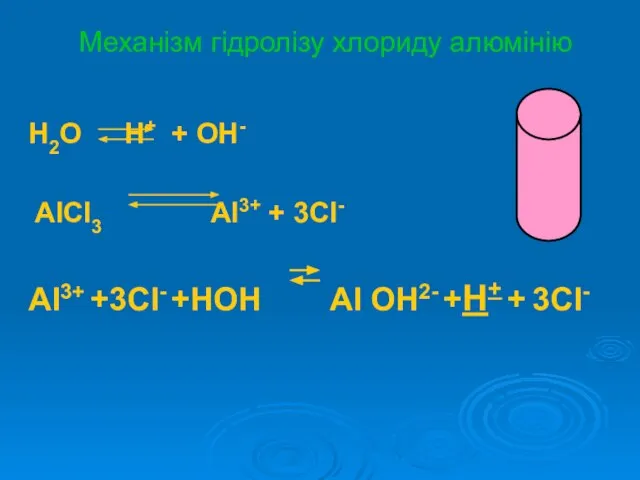
+HOH Al OH2- +H+ + 3Cl-
Слайд 9Схема гідролізу хлориду алюмінію
AlCl3
Al(OH)3 HCl
слабка основа сильна кислота [OH]- <
![Схема гідролізу хлориду алюмінію AlCl3 Al(OH)3 HCl слабка основа сильна кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/901248/slide-8.jpg)
[H]+
(що сильніше того і більше!)
Кисле снрндовище
Слайд 10
АЛГОРИТМ СКЛАДАННЯ РІВНЯНЬ реакції гідролізу СОЛЕЙ
Визначити склад солі, тобто вказати, яким по

силі підставою і який за силою кислотою утворена дана сіль.
Взяти іон слабкого електроліту і написати рівняння взаємодії його з складовими частинами однієї молекули води ; в результаті отримати короткий іонне рівняння гідролізу.
Написати на підставі короткого іонного рівняння молекулярне рівняння.
Вихідні речовини відомі - сіль і вода. Продукти гідролізу скласти , пов'язуючи утворилися іони з тими іонами солі, які не беруть участь у реакції гідролізу.
Слайд 11Механізм гідролізу карбонату натрію
H2O H+ + OH-
Na2CO3 2Na+ + CO32-
2Na+ +CO32- +HOH
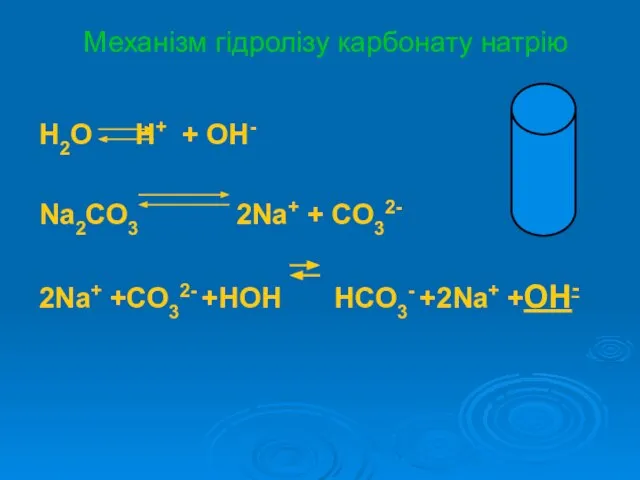
HCO3- +2Na+ +OH-
Слайд 12Механізм гідролізу хлориду натрію
H2O H+ + OH-
NaСl Na+ + Cl-
Na+ +Cl- +HOH
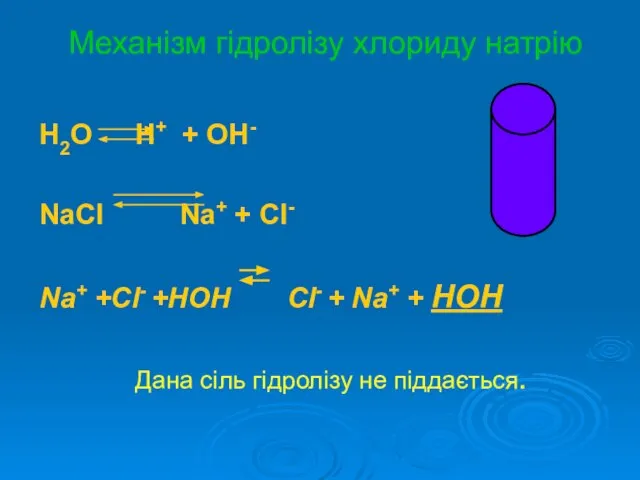
Cl- + Na+ + HOH
Дана сіль гідролізу не піддається.
Слайд 13Роль гідролізу в природі
Перетворення земної кори Забезпечення середовища морської води

Слайд 14Роль гідролізу в народному господарстві
Псування виробничого обладнання Вироблення з нехарчової сировини цінних

продуктів (папір , мило, спирт , глюкоза , білкові дріжджі) Очищення промислових стоків та питної води (сульфат алюмінію + вода гідроксид алюмінію) Підготовка тканин до фарбування Вапнування грунтів засноване на гідролізі






![Схема гідролізу хлориду алюмінію AlCl3 Al(OH)3 HCl слабка основа сильна кислота [OH]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/901248/slide-8.jpg)





 Электроотрицательность
Электроотрицательность Алкены
Алкены Оксиды. Классификация, химические и физические свойства
Оксиды. Классификация, химические и физические свойства Количественный анализ
Количественный анализ Клей
Клей Распределение электронов по энергетическим уровням
Распределение электронов по энергетическим уровням Загадки химии
Загадки химии Коррозия металлов
Коррозия металлов Уравнения химических реакций
Уравнения химических реакций 1 Класифікація_Завада_лекция 1_укр_2018(1)
1 Класифікація_Завада_лекция 1_укр_2018(1) 9 класс Урок №8. Аминокислоты. Белки. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А.
9 класс Урок №8. Аминокислоты. Белки. Составитель презентации – учитель химии МОУ СОШ г. Холма Насонова Т.А. Соли. Состав и классификация
Соли. Состав и классификация Обновление экзаменационных моделей ОГЭ и ЕГЭ по химии
Обновление экзаменационных моделей ОГЭ и ЕГЭ по химии Практикум по химии и технологии нефти и газа
Практикум по химии и технологии нефти и газа მეტალები
მეტალები Основания. Классификация
Основания. Классификация Карбоновые кислоты и их гетерофункциональные производные: гидрокси- и оксокарбоновые кислоты
Карбоновые кислоты и их гетерофункциональные производные: гидрокси- и оксокарбоновые кислоты Массообменные процессы
Массообменные процессы Химия в косметике
Химия в косметике Морфологогия минералов
Морфологогия минералов Металлы (Ме)
Металлы (Ме) Три секрета прочности волокнистых композитов
Три секрета прочности волокнистых композитов Неметаллы. Обобщение и систематизация знаний
Неметаллы. Обобщение и систематизация знаний Хром
Хром Углеводороды. 9 класс
Углеводороды. 9 класс 8-29 класс (1)
8-29 класс (1) Template biosynthesis
Template biosynthesis Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений