Содержание
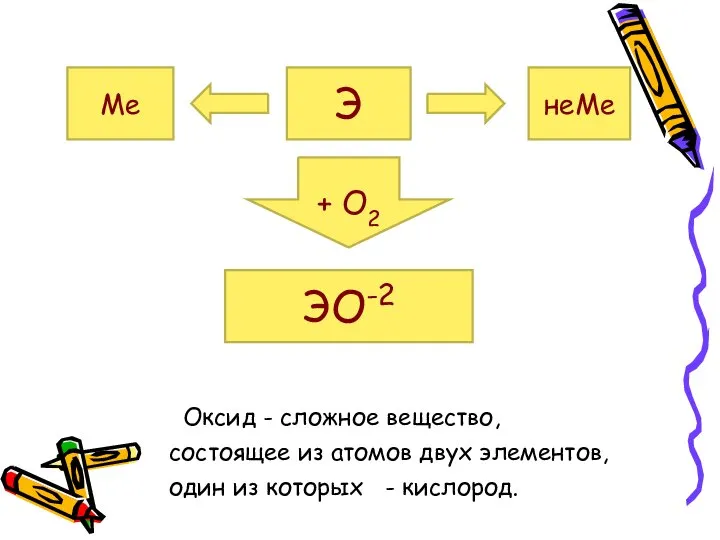
- 3. Оксид - сложное вещество, состоящее из атомов двух элементов, один из которых - кислород. Э Ме
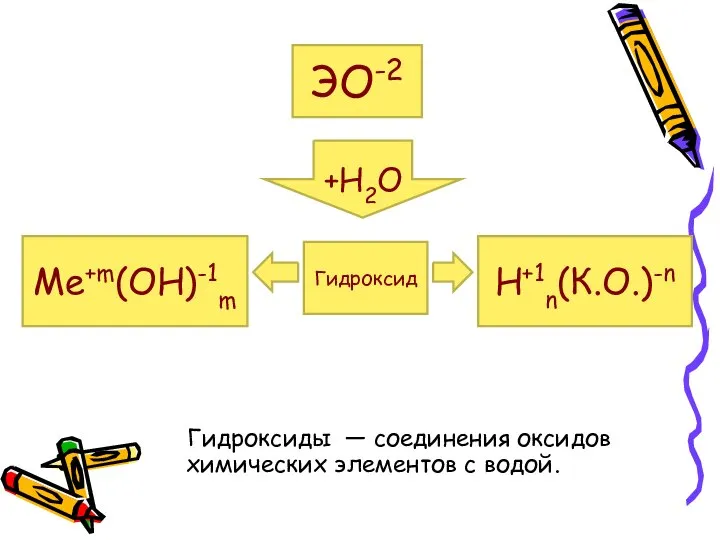
- 4. Гидроксиды — соединения оксидов химических элементов с водой. ЭО-2 +Н2О Гидроксид Ме+m(ОН)-1m Н+1n(К.О.)-n
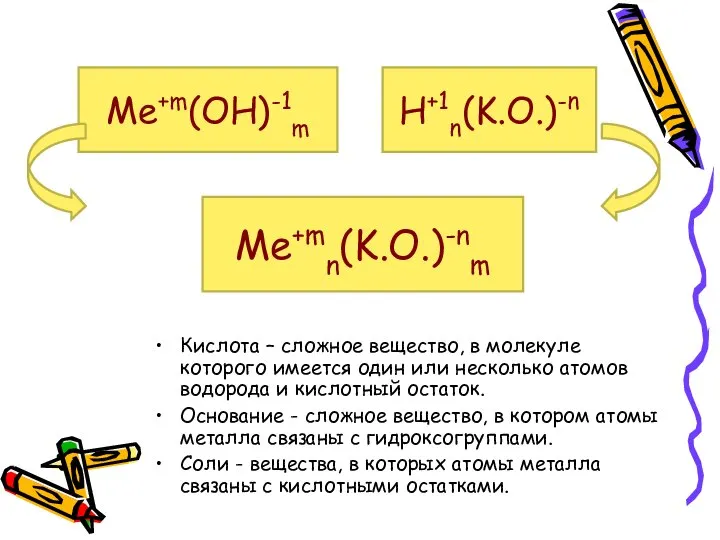
- 5. Кислота – сложное вещество, в молекуле которого имеется один или несколько атомов водорода и кислотный остаток.
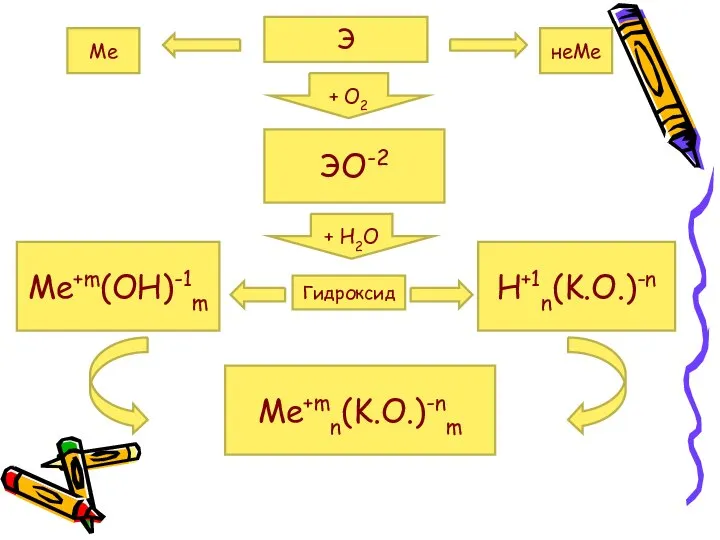
- 6. Э Ме неМе + О2 ЭО-2 Me+m(OH)-1m H+1n(K.O.)-n + Н2О Гидроксид Me+mn(K.O.)-nm
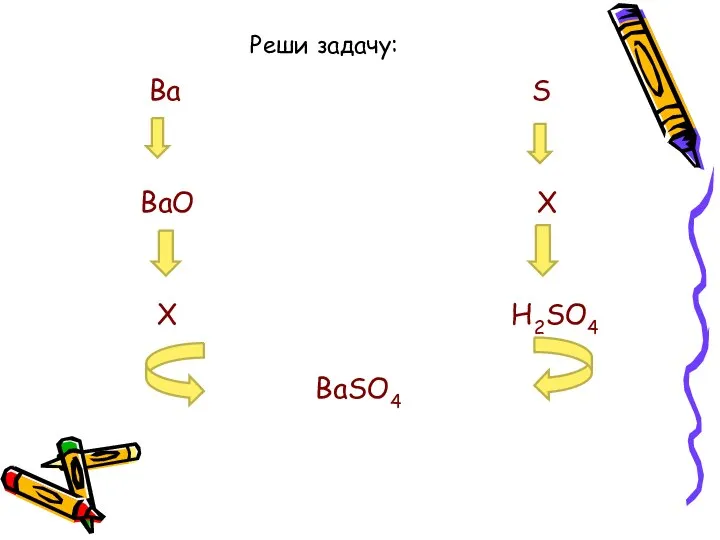
- 7. Реши задачу: Ba S BaO X X H2SO4 BaSO4
- 9. Скачать презентацию

 Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием
Методы восстановления. Формирование СН-связей декарбоксилированием и декарбонилированием Основные понятия химической термодинамики
Основные понятия химической термодинамики Биологическая роль III(A) группы
Биологическая роль III(A) группы Органические вещества
Органические вещества Презентация на тему Кристаллические решетки
Презентация на тему Кристаллические решетки  Адсорбция твёрдыми адсорбентами
Адсорбция твёрдыми адсорбентами Фторсодержащие полимеры
Фторсодержащие полимеры Презентация на тему Волокна
Презентация на тему Волокна  Презентация на тему Путешествие по континенту Химия
Презентация на тему Путешествие по континенту Химия  Соли в природе и их значение
Соли в природе и их значение Задача №3: Трансмутация. Команда: Карбораны
Задача №3: Трансмутация. Команда: Карбораны Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ
Курс химии для основных академических направлений подготовки специалистов НИЯУ МИФИ Металлическая химическая связь
Металлическая химическая связь Карбид кремния
Карбид кремния Кетоновые тела
Кетоновые тела Химия в еде
Химия в еде Степени окисления
Степени окисления Алкины
Алкины Презентация на тему Коррозия
Презентация на тему Коррозия  Ренгеноструктурный и рентгеноспектральный анализы
Ренгеноструктурный и рентгеноспектральный анализы Ароматические углеводороды
Ароматические углеводороды Алканы
Алканы Презентация на тему Органическая химия. История развития
Презентация на тему Органическая химия. История развития  Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов
Моноенаминирование 4-пиронов и 4-метилен-4н-пиранов Особенные свойства муравьиной кислоты
Особенные свойства муравьиной кислоты Физическая химия, термодинамика
Физическая химия, термодинамика Теоретические основы органической химии. Лекция 25
Теоретические основы органической химии. Лекция 25 valentnost
valentnost