Слайд 2 У металлов есть враг, который приводит к огромным безвозвратным потерям металлов,

ежегодно полностью разрушается около 10% производимого железа. По данным Института физической химии РАН, каждая шестая домна в России работает впустую – весь выплавляемый металл превращается в ржавчину. Этот враг - коррозия.
Слайд 3 Коррозия – разрушение металлов и сплавов под воздействием окружающей среды. Слово

коррозия происходит от латинского corrodere, что означает разъедать.
Слайд 4Химическая коррозия
Химическая коррозия – это взаимодействие металлов с сухими газами и

жидкостями – неэлектролитами. Такому виду коррозии подвергаются турбины, арматура печей и детали двигателей внутреннего сгорания.
Слайд 5Электрохимическая коррозия
Электрохимическая коррозия – это все случаи коррозии в присутствии воды

и жидкостей – электролитов.
Слайд 6Сущность коррозии.
Коррозия состоит из двух процессов: химического – это отдача электронов

и электрического – это перенос электронов.
Слайд 7Закономерности коррозии:
1. Если соединены два разных металла, то коррозии подвергается

только более активный, и пока он полностью не разрушится, менее активный защищён.
Слайд 8 2. Скорость коррозии тем больше, чем дальше друг от друга в

ряду напряжений расположены соединённые металлы.
Слайд 9Способы защиты от коррозии.
Одним из наиболее распространенных способов защиты металлов от

коррозии является нанесение на их поверхность защитных пленок: лака, краски, эмали.
Слайд 10 Широко распространенным способом защиты металлов от коррозии является покрытие их слоем

других металлов. Покрывающие металлы сами корродируют с малой скоростью, так как покрываются плотной оксидной пленкой. Производят покрытие цинком, никелем, хромом и др.
Слайд 11 Создание сплавов с антикоррозионными свойствами. Для этого в основной металл добавляют

до 12% хрома, никеля, кобальта или меди.
Слайд 12 Изменение состава среды. Для замедления коррозии вводятся ингибиторы. Это вещества, которые

замедляют скорость реакции.











 Минерал Александрит
Минерал Александрит Soft Matter. Emulsions
Soft Matter. Emulsions Химические свойства металлов. Электрохимический ряд напряжения металлов
Химические свойства металлов. Электрохимический ряд напряжения металлов Фторсодержащие полимеры
Фторсодержащие полимеры Алмаз. Свойства алмазов
Алмаз. Свойства алмазов Относительная атомная масса
Относительная атомная масса Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Химия в косметике
Химия в косметике Простые вещества – неметаллы. Получение и химические свойства неметаллов
Простые вещества – неметаллы. Получение и химические свойства неметаллов Диффузия золота и свинца
Диффузия золота и свинца Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Основные классы неорганических соединений (урок - семинар)
Основные классы неорганических соединений (урок - семинар) Основы квантовой химии
Основы квантовой химии Презентация на тему Азотная кислота и ее соли (9 класс)
Презентация на тему Азотная кислота и ее соли (9 класс)  Подготовка к олимпиаде по химии. Некоторые идеи составления и решения нестандартны задач
Подготовка к олимпиаде по химии. Некоторые идеи составления и решения нестандартны задач Скорость протекания химических реакций
Скорость протекания химических реакций Белки-1 2020
Белки-1 2020 Рука руку моет. Механизм двух реакций
Рука руку моет. Механизм двух реакций Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Энергетические уровни
Энергетические уровни Карбоновые кислоты
Карбоновые кислоты Химияның негізгі түсініктері мен зандары
Химияның негізгі түсініктері мен зандары Химия в быту
Химия в быту Основания. Щелочи – растворимые основания
Основания. Щелочи – растворимые основания Химические методы. Золь-гель метод
Химические методы. Золь-гель метод Многоатомные спирты
Многоатомные спирты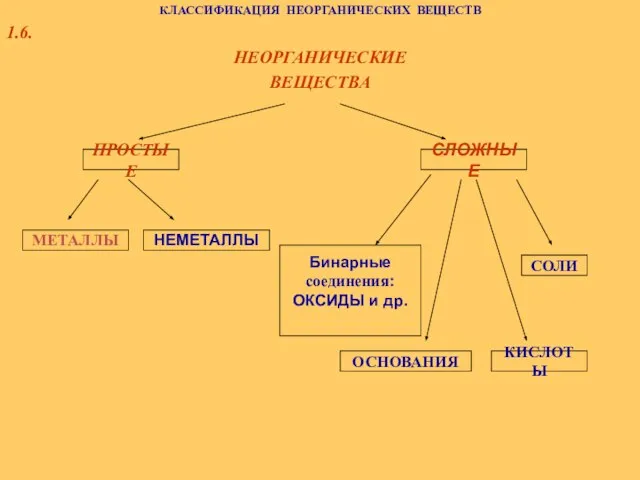 Классификация неорганических веществ
Классификация неорганических веществ