Содержание
- 2. Металлы (Ме) Цели урока: Определить положение металлов в ПСХЭ. Изучить строение атома и строение молекулы металлов.
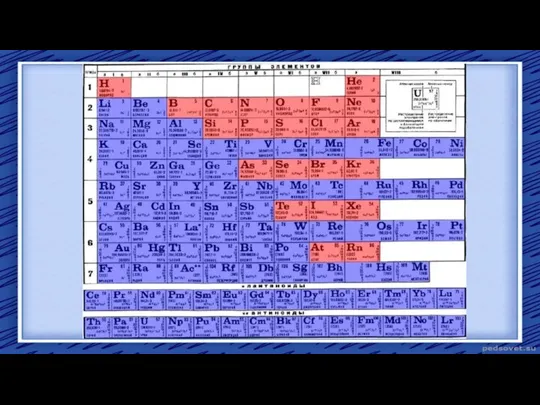
- 4. Положение в ПСХЭ 95 элементов – металлы Это переходные металлы
- 5. Полумета́ллы (металлоиды) - химические элементы, расположенные в ПСХЭ на границе между Ме и НеМе. В разных
- 6. Строение атома ))) 1-3 ē (Искл. Ge, Sn, Pb - 4 ē; Sb, Bi - 5
- 7. Строение молекулы Металлическая связь - это связь в металлах и сплавах, возникающая между катионами металлов, и
- 8. Физические свойства 1. Твердые (искл. Hg). 2. Металлический серебристый блеск (Искл. – Au, Cu, Sr).
- 9. Физические свойства 3. Пластичность. Высокая: Au, Ag, Cu, Sn, Pb. Низкая: Cr, Bi, Mn. 4. Электро-
- 10. Физические свойства Легкие Fe (ρ = 7,87г/см3) Тяжелые Al, Mg, Ti, Na, Li (самый легкий) 5.
- 11. Физические свойства 6. Высокие температуры плавления Zn, Pb, Sn, Na, Ga, Сs, (самые) Легкоплавкие Fe (tпл.
- 12. Физические свойства 7. Отношение к магнитному полю. а) ферромагнетики (хорошо намагничиваются) - Fe, Co, Ni. б)
- 13. Химические свойства М Е Т А Л Л Ы + НеМе 2Fe + 3Cl2 → 2FeCl3
- 15. Скачать презентацию











 Образование первичной структуры белка
Образование первичной структуры белка Железо
Железо Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Сплавы металлов (познавательная презентация)
Сплавы металлов (познавательная презентация) Предмет органической химии. Особенности органических веществ
Предмет органической химии. Особенности органических веществ Отжиг сталей (отжиг 2-го рода) Лекция 2
Отжиг сталей (отжиг 2-го рода) Лекция 2 Металлы II А подгруппы
Металлы II А подгруппы Презентация
Презентация Фосфор - светоносный
Фосфор - светоносный 1662922113131__olk9yp
1662922113131__olk9yp Соединения щелочных металлов
Соединения щелочных металлов Хлор. Химические свойства и применение. Лекция 5
Хлор. Химические свойства и применение. Лекция 5 Сложные неорганические вещества
Сложные неорганические вещества Презентация по Химии "Строение и физические свойства металлов"
Презентация по Химии "Строение и физические свойства металлов"  Основной закон радиоактивного распада и активность радионуклидов
Основной закон радиоактивного распада и активность радионуклидов Контроль качества лекарственных средств, производных аминокислот ароматического ряда. Лекция № 11
Контроль качества лекарственных средств, производных аминокислот ароматического ряда. Лекция № 11 Магматические породы
Магматические породы Строение металлов и их сплавов
Строение металлов и их сплавов Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Материальный и тепловой балансы абсорбции
Материальный и тепловой балансы абсорбции Химия и сельское хозяйство
Химия и сельское хозяйство Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов Vielu īpašības
Vielu īpašības Обмен белков и аминокислот. Синтез заменимых аминокислот
Обмен белков и аминокислот. Синтез заменимых аминокислот Молярный объем газов. Закон Авогадро
Молярный объем газов. Закон Авогадро Сульфиты. Виды сульфидов
Сульфиты. Виды сульфидов Нафтены и арены
Нафтены и арены