Слайд 2Цели:
совершенствовать свои знания в умении составлять уравнения реакций с участием всех

классов неорганических веществ;
экспериментально изучить качественные реакции на Fе2+ и Fе3+
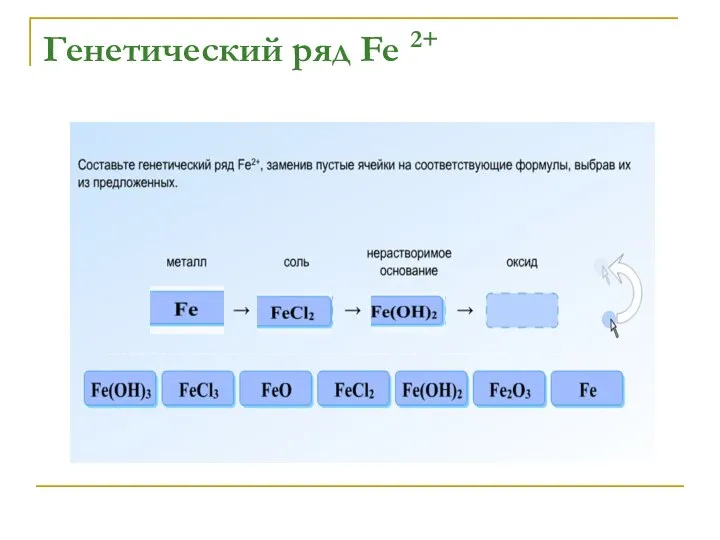
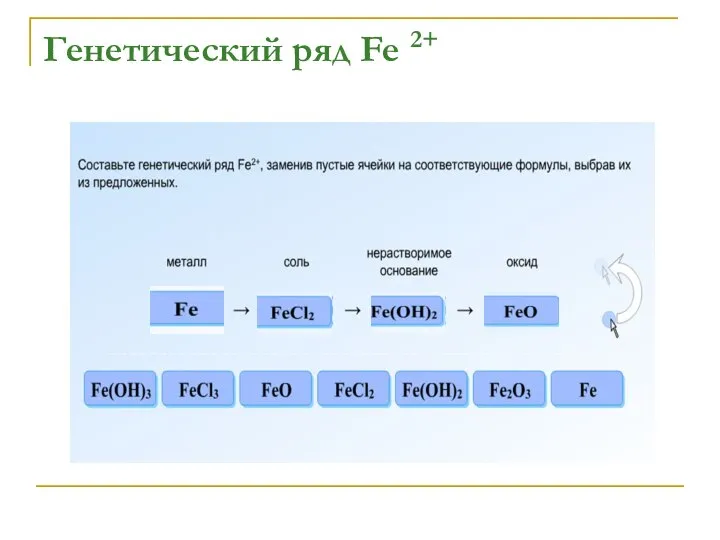
Слайд 13Осуществить превращения:
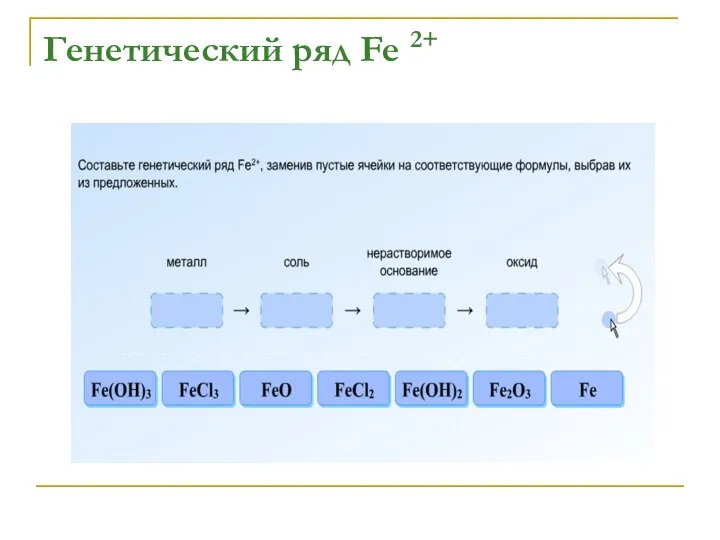
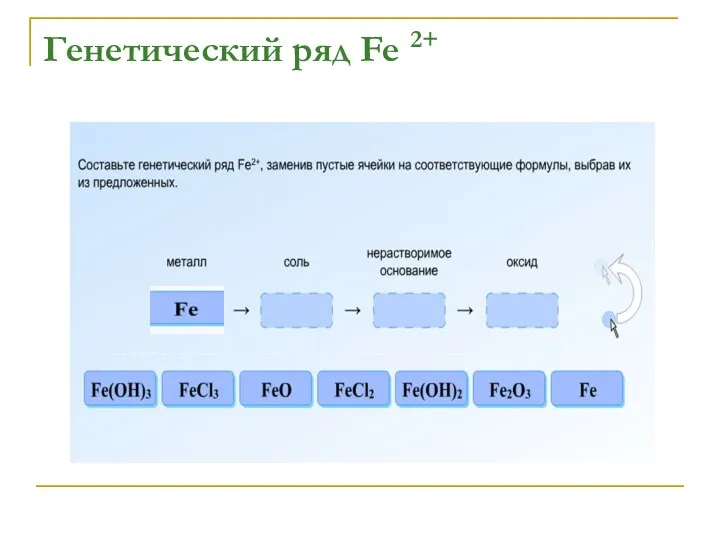
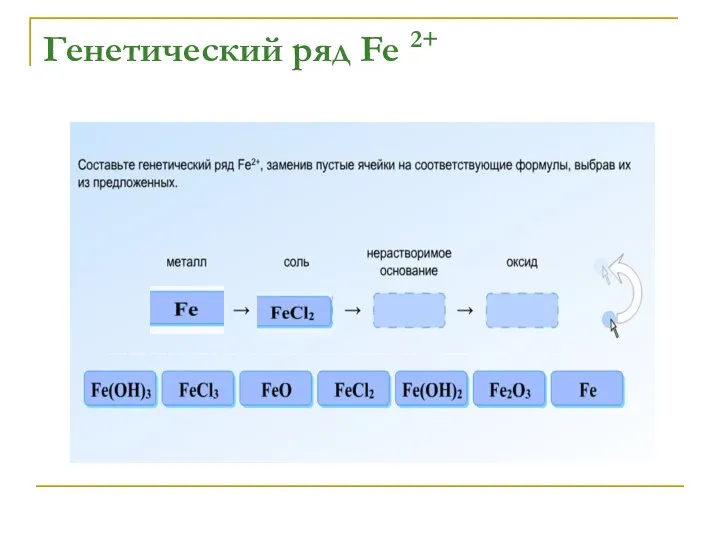
Fe → FeCl2 → Fe(OH)2→ FeO
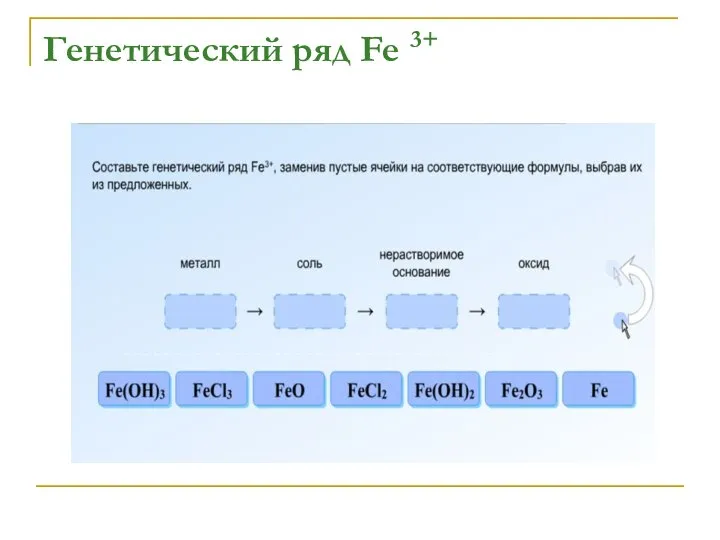
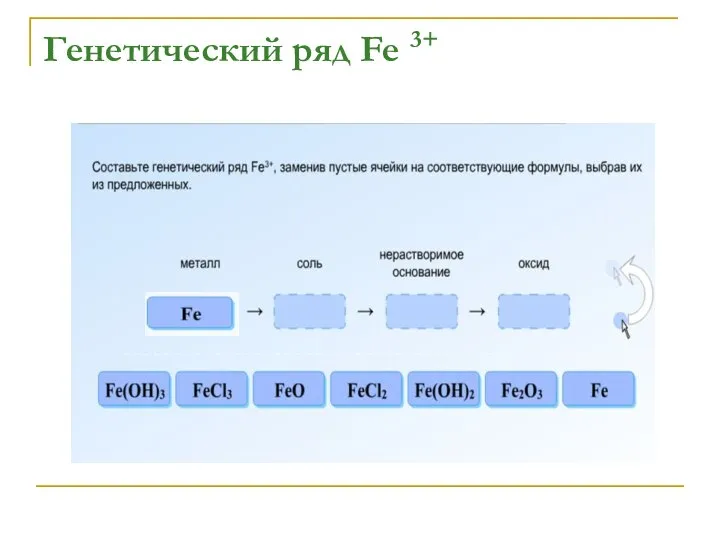
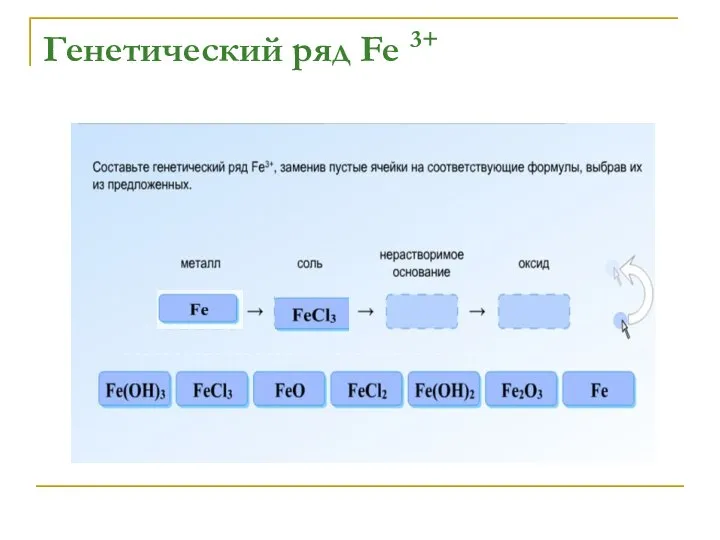
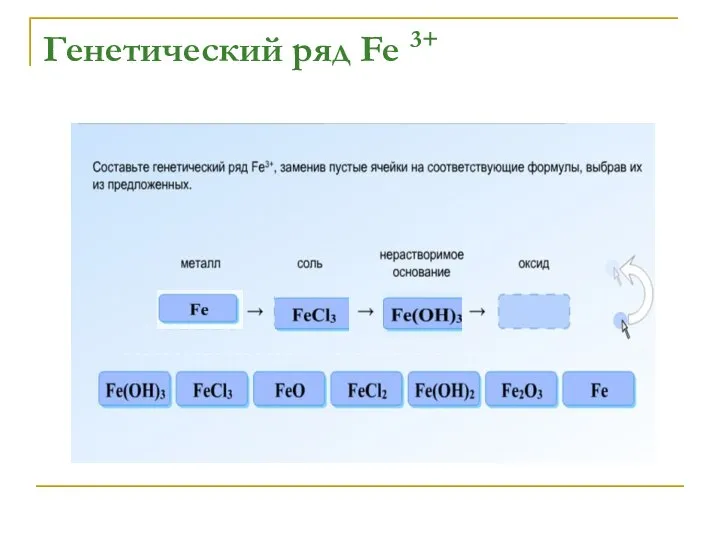
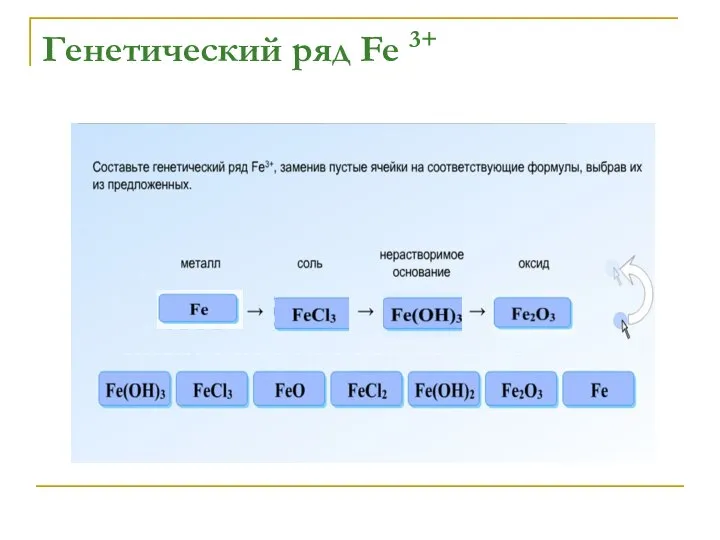
Fe → FeCl3 → Fe(OH)3 →

Fe2O3
Слайд 14Лабораторная работа
I группа
В трех пронумерованных пробирках выданы растворы солей:
NaCl
FeCl2
BaCl2
Определить, в какой

пробирке находится соль железа (II), выбрав для этого подходящий реактив из предложенных
Заполнить таблицу
Сформулировать вывод. Как определить соли железа (II)?
Слайд 15Лабораторная работа
II группа
В трех пронумерованных пробирках выданы растворы солей:
NaCl
FeCl3
BaCl2
Определить, в какой

пробирке находится соль железа (III), выбрав для этого подходящий реактив из предложенных
Заполнить таблицу
Сформулировать вывод. Как определить соли железа (III)?
Слайд 16Лабораторная работа
III группа
Экспериментально определить реактивы для распознавания солей железа (II) и

железа (III)
Заполнить таблицу
Сформулировать выводы
Слайд 17K3[Fe(CN)6]
Красная кровяная соль
Гексацианоферрат (III) калия -
Написать уравнение диссоциации:
K3[Fe(CN)6] =
![K3[Fe(CN)6] Красная кровяная соль Гексацианоферрат (III) калия - Написать уравнение диссоциации: K3[Fe(CN)6] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-16.jpg)
Слайд 18K4[Fe(CN)6]
Желтая кровяная соль
Гексацианоферрат (II) калия
Написать уравнение диссоциации:
K4[Fe(CN)6] =
![K4[Fe(CN)6] Желтая кровяная соль Гексацианоферрат (II) калия Написать уравнение диссоциации: K4[Fe(CN)6] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-17.jpg)
Слайд 19Написать уравнения качественных реакций на ионы Fе2+ и Fе3+
А) Fe SO4 +K3[Fe(CN)6]=
Б) FeCl3 +

K4[Fe(CN)6] =
Слайд 20Написать уравнения качественных реакций на ионы Fе2+ и Fе3+
К3[Fe(CN)6 ] + Fe SO4 = KFe[Fe(CN)6])↓ +
![Написать уравнения качественных реакций на ионы Fе2+ и Fе3+ К3[Fe(CN)6 ] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-19.jpg)
красная кровяная соль турнбуллева синь
+K2SO4
К4[Fe(CN)6 ] + FeCl3 = KFe[Fe(CN)6])↓ + 3KCl
берлинская лазурь
Слайд 21
FeCl2
FeСl3
Fe(OH)2
Fe(OH)3
Fe
K4[Fe(CN)6]
K3[Fe(CN)6]
FeO
Fe2O3
![FeCl2 FeСl3 Fe(OH)2 Fe(OH)3 Fe K4[Fe(CN)6] K3[Fe(CN)6] FeO Fe2O3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-20.jpg)





![K3[Fe(CN)6] Красная кровяная соль Гексацианоферрат (III) калия - Написать уравнение диссоциации: K3[Fe(CN)6] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-16.jpg)
![K4[Fe(CN)6] Желтая кровяная соль Гексацианоферрат (II) калия Написать уравнение диссоциации: K4[Fe(CN)6] =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-17.jpg)

![Написать уравнения качественных реакций на ионы Fе2+ и Fе3+ К3[Fe(CN)6 ] +](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-19.jpg)
![FeCl2 FeСl3 Fe(OH)2 Fe(OH)3 Fe K4[Fe(CN)6] K3[Fe(CN)6] FeO Fe2O3](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/957165/slide-20.jpg)
 Знаки химических элементов. 8 класс
Знаки химических элементов. 8 класс Химия дома
Химия дома Химические средства защиты растений. Последствия применения пестицидов
Химические средства защиты растений. Последствия применения пестицидов Аналитическая химия. Введение
Аналитическая химия. Введение Nxf_uZGQ8YFvfhQYo-sHuA
Nxf_uZGQ8YFvfhQYo-sHuA Презентация на тему Воздух. Кислород. Горение
Презентация на тему Воздух. Кислород. Горение  8. Изотопы. Ядерные реакции
8. Изотопы. Ядерные реакции Превращения в нашей жизни: физические и химические
Превращения в нашей жизни: физические и химические Гипер-гипофосфатемия
Гипер-гипофосфатемия Химическая организация клетки
Химическая организация клетки Курс Технология конструкционных материалов
Курс Технология конструкционных материалов Лиофобные дисперсные системы. Конденсация. Растворение. Флокуляция. Лекция 13
Лиофобные дисперсные системы. Конденсация. Растворение. Флокуляция. Лекция 13 Микропластик в окружающей среде
Микропластик в окружающей среде Периодическая система элементов, строение атома
Периодическая система элементов, строение атома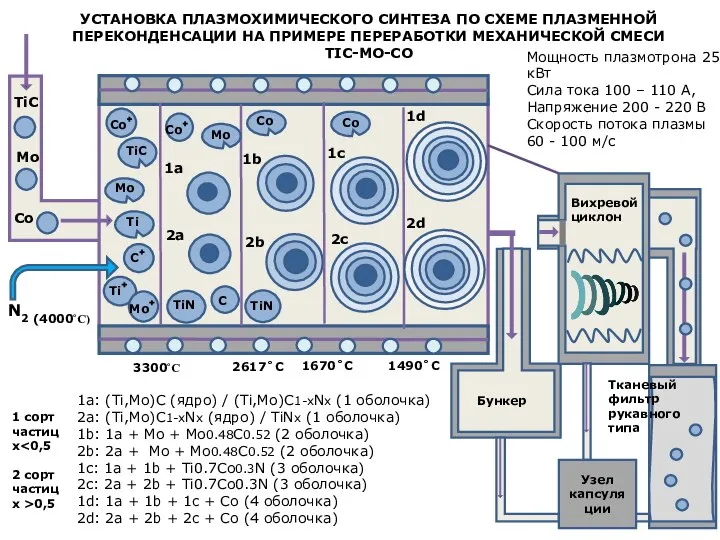 Установка плазмохимического синтеза по схеме плазменной переконденсации на примере переработки механической смеси tic-mo-co
Установка плазмохимического синтеза по схеме плазменной переконденсации на примере переработки механической смеси tic-mo-co Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Классификация органических соединений. Предельные углеводороды (УВ)
Классификация органических соединений. Предельные углеводороды (УВ) Химическая связь в молекулах. Экзаменационные вопросы
Химическая связь в молекулах. Экзаменационные вопросы Химия – это наука о …
Химия – это наука о … Оксиды
Оксиды Кислоты. Классификация кислот
Кислоты. Классификация кислот Полезные ископаемые
Полезные ископаемые Углеводы. Классификация
Углеводы. Классификация Классы неорганических соединений
Классы неорганических соединений Решение задач по органической химии
Решение задач по органической химии Три службы Менделеева для России
Три службы Менделеева для России Теоретические основы органической химии. Строение атома углерода. Гибридизация. Номенклатура и изомерия
Теоретические основы органической химии. Строение атома углерода. Гибридизация. Номенклатура и изомерия Альдегиды (номенклатура и изомерия)
Альдегиды (номенклатура и изомерия)