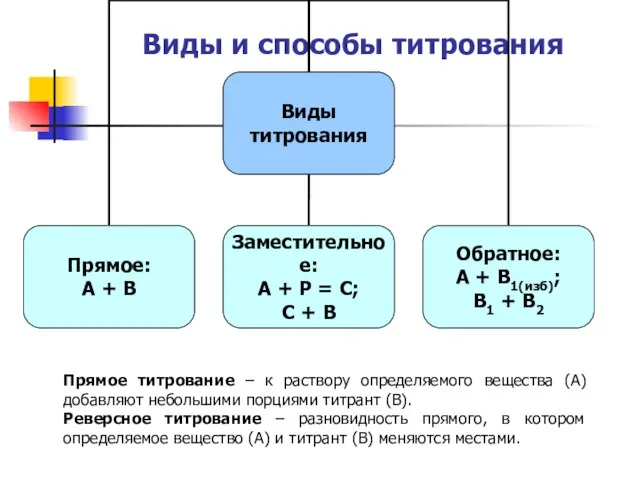
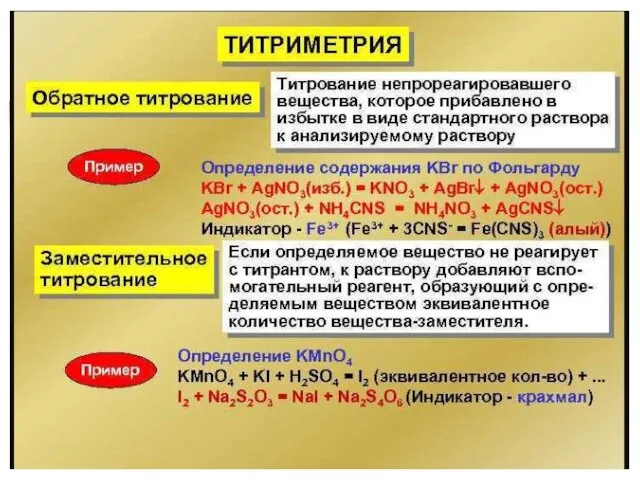
избыточное, но точно измеренное количество титранта-1 (титрант по отношению к определяемому веществу) (В1). Не прореагировавший объем титранта-1 (В1) оттитровывают титрантом-2 (титрант по отношению к титранту 1) (В2). Количество израсходованного титранта-1 (В1) на взаимодействие с определяемым веществом определяют по разнице между добавленным объемом титранта 1 (В1) и его объемом, оттитрованным титрантом-2 (В2).
Заместительное титрование – применяют в тех случаях, когда прямое или обратное титрование вещества невозможно или вызывает затруднение, т.е. непосредственная реакция исследуемого вещества и реагента не удовлетворяет требованиям, предъявляемым к реакциям, применяемым в титриметрии. К определяемому веществу (А) добавляют реагент (Р) в избытке. При этом выделяется эквивалентное определяемому веществу количество заместителя (С), который затем оттитровывают подходящим титрантом (В). Оттитровывается заместитель (С), а в расчетах берется определяемое вещество (А).







 Азот
Азот Презентация на тему Роль йода в организме
Презентация на тему Роль йода в организме  Степень окисления
Степень окисления Понятие о пестицидах. Меры безопасности при работе с ядами
Понятие о пестицидах. Меры безопасности при работе с ядами Презентация на тему Химия в быту
Презентация на тему Химия в быту  Получение металлов
Получение металлов Важнейшие классы неорганических соединений
Важнейшие классы неорганических соединений Валентность, Составление формул
Валентность, Составление формул Алгоритмы при изучении химии
Алгоритмы при изучении химии По страницам истории российской химической науки
По страницам истории российской химической науки Хим-1 презент
Хим-1 презент Кристаллическая структура вещества. Вывод формульных единиц по отношению масс элементов и по массовым долям элементов. (Урок №6)
Кристаллическая структура вещества. Вывод формульных единиц по отношению масс элементов и по массовым долям элементов. (Урок №6) Неметаллы в природе и жизни человека
Неметаллы в природе и жизни человека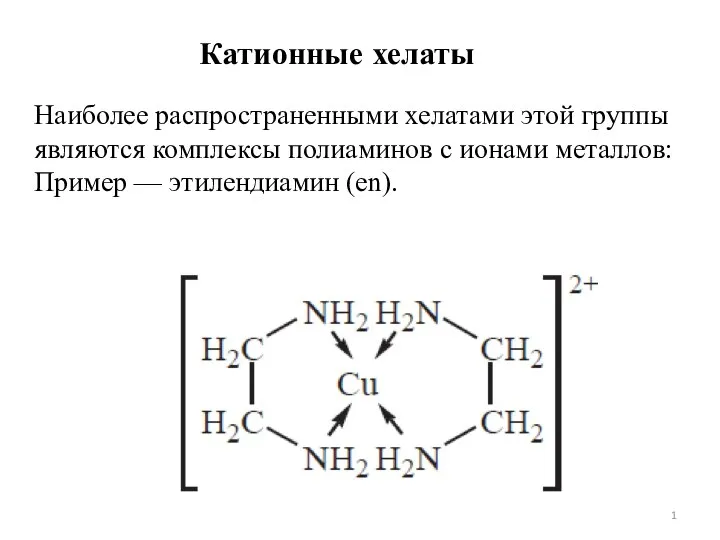 Хелатный эффект. Лекция 7
Хелатный эффект. Лекция 7 Обмен белков и аминокислот. Синтез заменимых аминокислот
Обмен белков и аминокислот. Синтез заменимых аминокислот Неметаллы
Неметаллы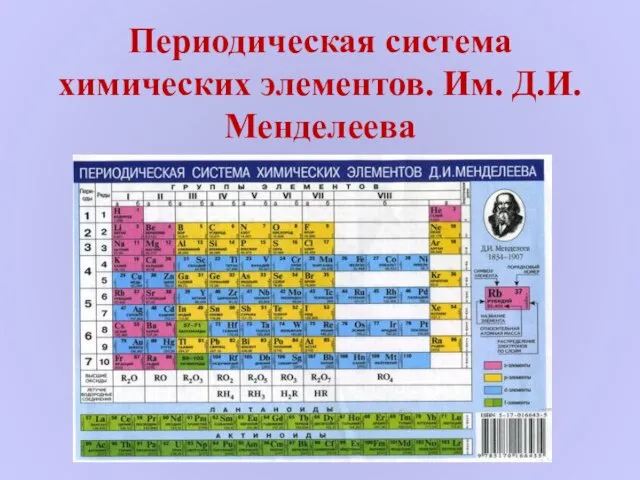 Периодическая система химических элементов. Им. Д.И. Менделеева
Периодическая система химических элементов. Им. Д.И. Менделеева Простые вещества – неметаллы. Аллотропия
Простые вещества – неметаллы. Аллотропия Презентация на тему Стекло
Презентация на тему Стекло  Исследовательская работа на тему: «Выращивание кристалла в домашних условиях» Работу выполнила ученица 10-а класса Алексеева О
Исследовательская работа на тему: «Выращивание кристалла в домашних условиях» Работу выполнила ученица 10-а класса Алексеева О Аналитическая химия
Аналитическая химия Презентация на тему Массовая доля вещества в растворе
Презентация на тему Массовая доля вещества в растворе  _ _Производство цветных металлов. Методы плавки алюминия_
_ _Производство цветных металлов. Методы плавки алюминия_ Углеводороды в природе
Углеводороды в природе Презентация на тему Всё об алюминии
Презентация на тему Всё об алюминии  Исследование снега на общую химическую токсичность методом биотестирования Автор: Милюта Юлия, Тюменская область, Тюменский рай
Исследование снега на общую химическую токсичность методом биотестирования Автор: Милюта Юлия, Тюменская область, Тюменский рай Порох. Сера, халькогены
Порох. Сера, халькогены Сложные неорганические вещества
Сложные неорганические вещества