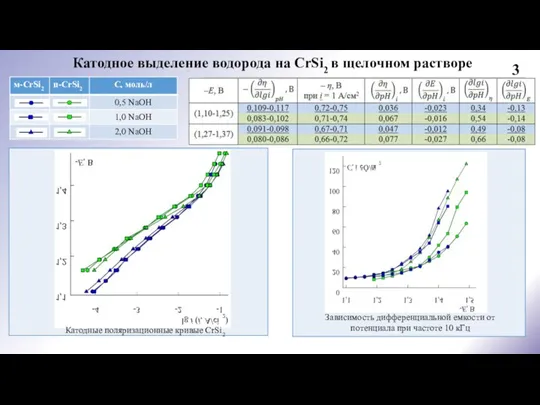
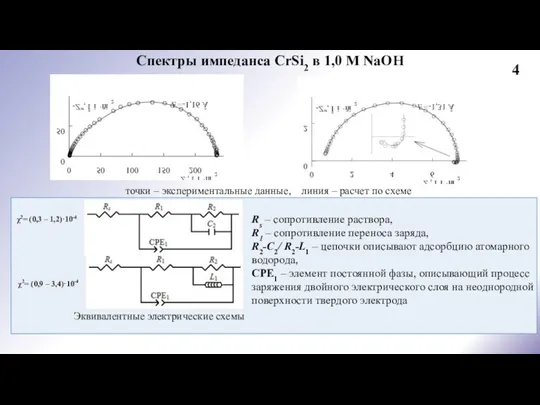
CrSi2-электроде в щелочном электролите протекает по маршруту разряд-электрохимическая десорбция с замедленной стадией десорбцией; в области высоких катодных поляризаций – по маршруту разряд-электрохимическая десорбция с замедленной стадией разряда; обе стадии необратимы, коэффициенты переноса стадий равны, одновременно протекает реакция абсорбции водорода в кинетическом режиме (во всем исследованном диапазоне потенциалов); для адсорбированного атомарного водорода выполняется изотерма адсорбции Ленгмюра.
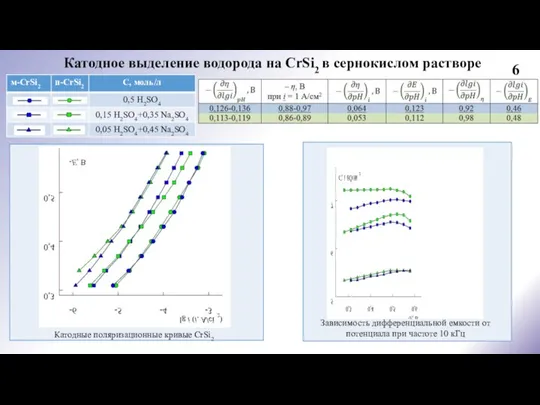
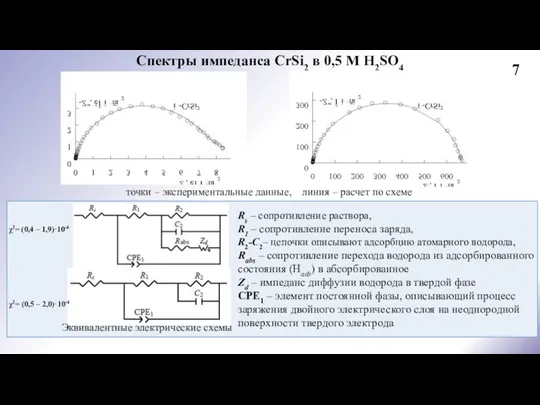
2. Найдено, что реакция выделения водорода на CrSi2-электроде в сернокислом электролите протекает по маршруту разряд – электрохимическая десорбция с замедленной стадией десорбцией, обе стадии необратимы, коэффициенты переноса равны, одновременно с реакцией выделения водорода протекает реакция абсорбции водорода для м-CrSi2 со смешанным диффузионно-кинетическим контролем, для п-CrSi2 – с кинетическим контролем; для Надс выполняется изотерма адсорбции Ленгмюра. Отмечается влияние тонкой оксидной пленки на кинетику выделения водорода на CrSi2 при невысоких катодных поляризациях.
3. Обнаружено, что механизм реакции выделения водорода на моно- и поликристаллическом CrSi2-электродах одинаков; изменение кинетических параметров р.в.в. на п-CrSi2 по сравнению с м-CrSi2 обусловлено структурой материала – на поликристаллическом электроде процесс абсорбции протекает более интенсивно.
4. Сделан вывод, что CrSi2 в щелочном и сернокислом электролитах представляет перспективный электродный материал, проявляющий активность в реакции электролитического выделения водорода.
Выводы




 Вещество как система. Основы классификации и номенклатуры неорганических веществ
Вещество как система. Основы классификации и номенклатуры неорганических веществ Презентация на тему Микроэлементы: Хром, Йод, Фтор
Презентация на тему Микроэлементы: Хром, Йод, Фтор  Скорость химических реакций
Скорость химических реакций Липиды
Липиды Алкены (часть 2)
Алкены (часть 2) Основания, их состав и название
Основания, их состав и название Презентация на тему Природный и попутный нефтяной газы, их состав, использование
Презентация на тему Природный и попутный нефтяной газы, их состав, использование  Свойства Н2
Свойства Н2 Электроны в кристаллах. Приложения зонной теории
Электроны в кристаллах. Приложения зонной теории Разбор контрольной работы. Химия (9 класс)
Разбор контрольной работы. Химия (9 класс) Пересчет данных анализа, выраженных в ионной форме
Пересчет данных анализа, выраженных в ионной форме Кабинет химии
Кабинет химии Типичные реакции оснований
Типичные реакции оснований Спирты в жизни человека
Спирты в жизни человека Строение бензола
Строение бензола Обновление экзаменационных моделей ОГЭ и ЕГЭ по химии
Обновление экзаменационных моделей ОГЭ и ЕГЭ по химии Внеклассное мероприятие по химии Первоначальные химические понятия
Внеклассное мероприятие по химии Первоначальные химические понятия Теоретические основы каталитических процессов переработки нефтегазового сырья. Тема 6
Теоретические основы каталитических процессов переработки нефтегазового сырья. Тема 6 Аргентум, или серебро
Аргентум, или серебро Химические свойства карбоновых кислот
Химические свойства карбоновых кислот Алкины. Понятие об алкинах
Алкины. Понятие об алкинах Влияние эллементов на состав растений. Содержание тяжелого металла в растениях. Нитраты в растениях
Влияние эллементов на состав растений. Содержание тяжелого металла в растениях. Нитраты в растениях Металлы
Металлы Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Иттрий-алюминиевый гранат и иттрий-алюминиевый перовскит
Иттрий-алюминиевый гранат и иттрий-алюминиевый перовскит Презентация на тему Вода – растворитель
Презентация на тему Вода – растворитель  Медь и ее сплавы
Медь и ее сплавы Методика изготовления сенсора
Методика изготовления сенсора