Содержание
- 4. Водород Вещество и элемент Газ без цвета, вкуса и запаха
- 5. 2. Историческая справка 1766 г. – водород открыл Г. Кавендиш 1784 г. – А. Лавуазье назвал
- 6. Антуан Лоран Лавуазье 1743–1794 гг. Генри Кавендиш 1731–1810 гг.
- 8. Водород
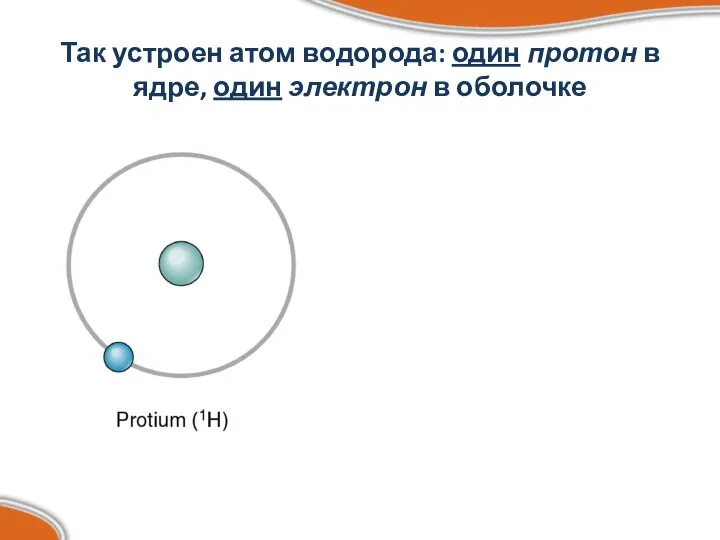
- 9. Так устроен атом водорода: один протон в ядре, один электрон в оболочке
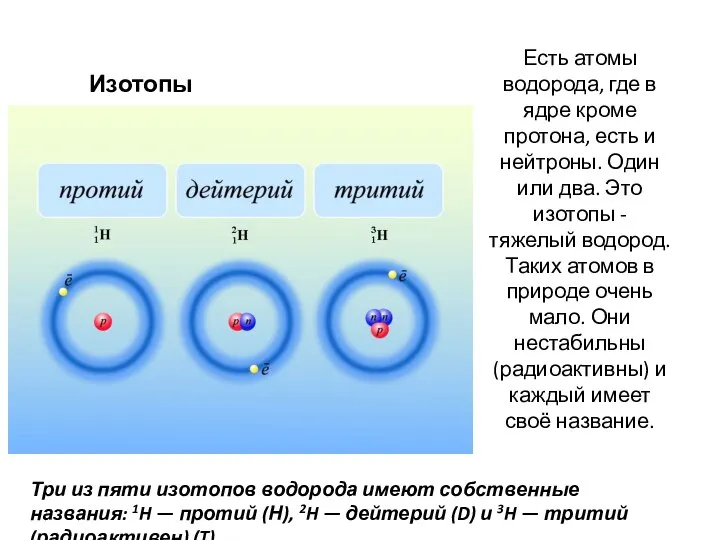
- 10. Есть атомы водорода, где в ядре кроме протона, есть и нейтроны. Один или два. Это изотопы
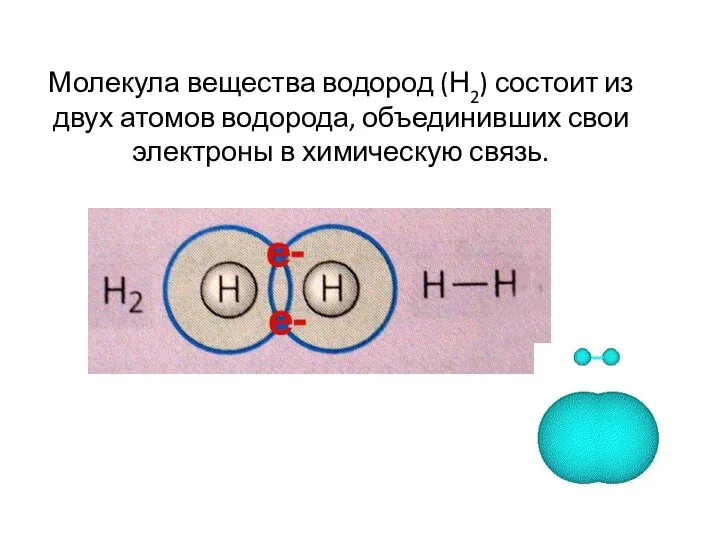
- 11. Молекула вещества водород (Н2) состоит из двух атомов водорода, объединивших свои электроны в химическую связь.
- 12. Физические свойства Н2 Газ без цвета, вкуса и запаха. Легче воздуха в 14,5 раз. Плохо растворим
- 13. Физические свойства t0пл. -259,10 С; t0 кип. -2530 С; теплопроводность в 7 раз больше чем воздуха;
- 14. Получение водорода В лаборатории: Взаимодействие цинка с соляной кислотой: Zn+2HCl=ZnCl2+ H2 Взаимодействие калия с водой: 2К+2H2O=2KOH+H2
- 15. Химические свойства Взаимодействие с простыми веществами Взаимодействие со сложными веществами H2
- 16. Химические свойства Взаимодействие с металлами: Ca + H2 = CaH2 CaH2 + 2H2O = Ca(OH)2 +
- 17. I.Взаимодействие с простыми веществами 1) Взаимодействие с неметаллами 1. O2 + 2H2 = 2Н2О 2. S
- 18. Смесь водорода с одним объемом кислорода – гремучий газ Смесь водорода и воздуха – взрывоопасна! Обычно
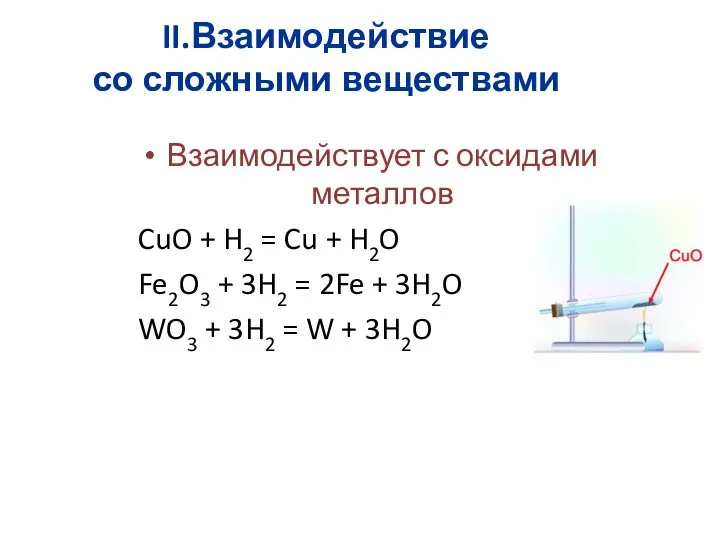
- 19. II.Взаимодействие со сложными веществами Взаимодействует с оксидами металлов CuO + H2 = Cu + H2O Fe2O3
- 20. ПРОВЕРЬ СЕБЯ 1. Водород проявляет степень окисления в соединениях: А) +1 и -1; Б) +2 и
- 21. ОТВЕТЫ А Б В Б А
- 22. Допиши химические реакции и укажи их тип: 1. H2O2 = 6. HgO= 2. S + O2=
- 24. Скачать презентацию













 Химия и производство. Химическая промышленность
Химия и производство. Химическая промышленность Простые вещества в стране Химляндии. 8 класс
Простые вещества в стране Химляндии. 8 класс Двовимірний ямр. Основні принципи
Двовимірний ямр. Основні принципи (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А Гидролиз солей
Гидролиз солей Язык естествознания. Химия
Язык естествознания. Химия Презентация по Химии "Ароматы и чем они «пахнут»"
Презентация по Химии "Ароматы и чем они «пахнут»"  Углеводы: моно-, ди-, полисахариды
Углеводы: моно-, ди-, полисахариды Презентация на тему Растворы (11 класс)
Презентация на тему Растворы (11 класс)  Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Дизайн молекулярных магнетиков
Дизайн молекулярных магнетиков Вода. Строение молекулы воды. Анализ и синтез воды
Вода. Строение молекулы воды. Анализ и синтез воды Кальций и его соединения. 9 класс
Кальций и его соединения. 9 класс Химические свойства и получение спиртов
Химические свойства и получение спиртов Презентация на тему Валентные состояния атома углерода
Презентация на тему Валентные состояния атома углерода  9 кл Урок 7 Розчинність речовин
9 кл Урок 7 Розчинність речовин Карбоновые кислоты
Карбоновые кислоты Простые и сложные вещества. Основные классы неорганических веществ
Простые и сложные вещества. Основные классы неорганических веществ Презентация на тему Атомы химических элементов
Презентация на тему Атомы химических элементов  Получение галогенов. Биологическое значение и применение галогенов и их соединений
Получение галогенов. Биологическое значение и применение галогенов и их соединений Силумины. Виды силуминов
Силумины. Виды силуминов Степень окисления
Степень окисления Амфотерность. Амфотерные соединения
Амфотерность. Амфотерные соединения Физическая и коллоидная химия
Физическая и коллоидная химия Жиры. Открытие жиров
Жиры. Открытие жиров khim
khim Органические вещества
Органические вещества Неметаллические материалы
Неметаллические материалы