Слайд 2Цель урока:
Выяснить, что такое скорость химической реакции.
Выяснить, какие факторы и как влияют

на скорость химической реакции.
Слайд 3
Скорость химической реакции:
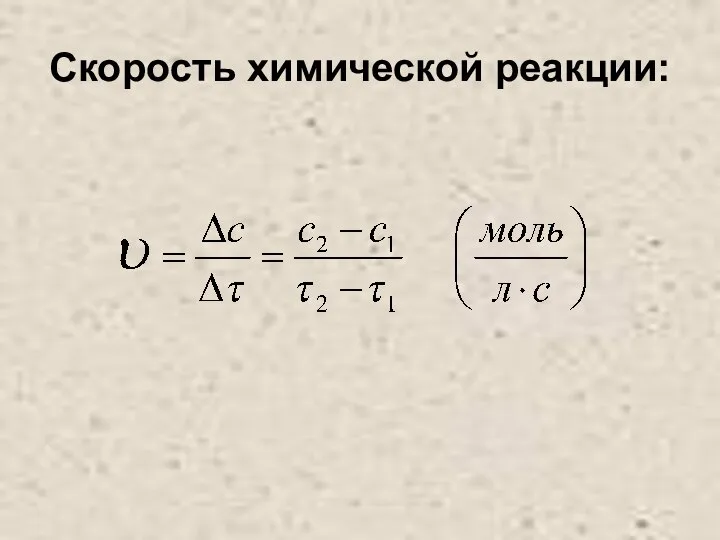
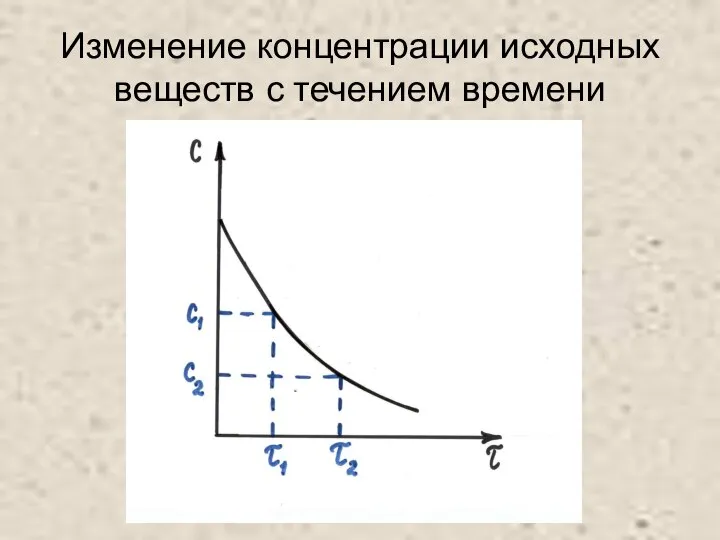
Слайд 4Изменение концентрации исходных веществ с течением времени
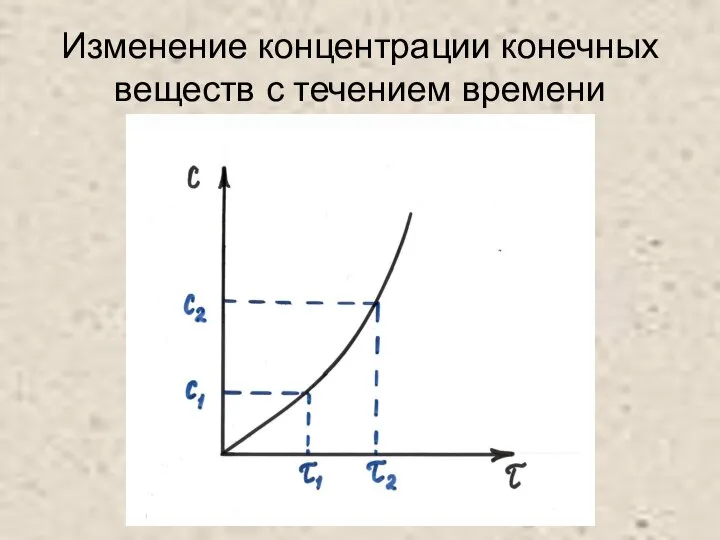
Слайд 5Изменение концентрации конечных веществ с течением времени
Слайд 6Скорость химической реакции в гомогенной системе:

Слайд 7Скорость химической реакции в гетерогенной системе:

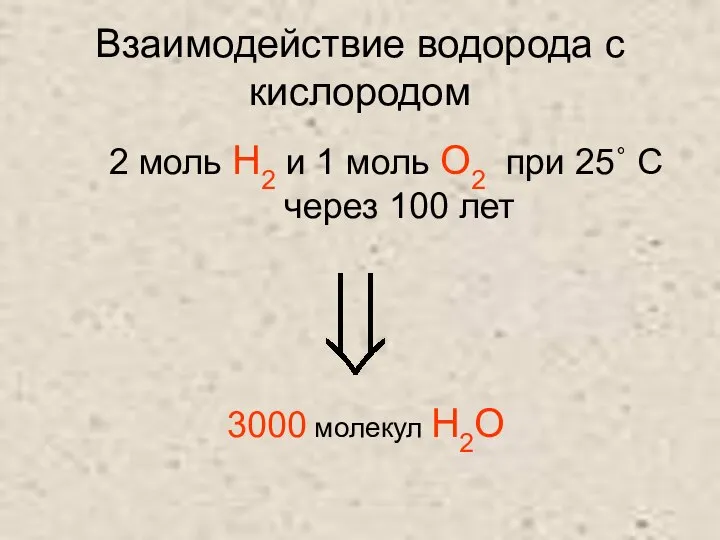
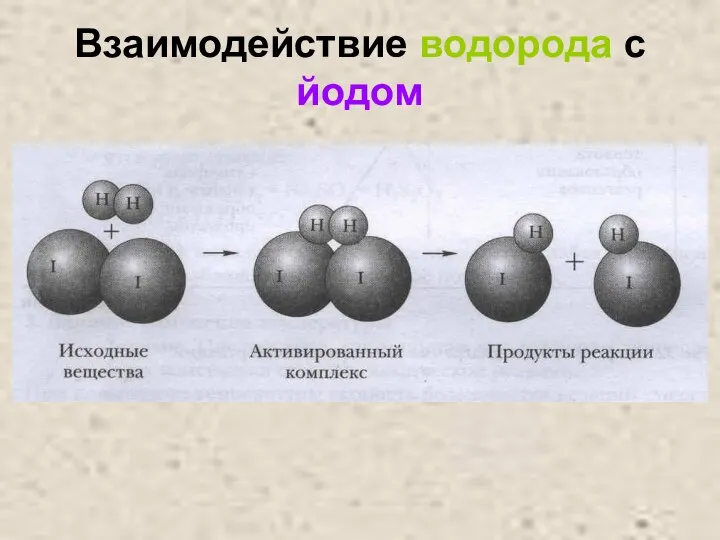
Слайд 8Взаимодействие водорода с кислородом
2 моль H2 и 1 моль О2 при 25˚
С
через 100 лет
3000 молекул H2О
Слайд 9Влияние на скорость реакции
различных факторов

Слайд 101) Природа реагирующих веществ
Zn + 2HCl = ZnCl2 + H2 ↑
Zn
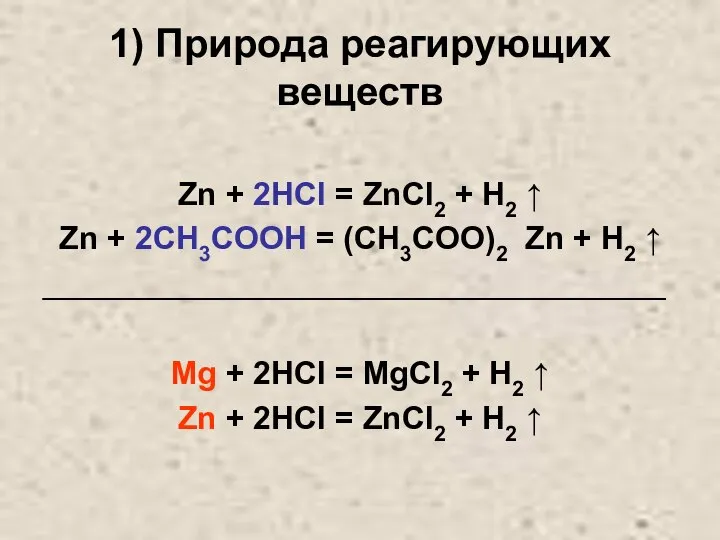
+ 2CH3COOH = (CH3COO)2 Zn + H2 ↑
___________________________________
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Слайд 112) Концентрация реагирующих веществ
Zn + 2HCl = ZnCl2 + H2 ↑
а) раствор

HCl
б) концентрированная HCl
Слайд 12Закон «действующих масс»:
Скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ.

Слайд 13Взаимодействие водорода с азотом

Слайд 15
3) Величина поверхности соприкосновения реагирующих веществ
CaCO3 + 2HCl = CaCl2 + H2O

+ CO2 ↑
а) кусочек CaCO3
б) измельченный CaCO3
Слайд 164) Температура
Правило Вант-Гоффа:
При повышении температуры на каждые 100 C скорость большинства

реакций увеличивается в 2-4 раза.
Слайд 17Правило Вант-Гоффа:
Где - температурный коэффициент

Слайд 18Задача:
Во сколько раз увеличится скорость реакции?

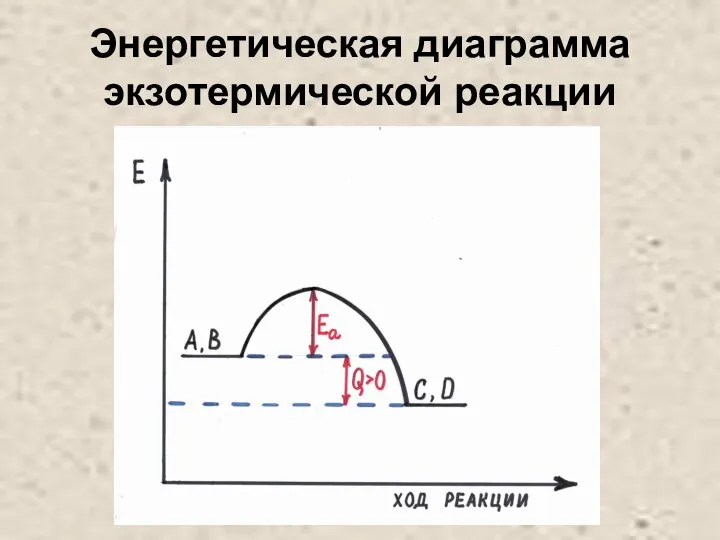
Слайд 24Энергетическая диаграмма экзотермической реакции
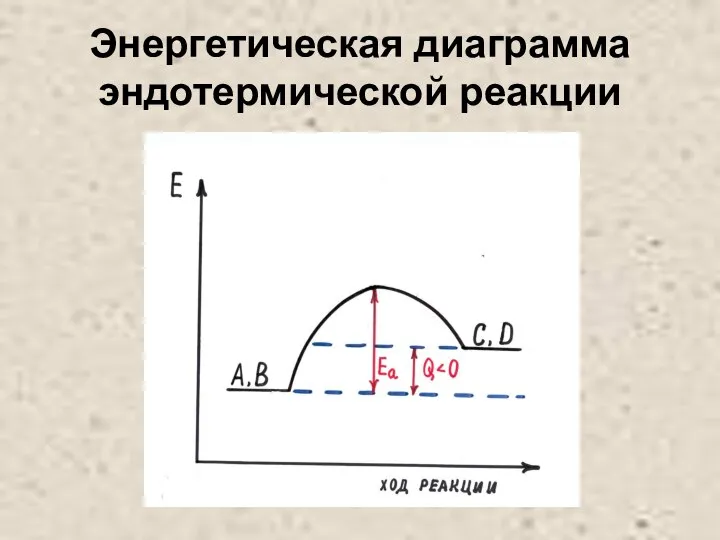
Слайд 25Энергетическая диаграмма эндотермической реакции
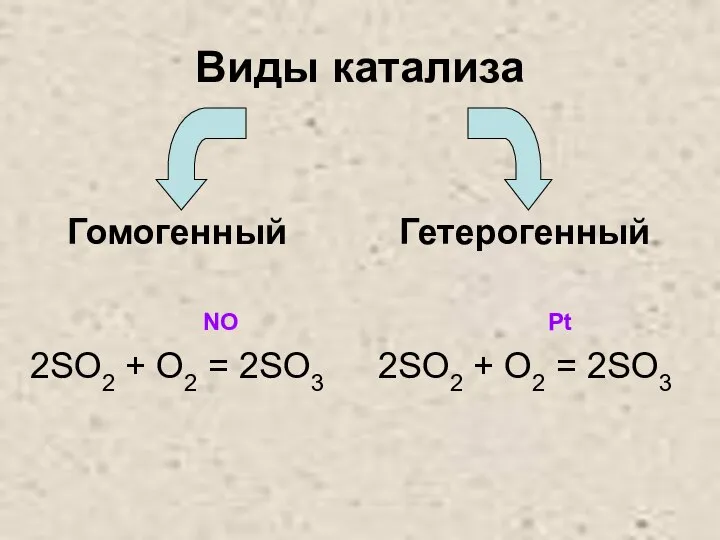
Слайд 26Виды катализа
Гомогенный
NO
2SO2 + O2 = 2SO3
Гетерогенный
Pt
2SO2 + O2 = 2SO3
Слайд 27Механизм действия катализаторов
Для гомогенного катализа:
K
A + B = AB
A + K

= [AK]
[AK] + B = AB + K
Слайд 28Окисление SO2 в SO3
NO
SO2 + ½ O2 = SO3
NO + ½

O2 = NO2
SO2 + NO2 = SO3 + NO
Слайд 29Разложение H2O2
раствор K2Cr2O7
2H2O2 = 2H2O + O2 ↑


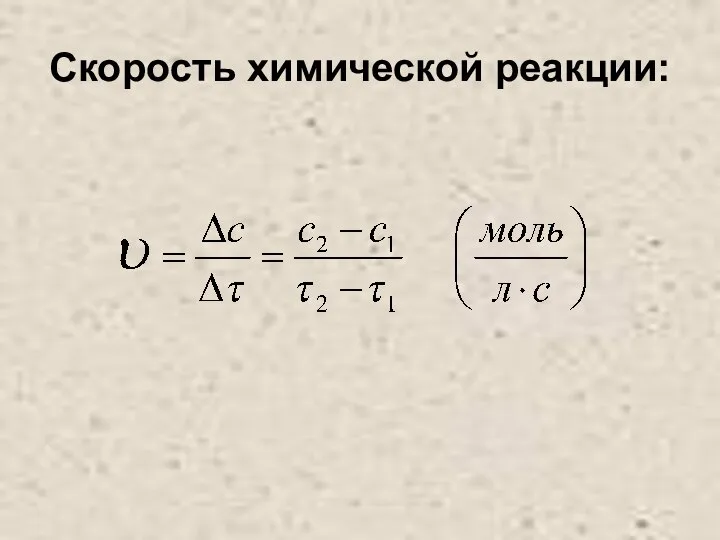























 Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения
Важнейшие классы бинарных соединений – оксиды и летучие водородные соединения Судың диссоциациясы
Судың диссоциациясы Бордос сұйықтығын дайындау және оның сапасын тексеру
Бордос сұйықтығын дайындау және оның сапасын тексеру Общие химические свойства неметаллов. Урок в 10 классе
Общие химические свойства неметаллов. Урок в 10 классе Презентация на тему Славный путь М.В. Ломоносова
Презентация на тему Славный путь М.В. Ломоносова  Полимеры
Полимеры Метелёва И.Е. учитель химии
Метелёва И.Е. учитель химии Биологическая роль III(A) группы
Биологическая роль III(A) группы Проект синтеза бензина для промышленных целей отделения Д-3 цеха Д 2-6-3-5-12
Проект синтеза бензина для промышленных целей отделения Д-3 цеха Д 2-6-3-5-12 Почему амины считают органическими основаниями?
Почему амины считают органическими основаниями? Свойства неорганических веществ
Свойства неорганических веществ Карбоновые кислоты
Карбоновые кислоты Карбоновые кислоты
Карбоновые кислоты Карбоновые кислоты. Тест. 10 класс
Карбоновые кислоты. Тест. 10 класс Fyzikálne a chemické deje
Fyzikálne a chemické deje Концепция химической связи
Концепция химической связи Презентация на тему Катализ
Презентация на тему Катализ  Скорость химической реакции
Скорость химической реакции Названия и формулы кислот
Названия и формулы кислот Чистые вещества и смеси
Чистые вещества и смеси Кетоны. Номенклатура
Кетоны. Номенклатура Санитарно-гигиенические показатели питьевой воды
Санитарно-гигиенические показатели питьевой воды Строение атома
Строение атома Скорость химической реакции
Скорость химической реакции Презентация на тему Алхимики
Презентация на тему Алхимики  Гибридизация АО. Пространственное строение молекул (геометрия молекул)
Гибридизация АО. Пространственное строение молекул (геометрия молекул) Нахождение формулы вещества по массовым долям элементов
Нахождение формулы вещества по массовым долям элементов