Содержание
- 2. ДОД
- 3. Комплексные соединения - это сложные вещества, в состав которых входят комплексный катион и анион, либо катион
- 4. Комплексные соединения / координационные соединения — частицы (нейтральные молекулы или ионы), которые образуются в результате присоединения
- 5. Комплексообразователь – это d-элемент, обладающий достаточным количеством свободных орбиталей (Cu+2, Ag+, Pt+4, Fe+2, Fe+3, Co+2, Co+3,
- 6. Комплексные соли/соединения [Ag(NH3)2]Cl [Cu(H2O)4]SO4 ∙ H2O K4[Fe(CN)6] Li[AlH4] K3[Fe(CN)6]
- 7. Комплексные соли/соединения Катионные [Co(NH3)6]3+ Анионные [CoF6]3- нейтральные [Al (H2O)3(OH)3] Соединения с комплексными анионами:
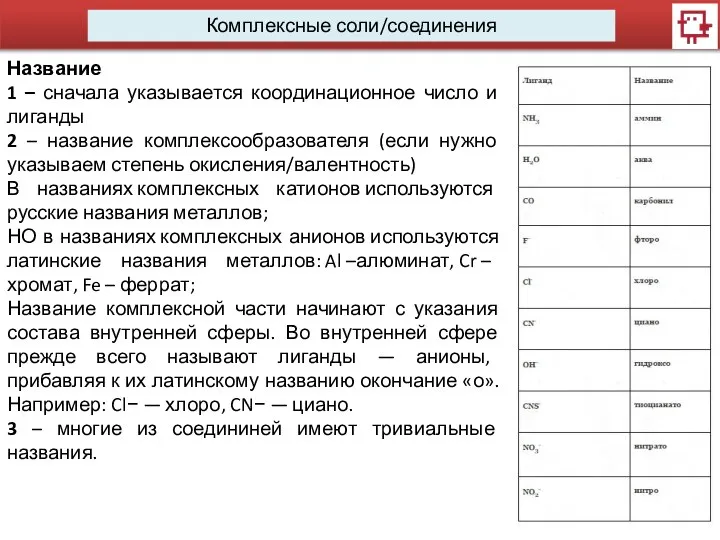
- 8. Комплексные соли/соединения Название 1 – сначала указывается координационное число и лиганды 2 – название комплексообразователя (если
- 9. Комплексные соли/соединения K4[Fe(CN)6] – гексацианоферрат (II) калия (жёлтая кровяная соль) K3[Fe(CN)6] – гексацианоферрат (III) калия (красная
- 10. Комплексные соли/соединения Диссоциация ступенчатая Na2[Zn(OH)4] →2Na+ + [Zn(OH)4]2- (первая ступень – необратимо) [Zn(OH)4]2- ↔ Zn2+ +
- 11. Комплексные соли/соединения трихлоротриамминкобальт Цис- транс- изомерия
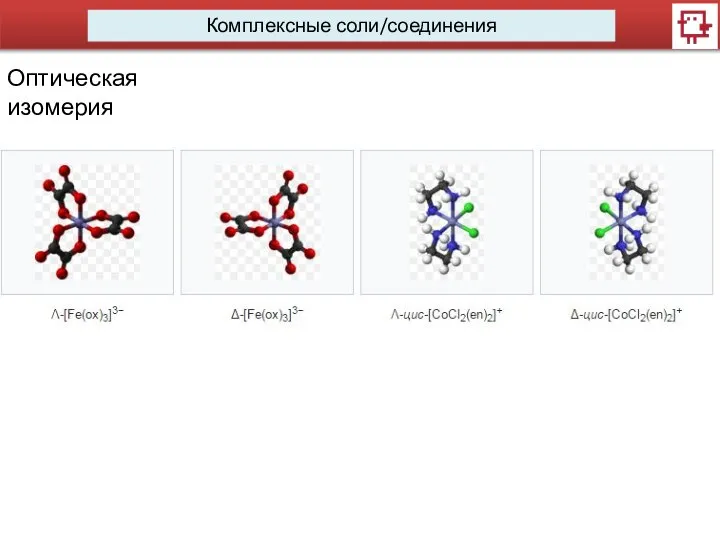
- 12. Комплексные соли/соединения Оптическая изомерия
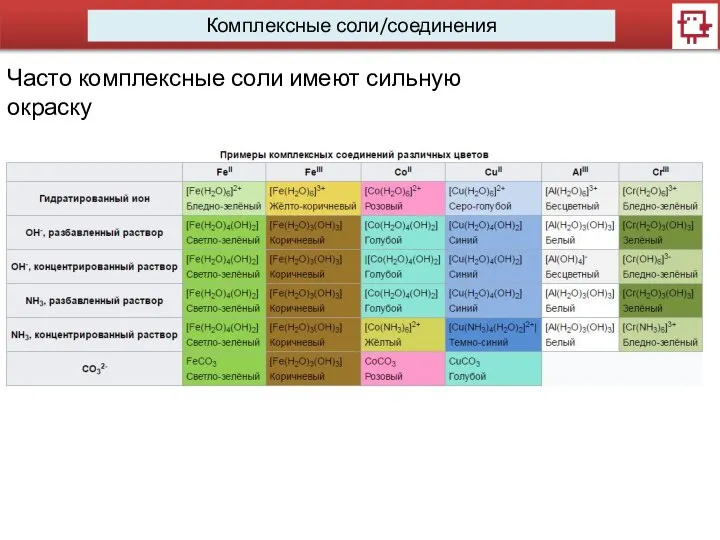
- 13. Комплексные соли/соединения Часто комплексные соли имеют сильную окраску
- 15. Скачать презентацию



![Комплексные соли/соединения [Ag(NH3)2]Cl [Cu(H2O)4]SO4 ∙ H2O K4[Fe(CN)6] Li[AlH4] K3[Fe(CN)6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/950044/slide-5.jpg)
![Комплексные соли/соединения Катионные [Co(NH3)6]3+ Анионные [CoF6]3- нейтральные [Al (H2O)3(OH)3]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/950044/slide-6.jpg)
![Комплексные соли/соединения K4[Fe(CN)6] – гексацианоферрат (II) калия (жёлтая кровяная соль) K3[Fe(CN)6] –](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/950044/slide-8.jpg)
![Комплексные соли/соединения Диссоциация ступенчатая Na2[Zn(OH)4] →2Na+ + [Zn(OH)4]2- (первая ступень – необратимо)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/950044/slide-9.jpg)

 Презентация на тему Соединения серы
Презентация на тему Соединения серы  Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Незаменимая уксусная кислота
Незаменимая уксусная кислота Перегонка. Вклад алхимиков в органическую химию
Перегонка. Вклад алхимиков в органическую химию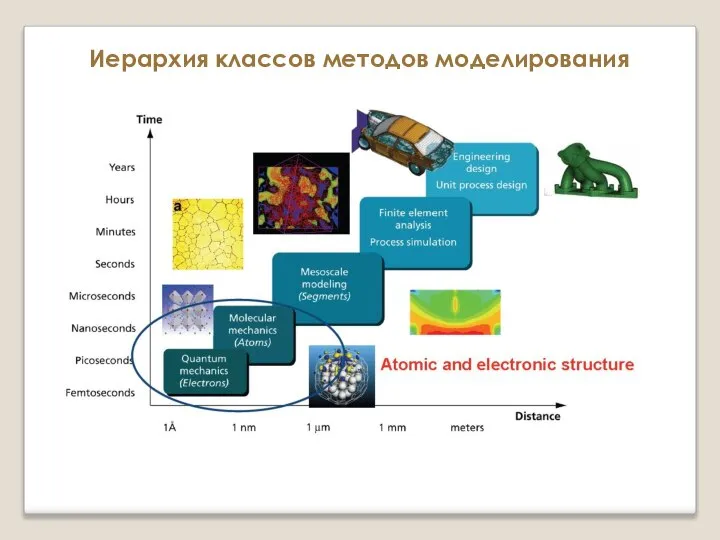 Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Магний и кальций
Магний и кальций Сахароза, крахмал, целлюлоза
Сахароза, крахмал, целлюлоза Строение сложного фермента
Строение сложного фермента Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент
Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Углеводороды. Общие знания
Углеводороды. Общие знания Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Заполни электронные уровни элементов
Заполни электронные уровни элементов Явление аллотропии
Явление аллотропии Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Центробежное осаждение
Центробежное осаждение Характеристика кислорода и серы
Характеристика кислорода и серы Актуальные задачи химии
Актуальные задачи химии Металлы - наши друзья или враги
Металлы - наши друзья или враги Получение, свойства и применение алкенов
Получение, свойства и применение алкенов Классификация силикатов
Классификация силикатов Способы получения металлов
Способы получения металлов Фуллерены
Фуллерены 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Природные источники углеводородов
Природные источники углеводородов علاوي الندوة
علاوي الندوة Цезій
Цезій