Содержание
- 2. Первооткрывателями кислорода и водорода считаются: Французский химик Антуан Лоран Лавуазье. Он был управляющим селитровым и пороховым
- 3. Лавуазье, Пристли и Шееле произвели ряд опытов. Сначала они открыли кислород в воде и воздухе. Но
- 4. Синтез воды Водород и кислород соединяются с образованием воды в тех же объемных отношениях (2:1), в
- 5. Физические свойства воды Цвет подземных вод зависит от их химического состава и механических примесей. Обычно подземные
- 6. Электропроводность подземных вод зависит от количества растворенных в них солей. Пресные воды обладают незначительной электропроводностью. Дистиллированная
- 7. Химические свойства воды Взаимодействие с простыми веществами При комнатной температуре вода реагирует с активными металлами с
- 8. Взаимодействие со сложными веществами Вода реагирует с оксидами активных металлов с образованием щелочей: Вода реагирует с
- 10. Скачать презентацию
Слайд 2Первооткрывателями кислорода и водорода считаются:
Французский химик Антуан Лоран Лавуазье. Он был управляющим селитровым и
Первооткрывателями кислорода и водорода считаются:
Французский химик Антуан Лоран Лавуазье. Он был управляющим селитровым и

пороховым заводом, а позднее, после победы французской буржуазной революции, комиссаром национальной казны, одним из влиятельнейших людей Франции.
Английский химик Генри Кавендиш, родом из старой герцогской семьи, пожертвовавший значительную долю своего состояния науке.
Соотечественник Кавендиша, Джозеф Пристли. Он был священником. Как ярый сторонник французской революции, Пристли был изгнан из Англии и бежал в Америку.
Известный шведский химик Карл Вильгельм Шееле, фармацевт.
Английский химик Генри Кавендиш, родом из старой герцогской семьи, пожертвовавший значительную долю своего состояния науке.
Соотечественник Кавендиша, Джозеф Пристли. Он был священником. Как ярый сторонник французской революции, Пристли был изгнан из Англии и бежал в Америку.
Известный шведский химик Карл Вильгельм Шееле, фармацевт.
Слайд 3Лавуазье, Пристли и Шееле произвели ряд опытов. Сначала они открыли кислород в воде
Лавуазье, Пристли и Шееле произвели ряд опытов. Сначала они открыли кислород в воде

и воздухе. Но Лавуазье не удовлетворился тем, что открыл кислород. Он хотел знать, с какими веществами соединяется кислород. Почти одновременно с Кавендишем, который тоже разложил воду на составные части, Лавуазье открыл водород. Этот элемент получил название «Hydrogenium».
Откуда же берется вода? Вода возникает из пламени: при сгорании водорода, иначе говоря, при соединении водорода с кислородом образуется водяной пар. Так произошло открытие состава воды.
Откуда же берется вода? Вода возникает из пламени: при сгорании водорода, иначе говоря, при соединении водорода с кислородом образуется водяной пар. Так произошло открытие состава воды.
Слайд 4Синтез воды
Водород и кислород соединяются с образованием воды в тех же объемных
Синтез воды
Водород и кислород соединяются с образованием воды в тех же объемных

отношениях (2:1), в каких они выделяются при её разложении. Это можно подтвердить опытом в приборе, называемом эвдиометром. Эвдиометр представляет собой толстостенную трубку, плотно закрытую резиновой пробкой, в которую вставлены медные проволочки. С наружной стороны трубки нанесены деления на равном расстоянии друг от друга. Эвдиометр заполняют прокипяченной водой, опускают открытым концом в чашку с водой так, чтобы из него не выливалась вода, и укрепляют в лапке штатива. В эвдиометр вводят столько кислорода, чтобы он заполнил трубку до второго деления (два объема), а следующие два объема заполняют водородом. Свободные концы медных проволочек эвдиометра соединяют проводами с индукционной катушкой, а последнюю с источником электрического тока. При включении тока между медными проволочками внутри трубки проскакивает электрическая искра, от которой происходит взрыв смеси водорода с кислородом. Вода в эвдиометре поднимается ровно на три деления. Чтобы узнать, какой газ остался в эвдиометре после взрыва, открытый конец трубки закрывают пробкой, эвдиометр из лапки штатива освобождают и перевертывают. Пробку вынимают и в открытый конец трубки быстро вносят тлеющую лучинку, она вспыхивает. Следовательно, в эвдиометре после взрыва остался один объем кислорода. Значит, во время взрыва израсходовались на образование воды два объема водорода и один объем кислорода.
Слайд 5Физические свойства воды
Цвет подземных вод зависит от их химического состава и механических примесей.
Физические свойства воды
Цвет подземных вод зависит от их химического состава и механических примесей.

Обычно подземные воды бесцветны. Желтоватый цвет характерен для вод болотного происхождения, содержащих гуминовые вещества. Сероводородные воды вследствие окисления H2S и образования тонкой коллоидной мути, состоящей из частиц серы, имеют изумрудный оттенок. Цвет воды оценивается по стандартной платино-кобальтовой шкале в градусах.
Запах в подземных водах обычно отсутствует. Ощущение запаха свидетельствует или о наличии газов биохимического происхождения (сероводород и др.), или о присутствии гниющих органических веществ. Характер запаха выражают описательно: без запаха, сероводородный, болотный, гнилостный, плесневелый и т.д. Интенсивность запаха оценивают по шкале в баллах.
Вкус воды зависит от состава растворенных веществ. Соленый вкус вызывается хлористым натрием, горький - сульфатом магния, ржавый - солями железа. Сладковатый вкус имеют воды, богатые органическими веществами, наличие свободной углекислоты придает приятный освежающий вкус. Вкус воды оценивается по таблицам в баллах.
Прозрачность подземных вод зависит от количества растворенных в них минеральных веществ, содержания механических примесей, органических веществ и коллоидов. Для указания степени прозрачности подземных вод служит следующая номенклатура: прозрачная, слабопалесцирующая, опалесцирующая, слегка мутная, мутная, сильно мутная. Подземные воды обычно бывают прозрачными. Мутность воды оценивается в мг\л по стандартной шкале.
Плотность воды определяется отношением её массы к объему при определенной температуре. За единицу плотности воды принята плотность дистиллированной воды при температуре 4°С. Плотность воды зависит от температуры, количества растворенных в ней солей, газов и взвешенных частиц и изменяется от 1 до 1,4 г/см3.
Сжимаемость воды незначительна и характеризуется коэффициентом сжимаемости β = (2,7-5)10-5 Па. Вязкость воды характеризует внутреннее сопротивление частиц жидкости её движению, количественно она выражается коэффициентами динамической и кинематической вязкости.
Запах в подземных водах обычно отсутствует. Ощущение запаха свидетельствует или о наличии газов биохимического происхождения (сероводород и др.), или о присутствии гниющих органических веществ. Характер запаха выражают описательно: без запаха, сероводородный, болотный, гнилостный, плесневелый и т.д. Интенсивность запаха оценивают по шкале в баллах.
Вкус воды зависит от состава растворенных веществ. Соленый вкус вызывается хлористым натрием, горький - сульфатом магния, ржавый - солями железа. Сладковатый вкус имеют воды, богатые органическими веществами, наличие свободной углекислоты придает приятный освежающий вкус. Вкус воды оценивается по таблицам в баллах.
Прозрачность подземных вод зависит от количества растворенных в них минеральных веществ, содержания механических примесей, органических веществ и коллоидов. Для указания степени прозрачности подземных вод служит следующая номенклатура: прозрачная, слабопалесцирующая, опалесцирующая, слегка мутная, мутная, сильно мутная. Подземные воды обычно бывают прозрачными. Мутность воды оценивается в мг\л по стандартной шкале.
Плотность воды определяется отношением её массы к объему при определенной температуре. За единицу плотности воды принята плотность дистиллированной воды при температуре 4°С. Плотность воды зависит от температуры, количества растворенных в ней солей, газов и взвешенных частиц и изменяется от 1 до 1,4 г/см3.
Сжимаемость воды незначительна и характеризуется коэффициентом сжимаемости β = (2,7-5)10-5 Па. Вязкость воды характеризует внутреннее сопротивление частиц жидкости её движению, количественно она выражается коэффициентами динамической и кинематической вязкости.
Слайд 6Электропроводность подземных вод зависит от количества растворенных в них солей. Пресные воды обладают
Электропроводность подземных вод зависит от количества растворенных в них солей. Пресные воды обладают

незначительной электропроводностью. Дистиллированная вода является изолятором. Электропроводность воды оценивают по удельному электрическому сопротивлению, которое выражается в Ом.м и изменяется от 0,02 до 1,0 Ом.м.
Радиоактивность воды определяется содержанием в ней радона, эманации радия. За редким исключением подземные воды в той или иной степени радиоактивны.
Температура подземных вод изменяется в очень широких пределах и зависит от геотермических особенностей района. Она отражает возрастные, тектонические, литологические и гидродинамические особенности водовмещающих толщ. Температура вод влияет на их химический состав, на вязкость и на коэффициент фильтрации. В естественных условиях подземные воды могут быть переохлажденными (ниже 0°С, распространены в районах многолетних не мерзлых пород), холодными (ниже 20°С, приурочены к верхней зоне земной коры до пояса постоянных годовых температур в средних широтах), термальными (20-100°С, вскрываются буровыми скважинами на различных глубинах) и перегретыми (100-375°С встречаются в районах современной вулканической деятельности).
Радиоактивность воды определяется содержанием в ней радона, эманации радия. За редким исключением подземные воды в той или иной степени радиоактивны.
Температура подземных вод изменяется в очень широких пределах и зависит от геотермических особенностей района. Она отражает возрастные, тектонические, литологические и гидродинамические особенности водовмещающих толщ. Температура вод влияет на их химический состав, на вязкость и на коэффициент фильтрации. В естественных условиях подземные воды могут быть переохлажденными (ниже 0°С, распространены в районах многолетних не мерзлых пород), холодными (ниже 20°С, приурочены к верхней зоне земной коры до пояса постоянных годовых температур в средних широтах), термальными (20-100°С, вскрываются буровыми скважинами на различных глубинах) и перегретыми (100-375°С встречаются в районах современной вулканической деятельности).
Слайд 7Химические свойства воды
Взаимодействие с простыми веществами
При комнатной температуре вода реагирует с активными металлами с
Химические свойства воды
Взаимодействие с простыми веществами
При комнатной температуре вода реагирует с активными металлами с

образованием щелочей и водорода:
При нагревании вода вступает в реакции с менее активными металлами, расположенными в ряду активности до водорода. При этом образуются оксиды и водород:
Вода может реагировать с некоторыми неметаллами. Так, вода загорается в атмосфере фтора:
При высокой температуре происходит её взаимодействие с углём:
При нагревании вода вступает в реакции с менее активными металлами, расположенными в ряду активности до водорода. При этом образуются оксиды и водород:
Вода может реагировать с некоторыми неметаллами. Так, вода загорается в атмосфере фтора:
При высокой температуре происходит её взаимодействие с углём:
Слайд 8Взаимодействие со сложными веществами
Вода реагирует с оксидами активных металлов с образованием щелочей:
Вода реагирует с кислотными
Взаимодействие со сложными веществами
Вода реагирует с оксидами активных металлов с образованием щелочей:
Вода реагирует с кислотными

оксидами (кроме оксида кремния). При этом образуются кислоты:
Некоторые неорганические и многие органические вещества подвергаются гидролизу (разложению водой).
Необратимый гидролиз характерен для солей, образованных слабым основанием и слабой кислотой:
Гидролиз белков, жиров и углеводов происходит в органах пищеварения животных и является неотъемлемой частью обмена веществ в живых организмах.
Вода может присоединяться к некоторым веществам. Такой процесс называется гидратацией.
В результате гидратации многих солей образуются их кристаллогидраты:
Одна из важнейших реакций с участием воды — фотосинтез:
Разложение воды (электролиз)
Некоторые неорганические и многие органические вещества подвергаются гидролизу (разложению водой).
Необратимый гидролиз характерен для солей, образованных слабым основанием и слабой кислотой:
Гидролиз белков, жиров и углеводов происходит в органах пищеварения животных и является неотъемлемой частью обмена веществ в живых организмах.
Вода может присоединяться к некоторым веществам. Такой процесс называется гидратацией.
В результате гидратации многих солей образуются их кристаллогидраты:
Одна из важнейших реакций с участием воды — фотосинтез:
Разложение воды (электролиз)
- Предыдущая
Волшебная страна - ГеометрияСледующая -
Отчет по педагогической практике Ароматические углеводороды. Бензол Презентация выполнена учителем химии лицея №1 пос. Львовский Подольского района Воробьёвой
Ароматические углеводороды. Бензол Презентация выполнена учителем химии лицея №1 пос. Львовский Подольского района Воробьёвой Презентация по Химии "Углекислый газ"
Презентация по Химии "Углекислый газ"  Щелочные металлы
Щелочные металлы Reactivi444
Reactivi444 Химическая связь
Химическая связь Основания
Основания Висмут
Висмут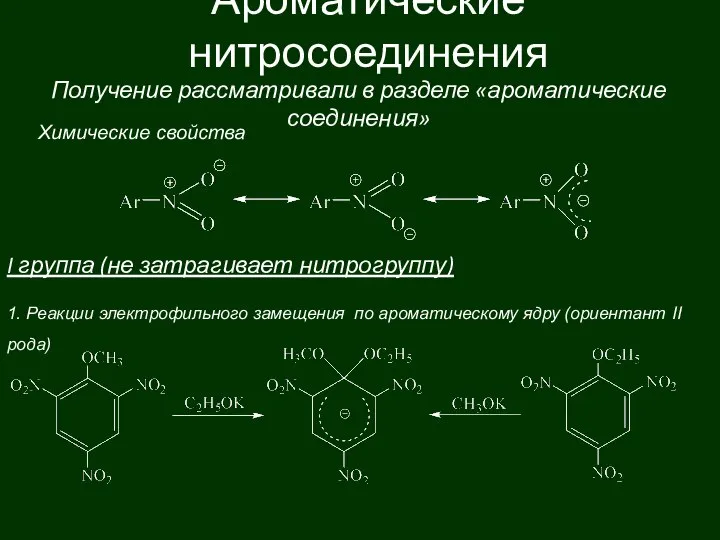 Ароматические нитросоединения
Ароматические нитросоединения Олимпиада Ломоносов
Олимпиада Ломоносов Физическая химия, термодинамика
Физическая химия, термодинамика Алмазы
Алмазы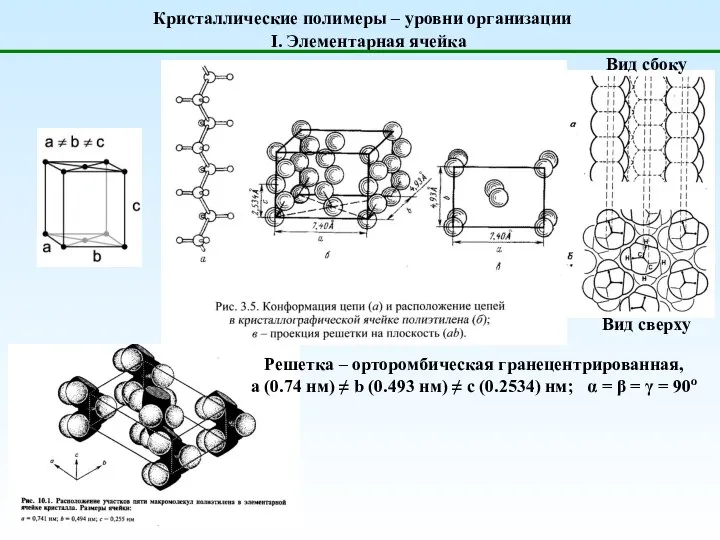 Структура-полимеров
Структура-полимеров Химические свойства кислорода. Применение кислорода
Химические свойства кислорода. Применение кислорода h-m-chniy-zv-yazok-budova-rechovin
h-m-chniy-zv-yazok-budova-rechovin Структура електронної оболонки атома. Енергетичні рівні та підрівні
Структура електронної оболонки атома. Енергетичні рівні та підрівні Химическая связь
Химическая связь Кислоты. Свойства кислот
Кислоты. Свойства кислот Увлекательный мир науки и практики
Увлекательный мир науки и практики Потенциометрические анализаторы Поверка рН - метра
Потенциометрические анализаторы Поверка рН - метра Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов
Периодическая система химических элементов Д.И. Менделеева. Знаки химических элементов Соли как производные кислот и оснований. Цель урока: 1.Дать определение солей. 2. Рассмотреть состав и название солей. 3. Продолжить
Соли как производные кислот и оснований. Цель урока: 1.Дать определение солей. 2. Рассмотреть состав и название солей. 3. Продолжить Металлы
Металлы Кислоты
Кислоты Сульфиты. Виды сульфидов
Сульфиты. Виды сульфидов Які існують способи розділення сумішей?
Які існують способи розділення сумішей? 10 класс урок № 2 ТХС
10 класс урок № 2 ТХС Электронное и пространственное строение алкенов. Гомология и изомерия алкенов
Электронное и пространственное строение алкенов. Гомология и изомерия алкенов Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева
Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева