Содержание
- 2. Биологические функции белков
- 3. Структурная (строительная, пластическая) функция Эта функция заключается в том, белки являются универсальным строительным материалом, из которого
- 4. Каталитическая функция В организме имеются особые белки, являющиеся катализаторами химических реакций. Такие белки получили название ферменты
- 5. Сократительная функция В основе всех форм движения и в первую очередь мышечного сокращения и расслабления лежит
- 6. Регуляторная функция Белки обладают амфотерностью и могут взаимодействовать как с кислотами, так и с основаниями. Поэтому
- 7. Транспортная функция Белковые молекулы имеют большой размер, хорошо растворимы в воде и, перемещаясь по водным пространствам
- 8. Защитная функция Белки выполняют защитную функцию, участвуя в обеспечении иммунитета. К защитной функции относится участие белков
- 9. Энергетическая функция Окисление белков, как и всех других органических соединений, сопровождается выделением энергии. При окислении 1
- 10. Исходя из важнейшей биологической роли белков в организме, их еще называют протеинами (от греч. рroteus –
- 11. Строение белков Белки - высокомолекулярные азотсодержащие соединения, состоящие из аминокислот. В одну молекулу белков входят десятки,
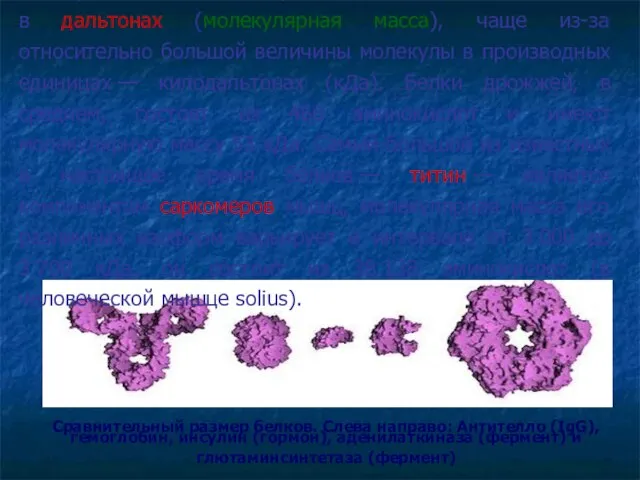
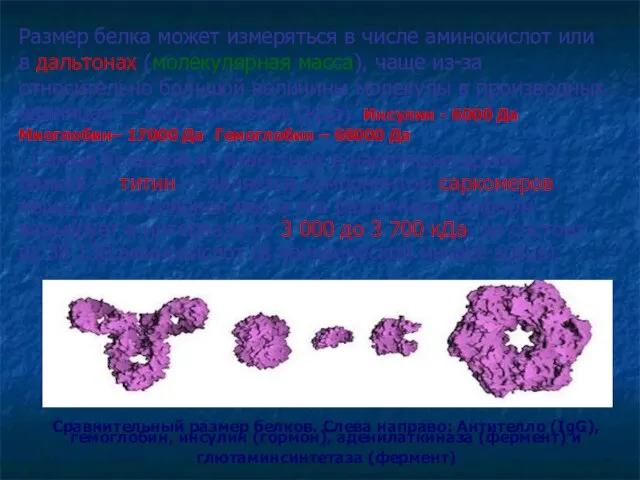
- 12. Сравнительный размер белков. Слева направо: Антителло (IgG), гемоглобин, инсулин (гормон), аденилаткиназа (фермент) и глютаминсинтетаза (фермент) Размер
- 13. Общая формула аминокислот R H-C-NH2 COOH
- 14. Классификация аминокислот Аминокислоты ациклические циклические (15) (5)
- 15. Классификация ациклических аминокислот Ациклические аминокислоты моноаминомонокарбоновые моноаминодикарбоновые диаминомонокарбоновые
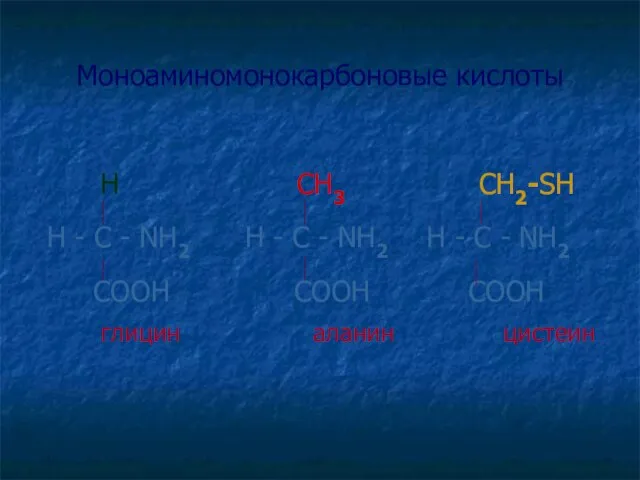
- 16. Моноаминомонокарбоновые кислоты H СН3 СН2-SH H - C - NH2 H - C - NH2 H
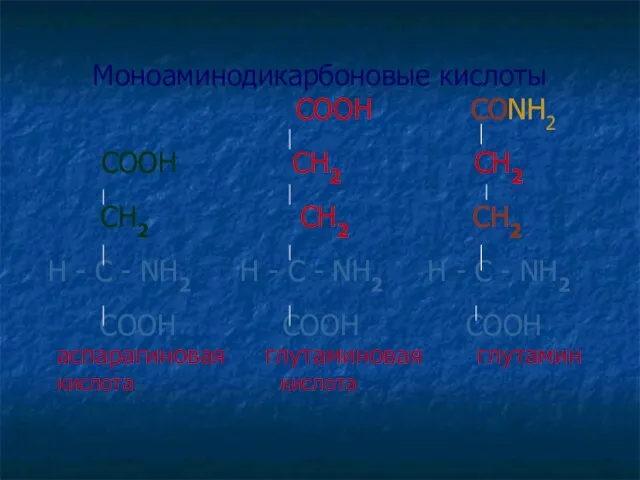
- 17. Моноаминодикарбоновые кислоты СООН СОNH2 СООН СН2 СН2 СH2 СН2 СН2 H - C - NH2 H
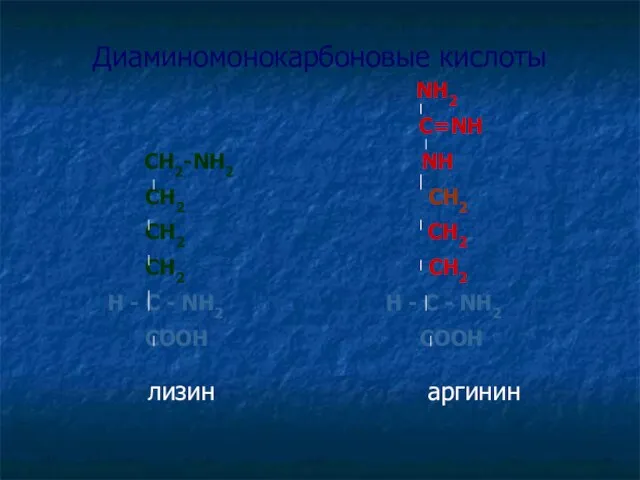
- 18. Диаминомонокарбоновые кислоты NH2 C=NH СН2-NH2 NH СH2 СH2 СН2 СН2 СH2 СН2 H - C -
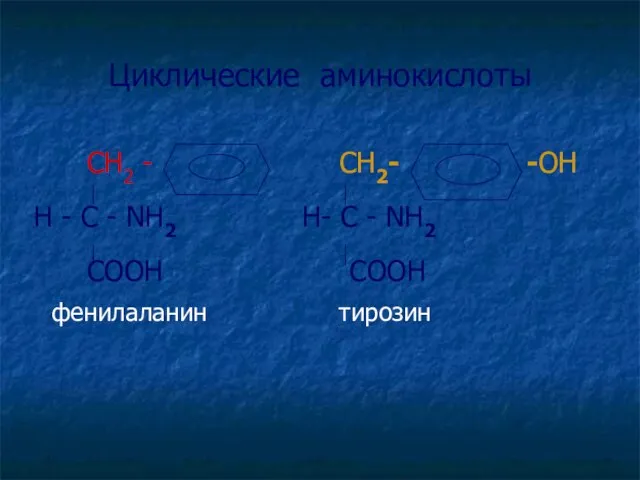
- 19. Циклические аминокислоты СН2 - СН2- -ОН H - C - NH2 Н- C - NH2 COOH
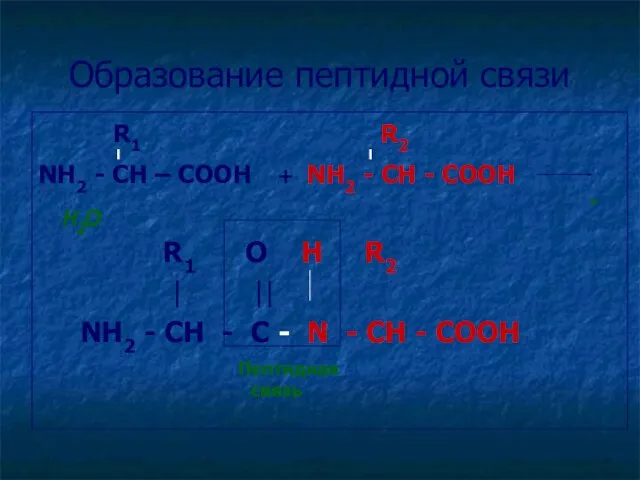
- 20. Образование пептидной связи R1 R2 NH2 - CH – COOH + NH2 - CH - COOH
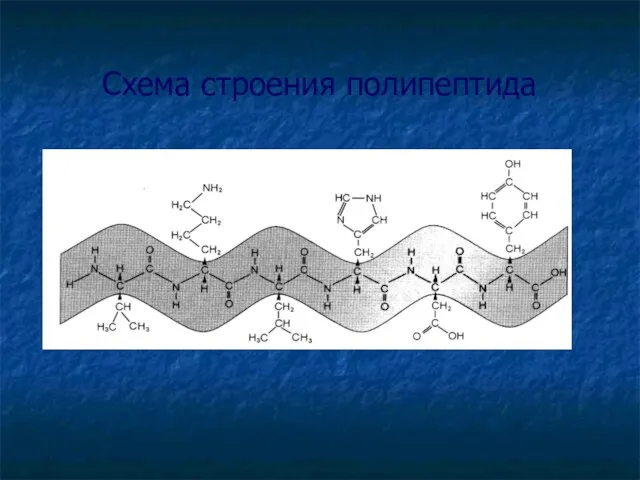
- 21. Схема строения полипептида
- 22. Полипептидная цепь белка трипсина
- 23. Участок молекулы коллагена
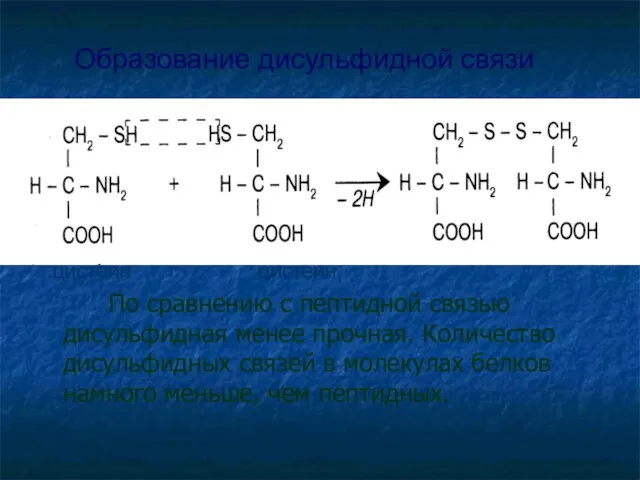
- 24. цистеин цистеин По сравнению с пептидной связью дисульфидная менее прочная. Количество дисульфидных связей в молекулах белков
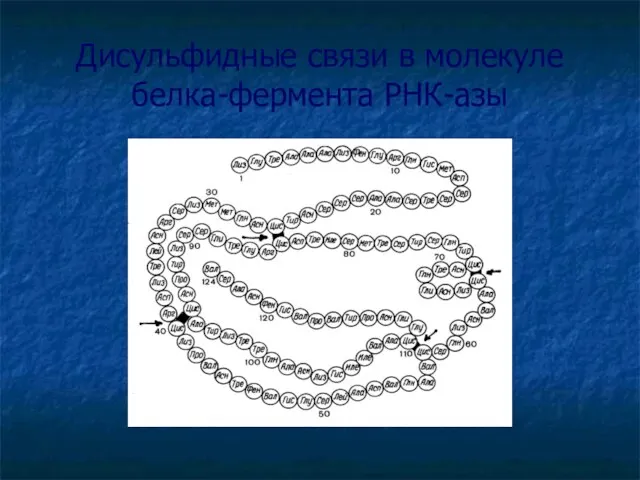
- 25. Дисульфидные связи в молекуле белка-фермента РНК-азы
- 26. Дисульфидные связи в молекуле инсулина
- 27. Классификация белков (по химическому составу) Простые белки Сложные белки (протеины) (протеиды) 1. Альбумины 1. Фосфопротеиды 2.
- 28. Тест 1 Содержание белков в организме взрослого человека составляет: а) 8-10 % б) 15-17 % в)
- 29. Тест 2 Обязательным химическим элементом, входящим в состав белков, является: а) азот б) кальций в) селен
- 30. Тест 3 Во все белки входят: а) 10 разновидностей аминокислот б) 20 разновидностей аминокислот в) 30
- 31. Тест 4 В состав аминокислот обязательно входят функциональные группы: а) альдегидная и спиртовая б) карбоксильная и
- 32. Тест 5 Главной химической связью в белках является: а) водородная б) дисульфидная в) ионная г) пептидная
- 33. Тест 6 Простые белки отличаются от сложных: а) молекулярной массой б) отсутствием дисульфидных связей в) отсутствием
- 34. Тест 7 Сложные белки отличаются от простых: а) изоэлектрической точкой б) наличием дисульфидных связей в) наличием
- 35. Тест 8 В образовании дисульфидной связи участвует аминокислота: а) аланин б) глицин в) глутамин г) цистеин
- 36. Тест 9 Формулу СН2-NH2 COOH имеет аминокислота: а) аланин б) глицин в) глутамин г) цистеин
- 37. Тест 10 Формулу СООН СН2 СН2-NH2 COOH имеет аминокислота: а) аспарагиновая кислота б) глутамин в) глутаминовая
- 38. ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА БЕЛКОВ
- 39. Сравнительный размер белков. Слева направо: Антителло (IgG), гемоглобин, инсулин (гормон), аденилаткиназа (фермент) и глютаминсинтетаза (фермент) Размер
- 40. Пространственная форма белковых молекул В молекуле белка условно выделяют четыре уровня её пространственной организации: Первичная структура
- 41. Первичная структура Первичная структура представляет собой последовательность расположения аминокислот в полипептидных цепях. Фиксируется первичная структура прочными
- 42. Первичная структура белка трипсина
- 43. Вторичная структура Вторичная структура характеризует пространственную форму полипептидных цепей. Часто полипептидные цепи в белковых молекулах закручиваются
- 44. Полипептидная цепь в форме α-спирали
- 45. Третичная структура Третичная структура отражает пространственную форму вторичной структуры. Например, вторичная структура в форме спирали может
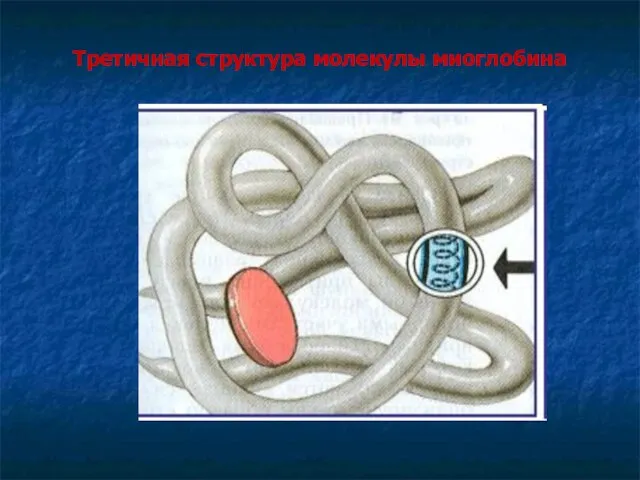
- 46. Третичная структура молекулы миоглобина
- 47. Конформация белка Пространственная форма всей белковой молекулы, являющаяся совокупностью первичной, вторичной и третичной структур обозначается термином
- 48. Четвертичная структура Четвертичной структурой обладают только некоторые белки. Четвертичная структура – сложное надмолекулярное образование, состоящее из
- 49. Объединение субъединиц в четвертичную структуру приводит к возникновению нового биологического свойства, отсутствующего у отдельных субъединиц. Образование
- 50. Схема строения белковой молекулы, обладающей четвертичной структурой
- 51. Из всех структур белковой молекулы кодируется только первичная. За счет информации, заключенной в молекуле ДНК, синтезируются
- 52. Кристаллы различных белков, выращенные на космической станции «Мир»Кристаллы различных белков, выращенные на космической станции «Мир» и
- 53. Классификация белков (по форме молекул) Глобулярные Фибриллярные 1. Альбумины 1. Коллаген 2. Глобулины 2. Кератины 3.
- 54. Амфотерность белков Амфотерность белков (наличие как кислотных, так и оснóвных свойств) обусловлена присутствием в их молекулах
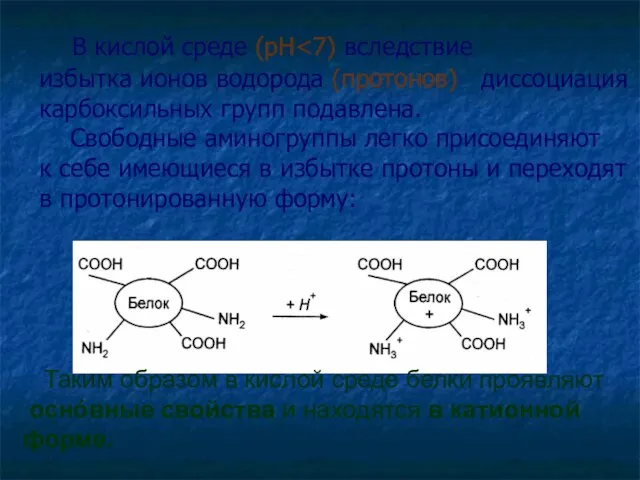
- 55. В кислой среде (рН Таким образом в кислой среде белки проявляют оснóвные свойства и находятся в
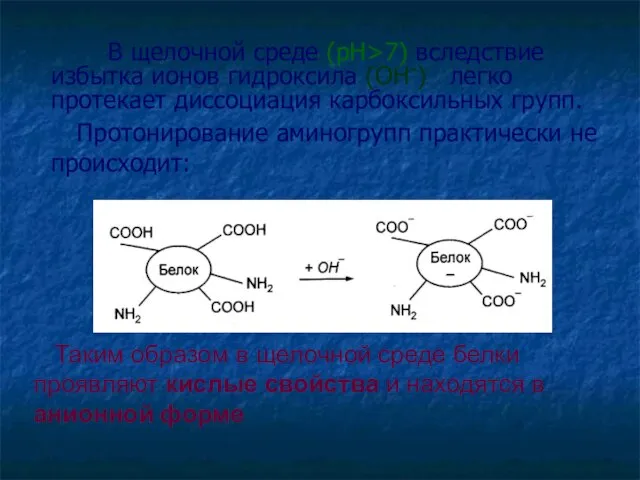
- 56. В щелочной среде (рН>7) вследствие избытка ионов гидроксила (ОН-) легко протекает диссоциация карбоксильных групп. Протонирование аминогрупп
- 57. Изоэлектрическое состояние При определенной кислотности в молекуле белка может быть одинаковое количество диссоциированных карбоксильных групп (–СОО-)
- 58. Значение рН, при котором молекулы белка нейтральны, называется изоэлектрической точкой и обозначается рI или рНиэт Для
- 59. Растворимость белков Не смотря на большой размер молекул (1–100 нм), белки хорошо растворяются в воде, и
- 60. Наличие заряда Только при одном строго определенном значении рН, равном изоэлектрической точке, белок нейтрален. При всех
- 61. Наличие гидратной оболочки У нативного белка гидрофобные группы (не взаимодействующие с водой) обычно находятся внутри молекулы,
- 62. Гидратная оболочка белковой молекулы
- 63. Высаливание белков Высаливание белков - выпадение белка в осадок под воздействием водоотнимающих средств, к которым в
- 64. В результате бóльшая часть воды связывается с ионами солей, что приводит к значительному уменьшению гидратных оболочек
- 65. Процесс высаливания не затрагивает структуру белковых молекул, поэтому в осадок выпадает белок, сохраняющий свою нативность, т.е.
- 66. Денатурация белков Денатурация – потеря белком нативных свойств. Денатурация обычно сопровождается выпадением белка в осадок. Факторы,
- 67. Физические факторы денатурации Нагревание (выше 50-60°С); различные виды излучения (ультрафиолетовое и ионизирующее излучение); ультразвук; вибрация.
- 68. Химические факторы денатурации Сильные кислоты; Сильные щелочи; Соли тяжелых металлов; Некоторые органические кислоты (трихлоруксусная, сульфосалициловая)
- 69. Механизм денатурации Под влиянием факторов денатурации в молекулах белков разрываются различные непептидные связи, что вызывает разрушению
- 70. Схема денатурации белка
- 71. Обратимость денатурации белка При кратковременном действии денатурирующих факторов конформационные изменения незначительны, поэтому возможен переход белка снова
- 72. Ренатурация белка а - денатурация б - ренатурация
- 73. Продолжительное воздействие факторов денатурации вызывает глубокое необратимое изменение трехмерной структуры белковых молекул, что делает ренатурацию невозможной.
- 74. Тест 1 Первичная структура белковой молекулы фиксируется: а) водородными связями б) дисульфидными связями в) ионными связями
- 75. Тест 2 Простые белки отличаются от сложных: а) молекулярной массой б) отсутствием дисульфидных связей в) отсутствием
- 76. Тест 3 При высаливании белок: а) подвергается гидролизу б) приобретает заряд в) теряет гидратную оболочку г)
- 77. Тест 4 При денатурации у белков в первую очередь изменяется структура: а) первичная б) вторичная в)
- 78. Тест 5 В кислой среде молекулы белков: а) имеют отрицательный заряд б) имеют положительный заряд в)
- 79. Тест 6 В щелочной среде молекулы белков: а) имеют отрицательный заряд б) имеют положительный заряд в)
- 80. Тест 7 При значении рН, равном изоэлектрической точке, молекулы белков: а) имеют отрицательный заряд б) имеют
- 81. Тест 8 Молекулы белков всегда нейтральны: а) в кислой среде б) в нейтральной среде в) в
- 82. Тест 9 Cложные белки отличаются от простых: а) изоэлектрической точкой б) наличием дисульфидных связей в) наличием
- 83. Тест 10 В молекуле ДНК содержится информация о: а) первичной структуре белка б) вторичной структуре белка
- 85. Скачать презентацию





































































 Нобелевские лауреаты и их достижения
Нобелевские лауреаты и их достижения Алканы. Строение,номенклатура, изомерия
Алканы. Строение,номенклатура, изомерия Органическая химия
Органическая химия Презентация на тему Увлекательные факты из жизни Менделеева
Презентация на тему Увлекательные факты из жизни Менделеева  Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Растворы электролитов
Растворы электролитов Пятичленные гетероциклы с двумя и более атомами азота
Пятичленные гетероциклы с двумя и более атомами азота Гидролиз солей
Гидролиз солей Скорость химических реакций
Скорость химических реакций Веселый химический КВН
Веселый химический КВН Понятие об ароматических спиртах и фенолах. Особенности строения фенола
Понятие об ароматических спиртах и фенолах. Особенности строения фенола Химическая коррозия
Химическая коррозия Строение атома
Строение атома Проблемы и меры по защите окружающей среды ПМР
Проблемы и меры по защите окружающей среды ПМР Алкены. Гомологический ряд алкенов. Изомерия алкенов
Алкены. Гомологический ряд алкенов. Изомерия алкенов Современные способы защиты ОТТ
Современные способы защиты ОТТ Закон сохранения массы веществ. 8 класс
Закон сохранения массы веществ. 8 класс Криогенный разрыв пласта
Криогенный разрыв пласта Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини
Виготовлення водних розчинів з заданою масовою часткою розчиненої речовини Применение неметаллов
Применение неметаллов Растворение
Растворение алотропні модифікації неметалів
алотропні модифікації неметалів Закон Авогадро. Молярный объём газов
Закон Авогадро. Молярный объём газов Разбор заданий на амины
Разбор заданий на амины Интеллектуальный турнир для старшеклассников Умножая таланты 2020
Интеллектуальный турнир для старшеклассников Умножая таланты 2020 Презентация на тему Теория электролитической диссоциации обобщающий урок
Презентация на тему Теория электролитической диссоциации обобщающий урок  Теория химического строения органических веществ А.М. Бутлерова
Теория химического строения органических веществ А.М. Бутлерова Сода: мифы и реальность
Сода: мифы и реальность