Содержание
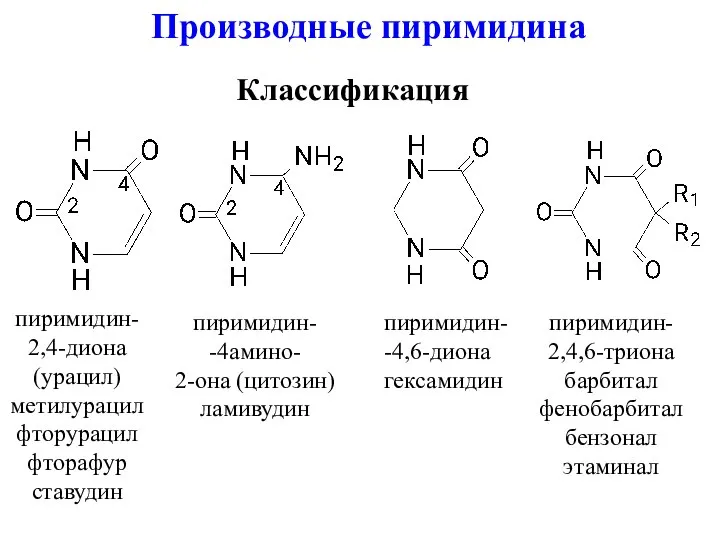
- 2. Классификация пиримидин- 2,4-диона (урацил) метилурацил фторурацил фторафур ставудин пиримидин- -4амино- 2-она (цитозин) ламивудин пиримидин- -4,6-диона гексамидин
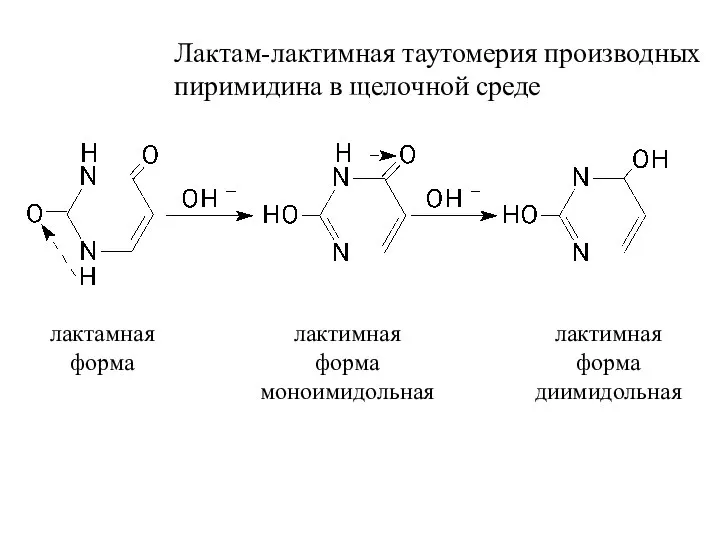
- 3. Лактам-лактимная таутомерия производных пиримидина в щелочной среде лактамная форма лактимная форма моноимидольная лактимная форма диимидольная
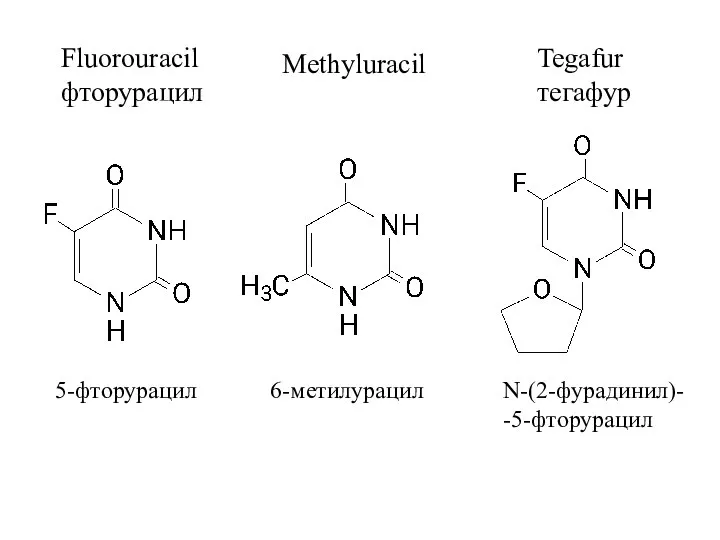
- 4. Fluorouracil фторурацил 5-фторурацил Methyluracil 6-метилурацил Tegafur тегафур N-(2-фурадинил)- -5-фторурацил
- 5. Zidovudine азидотимидин 1(3-азидо-2-дезокси- рибозил)тимидин Stavudine 3-дезокситимидин Lamivudine [1-(2-оксиметил)- 1,3-оксатиолан-5-ил] цитозин
- 6. Получение – ЛВ данной группы получают синтетически. Физико-химические свойства. Белые (иногда с желтоватым или бледно-розовым оттенком)
- 7. В химическом отношении ЛВ данной группы вступают в реакции комплексообразования с солями тяжелых металлов с образованием
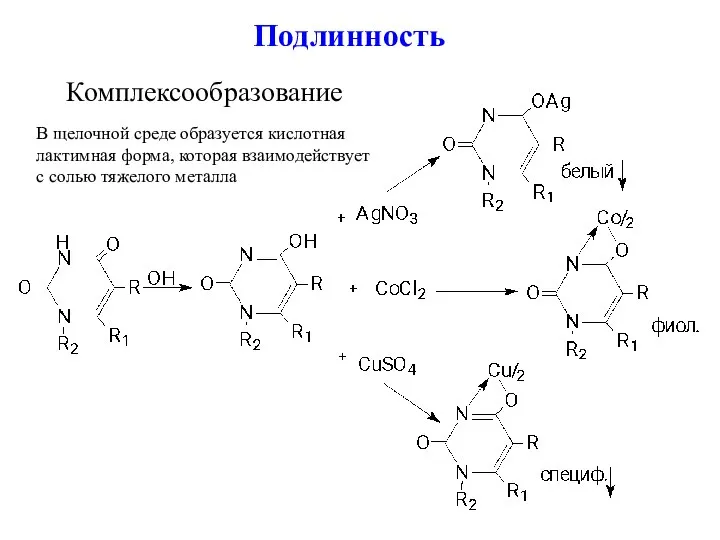
- 8. Подлинность Комплексообразование В щелочной среде образуется кислотная лактимная форма, которая взаимодействует с солью тяжелого металла
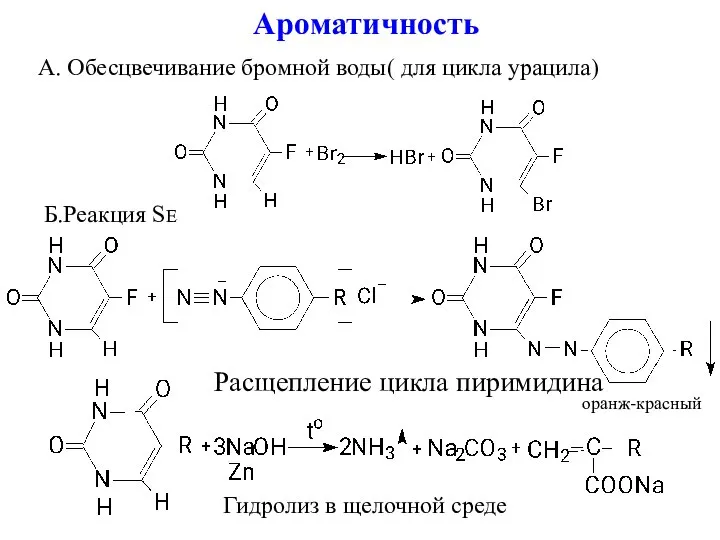
- 9. Ароматичность А. Обесцвечивание бромной воды( для цикла урацила) Б.Реакция SE оранж-красный Расщепление цикла пиримидина Гидролиз в
- 10. Фторид-ионы во фторурациле и тегафуре обнаруживают после дегалогенирования металлическим натрием. 2F- + CaCI2 = CaF2 +2CI-
- 11. Определение примесей. Степень чистоты ЛП данной группы определяют методом ТСХ (отсутствие промежуточных продуктов синтеза и посторонних
- 12. Методы количественного определения. 1. Кислотно-основное титрование в водной среде – косвенный вариант после реакции взаимодействия с
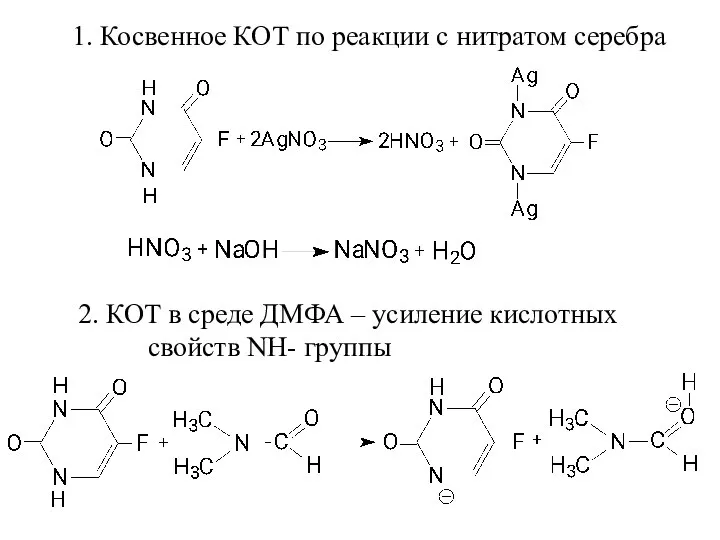
- 13. 1. Косвенное КОТ по реакции с нитратом серебра 2. КОТ в среде ДМФА – усиление кислотных
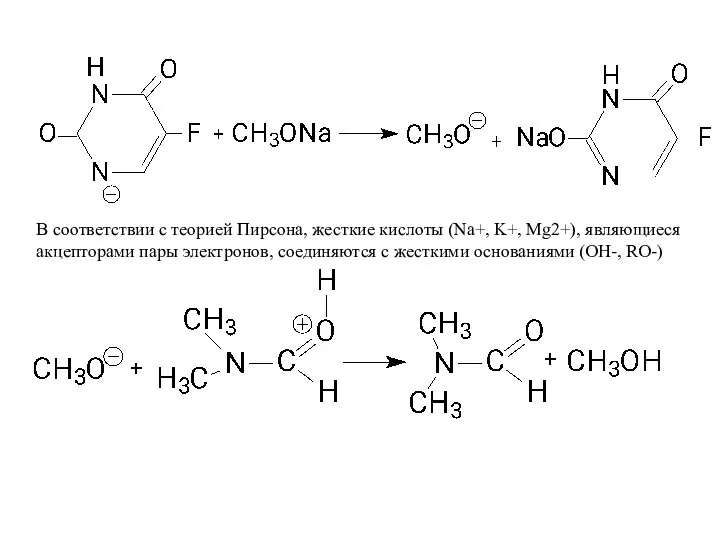
- 14. В соответствии с теорией Пирсона, жесткие кислоты (Na+, K+, Mg2+), являющиеся акцепторами пары электронов, соединяются с
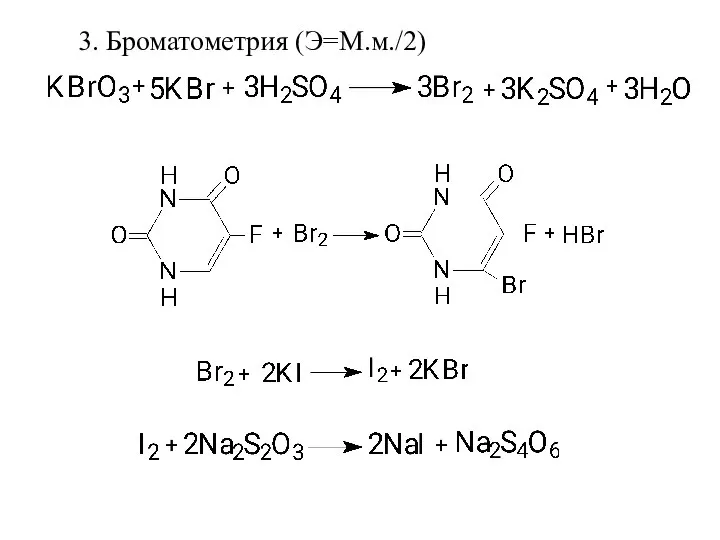
- 15. 3. Броматометрия (Э=М.м./2)
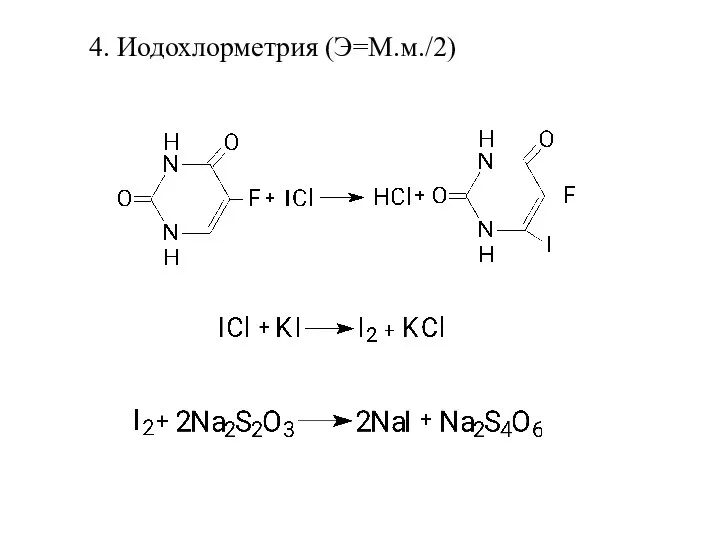
- 16. 4. Иодохлорметрия (Э=М.м./2)
- 17. Применение. Список А. Фторурацил и тегафур- противоопухолевые средства. Список Б. Азидотимидин, ставудин, ламивудин – в терапии
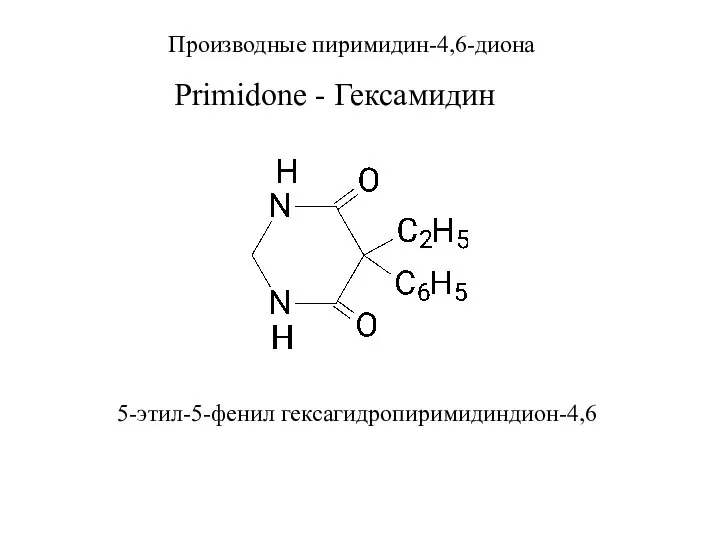
- 18. Primidone - Гексамидин 5-этил-5-фенил гексагидропиримидиндион-4,6 Производные пиримидин-4,6-диона
- 19. Примидон получают синтетически. Примидон – представляет собой белый кристаллический порошок без запаха. Нерастворим в воде, мало
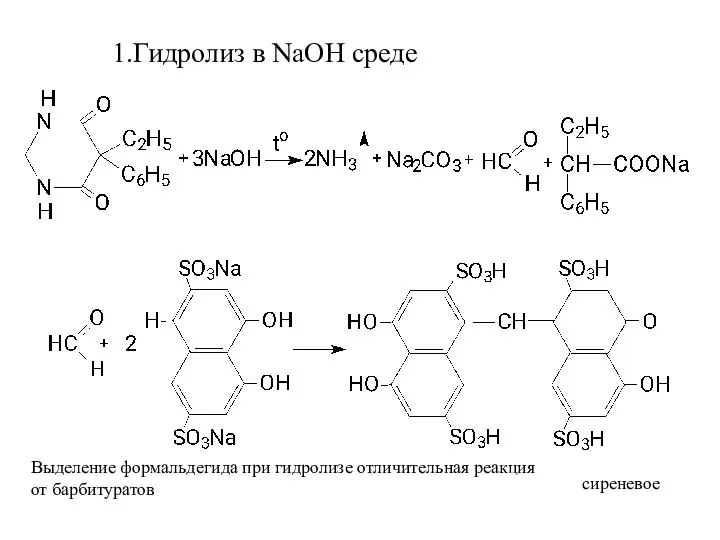
- 20. 1.Гидролиз в NaOH среде сиреневое Выделение формальдегида при гидролизе отличительная реакция от барбитуратов
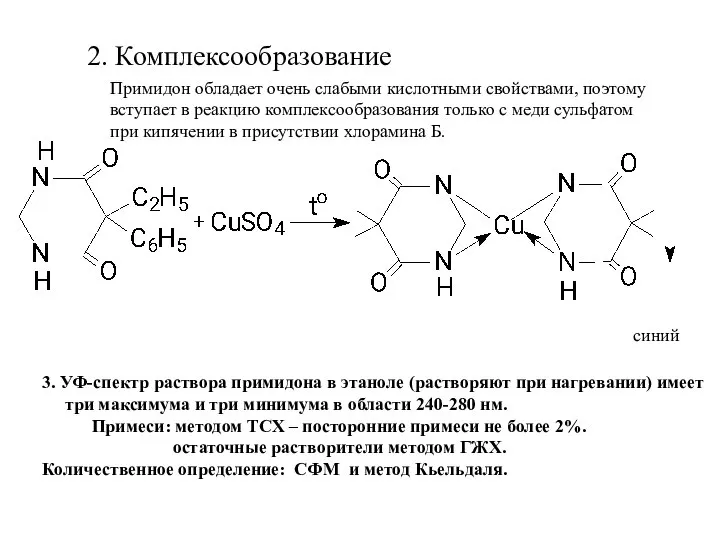
- 21. 2. Комплексообразование синий 3. УФ-спектр раствора примидона в этаноле (растворяют при нагревании) имеет три максимума и
- 22. Применение. Примидон обладает противосудорожным действием. Снотворное действие отсутствует. Хранение. Список Б. В хорошо укупоренной таре, в
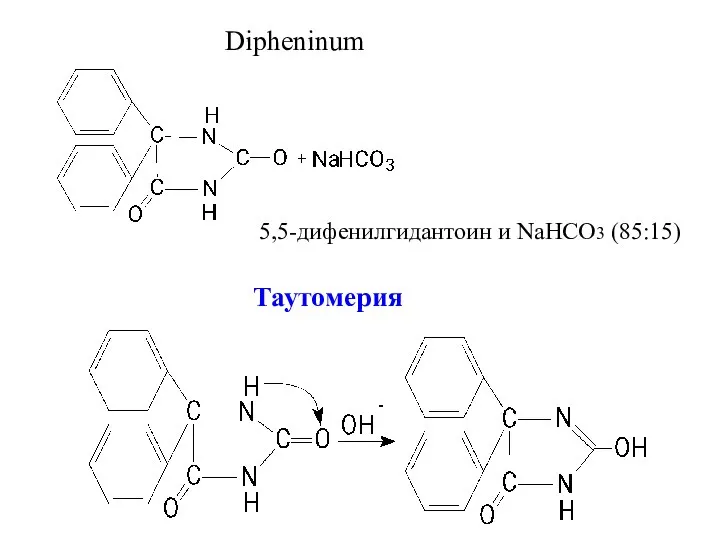
- 23. Dipheninum 5,5-дифенилгидантоин и NaHCO3 (85:15) Таутомерия
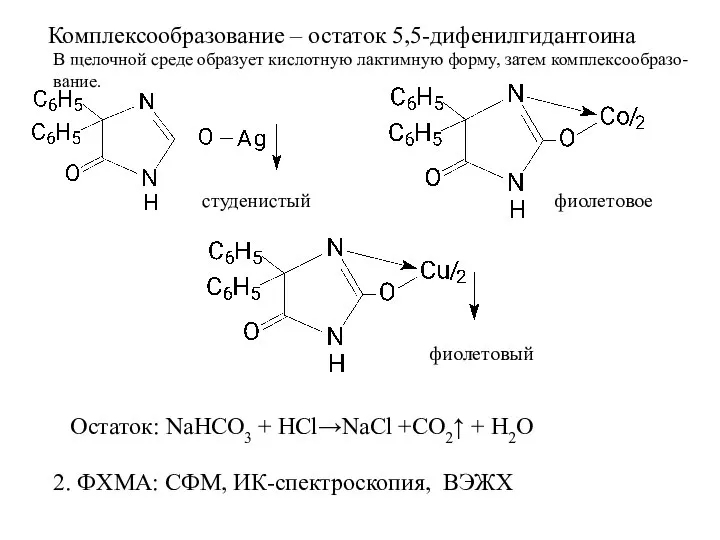
- 24. Комплексообразование – остаток 5,5-дифенилгидантоина фиолетовый студенистый фиолетовое Остаток: NaHCO3 + HCl→NaCl +CO2↑ + H2O 2. ФХМА:
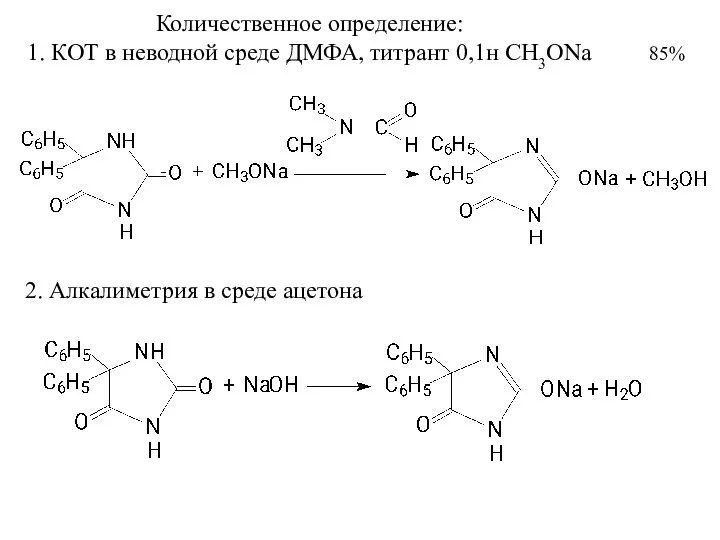
- 25. Количественное определение: 1. КОТ в неводной среде ДМФА, титрант 0,1н СH3ONa 2. Алкалиметрия в среде ацетона
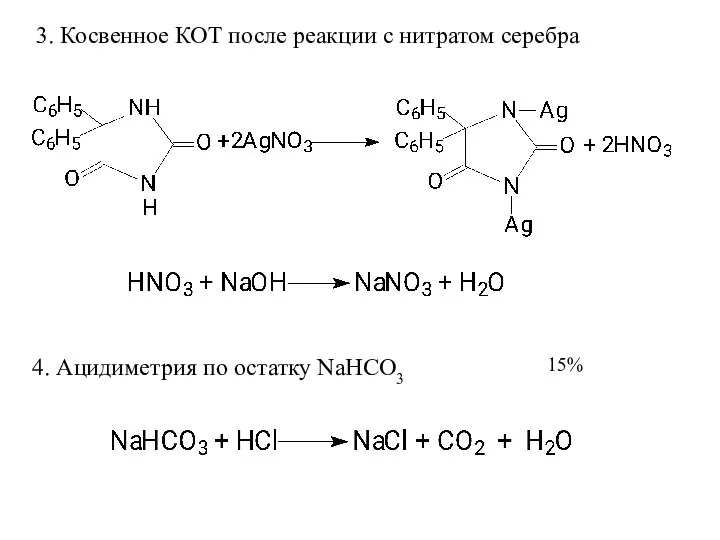
- 26. 3. Косвенное КОТ после реакции с нитратом серебра 4. Ацидиметрия по остатку NaHCO3 15%
- 28. Скачать презентацию
![Zidovudine азидотимидин 1(3-азидо-2-дезокси- рибозил)тимидин Stavudine 3-дезокситимидин Lamivudine [1-(2-оксиметил)- 1,3-оксатиолан-5-ил] цитозин](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1040081/slide-4.jpg)








 Получение формальдегида методом дегидрирования метанола
Получение формальдегида методом дегидрирования метанола Презентация на тему Простые вещества - неметаллы
Презентация на тему Простые вещества - неметаллы  Органическая химия. Подготовка к экзамену
Органическая химия. Подготовка к экзамену Потенциометрические анализаторы Поверка рН - метра
Потенциометрические анализаторы Поверка рН - метра Химия нефти и газа
Химия нефти и газа 2.Химич. м-ды колич. ан-за
2.Химич. м-ды колич. ан-за 20140111_mineraly
20140111_mineraly Алкадиены
Алкадиены Массовая доля химич элемента
Массовая доля химич элемента Типы химических реакций. Решение примеров
Типы химических реакций. Решение примеров Валентность
Валентность Nevarne snovi
Nevarne snovi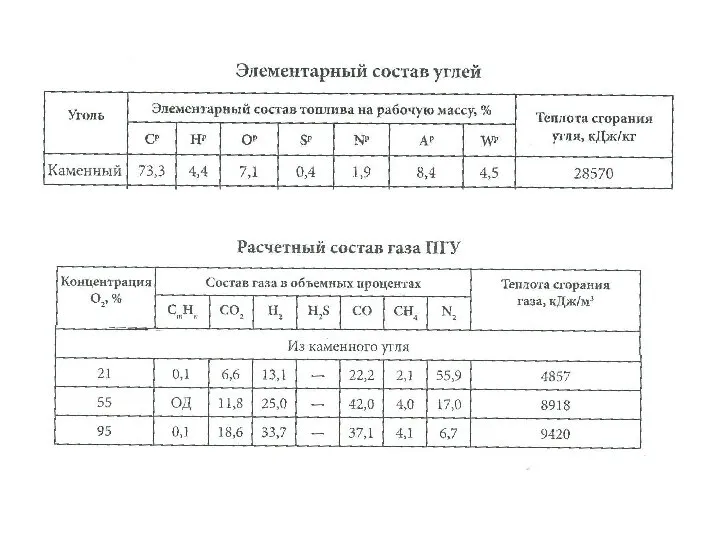 Элементарный состав углей
Элементарный состав углей Золоторудное поле Дуэт
Золоторудное поле Дуэт Кислотно-основные равновесия в растворах
Кислотно-основные равновесия в растворах Теория строения вещества. Межмолекулярные взаимодействия. Водородная связь. Специфические взаимодействия
Теория строения вещества. Межмолекулярные взаимодействия. Водородная связь. Специфические взаимодействия Степень окисления (СО) – § 18
Степень окисления (СО) – § 18 Природный и попутные нефтяные газы
Природный и попутные нефтяные газы Химия в косметике
Химия в косметике Задания на альдегиды и кетоны
Задания на альдегиды и кетоны Свойства глюкозы
Свойства глюкозы Основы молекулярно - кинетической теории
Основы молекулярно - кинетической теории Презентация на тему Правила безопасности труда в кабинете химии
Презентация на тему Правила безопасности труда в кабинете химии  Презентация на тему Знаешь ли ты классы неорганических веществ
Презентация на тему Знаешь ли ты классы неорганических веществ  Сера и её соединения
Сера и её соединения Презентация на тему Классы неорганических веществ
Презентация на тему Классы неорганических веществ  Металлом называется светлое тело, которое ковать можно
Металлом называется светлое тело, которое ковать можно Термодинамика живого объекта. Основы биоэнергетики. Лекция 2
Термодинамика живого объекта. Основы биоэнергетики. Лекция 2