Содержание
- 2. ВИЩІ КАРБОНОВІ КИСЛОТИ (СКОРОЧЕНО ВКК) - КАРБОНОВІ КИСЛОТИ, У МОЛЕКУЛАХ ЯКИХ МІСТИТЬСЯ ВІД 12 ДО 22
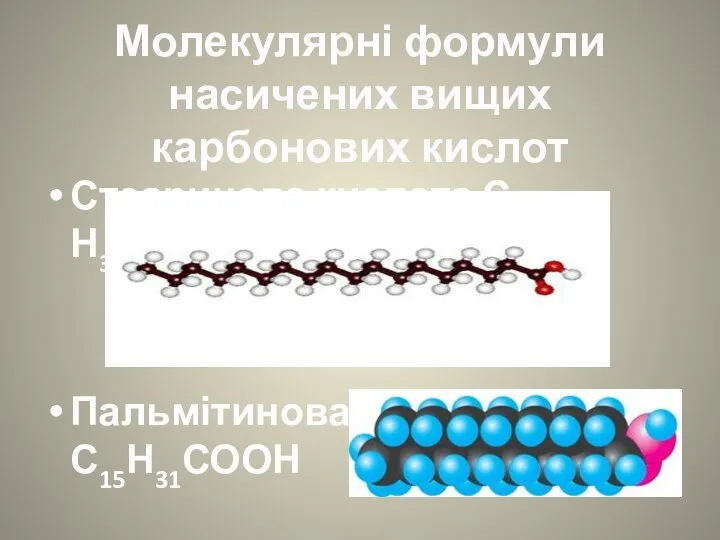
- 3. Молекулярні формули насичених вищих карбонових кислот Стеаринова кислота С17 Н35СООН Пальмітинова кислота С15Н31СООН
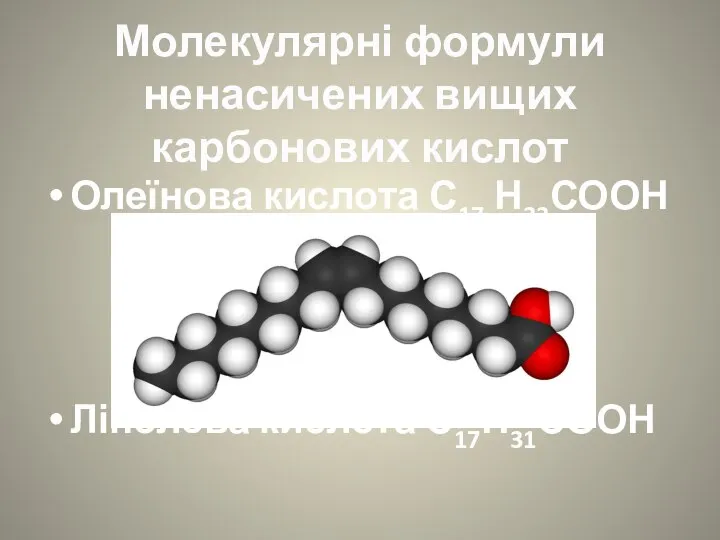
- 4. Молекулярні формули ненасичених вищих карбонових кислот Олеїнова кислота С17 Н33СООН Лінолева кислота С17Н31СООН
- 5. ФІЗИЧНІ ВЛАСТИВОСТІ Стеаринова та пальмітинова тверді речовини білого кольору, нерозчинні у воді, жирні на дотик, без
- 6. ХІМІЧНІ ВЛАСТИВОСТІ Взаємодія з лугами та солями більш слабких кислот - з утвореннями солей С17Н35СООН +
- 7. МИЛА Солі вищих (жирних) карбонових кислот Мають йонну будову Розчинні у воді – солі Натрія, Калія
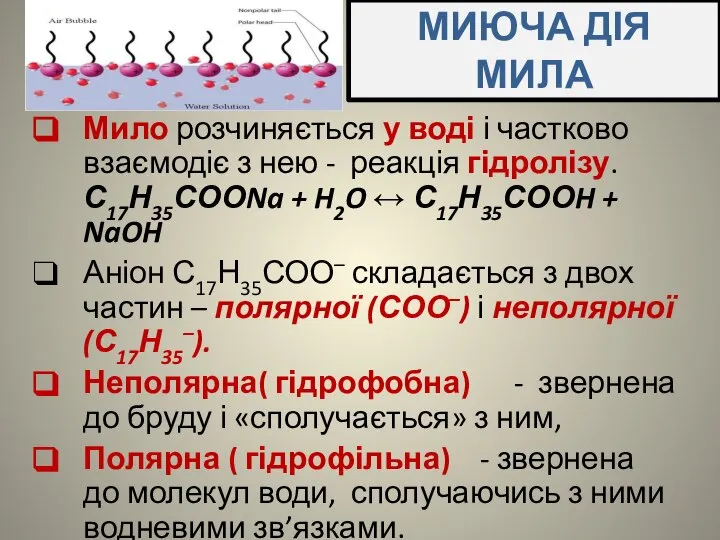
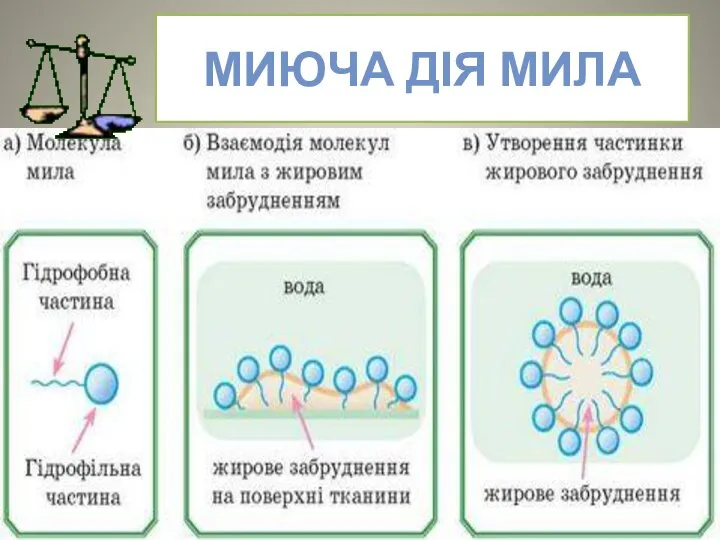
- 8. МИЮЧА ДІЯ МИЛА Мило розчиняється у воді і частково взаємодіє з нею - реакція гідролізу. С17Н35СООNa
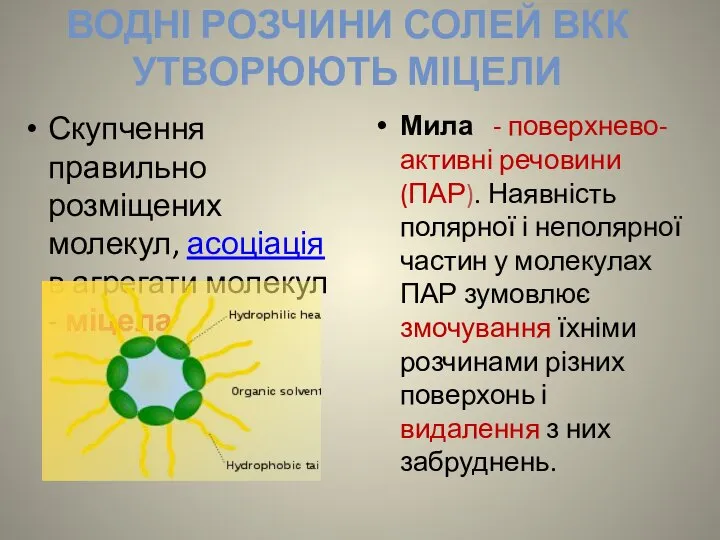
- 9. ВОДНІ РОЗЧИНИ СОЛЕЙ ВКК УТВОРЮЮТЬ МІЦЕЛИ Скупчення правильно розміщених молекул, асоціація в агрегати молекул - міцела
- 10. МИЮЧА ДІЯ МИЛА
- 11. ПРОЦЕСИ ПРИ РОЗЧИНЕННІ МИЛА 1. Емульгування жирів. Утворений при гідролізі мила луг емульгує жир, перетворює його
- 12. Лабораторний дослід. “Дослідження кислотності середовища розчину господарського мила” Відберіть дві проби розчину мила. У першу додайте
- 14. Скачать презентацию






 Углеводы. Тема 9
Углеводы. Тема 9 Silīcija savienojumi
Silīcija savienojumi Пероксид водорода
Пероксид водорода Генетическая связь между классами неорганических веществ
Генетическая связь между классами неорганических веществ Кремний и его соединения
Кремний и его соединения Пространственная изомерия органических соединений
Пространственная изомерия органических соединений Хром. Месторождения
Хром. Месторождения Степень окисления
Степень окисления Окситоцин. Сила любви и биология
Окситоцин. Сила любви и биология Органические соединения в быту. Понятие о бытовых химикатах
Органические соединения в быту. Понятие о бытовых химикатах Substancje chemiczne
Substancje chemiczne Химия вокруг нас
Химия вокруг нас Аминокислоты. Свойства. Промышленные способы получения
Аминокислоты. Свойства. Промышленные способы получения Типичные реакции оснований
Типичные реакции оснований Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы
Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы Произведение растворимости
Произведение растворимости Закон сохранения массы веществ
Закон сохранения массы веществ Химическая кинетика
Химическая кинетика Химическая связь и строение вещества
Химическая связь и строение вещества Арены. Бензол
Арены. Бензол Кислоты: состав, классификация, номенклатура, получение
Кислоты: состав, классификация, номенклатура, получение Mechanika płynów
Mechanika płynów Определение площади поверхности и пористости материалов методом сорбции газов
Определение площади поверхности и пористости материалов методом сорбции газов Эмпирические правила
Эмпирические правила Аймақтық мета морфизм тауж ыныстары
Аймақтық мета морфизм тауж ыныстары Диагностическое тестирование по химии в 8 классе
Диагностическое тестирование по химии в 8 классе Производство серной кислоты контактным способом
Производство серной кислоты контактным способом Окислительно-восстановительные реакции
Окислительно-восстановительные реакции