Содержание
- 2. В О Д О Р О Д «Вода… Ты не имеешь ни вкуса ни цвета ни
- 3. В О Д О Р О Д H -химический элемент сатомным номером 1, атомная масса 1.00794.
- 4. Так как в ядре атома водорода содержится только 1 протон то иногда говорят, что водород образует
- 6. В О Д О Р О Д
- 7. В О Д О Р О Д
- 8. ВОДА – ЭТО ЖИЗНЬ
- 9. Жидкой водой наполнен Мировой океан, поверхностные воды суши и подземные воды Твердый лед можно увидеть и
- 10. 1 % 99 % Вода - это самое распространенное вещество на Земле
- 11. Подземные воды Испарение воды Испарение воды конденсация Запасы воды остаются неизменными в течение миллиардов лет, т.к.
- 13. Сульфат меди хорошо растворим в воде Песок не растворяется в воде Борная кислота малорастворима в воде
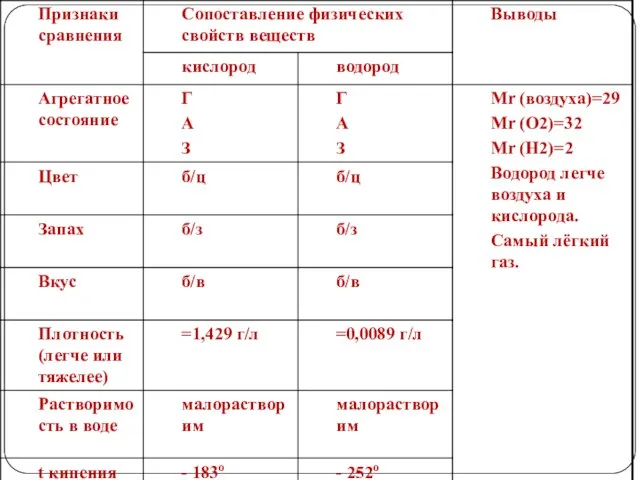
- 14. Общая характеристика газообразных веществ
- 16. В лаборатории: Взаимодействие цинка с соляной кислотой: Zn+2H Cl=ZnCl2+ H2 хлорид цинка Взаимодействие калия с водой:
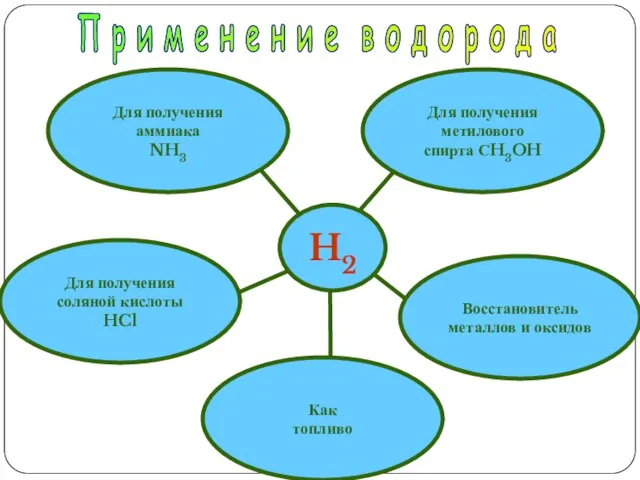
- 17. H2 Для получения аммиака NH3 Восстановитель металлов и оксидов Для получения соляной кислоты HCl Как топливо
- 18. Как горючий (воспламеняемый) воздух водород известен довольно давно.Его получали действием кислот на металлы, наблюдали горение и
- 19. Генри Кавендиш, подробно исследовавший свойства водорода, выдвинул подобную же гипотезу в 1766 г. Он называл водород
- 20. Лавуазье водород (Hydrogene) упомянул в числе пяти (свет, теплота, кислород, азот, водород) «простых тел, относящихся ко
- 21. 97 % - морская вода 3% - пресная вода Ледники – 79% Подземные воды 20% Реки,
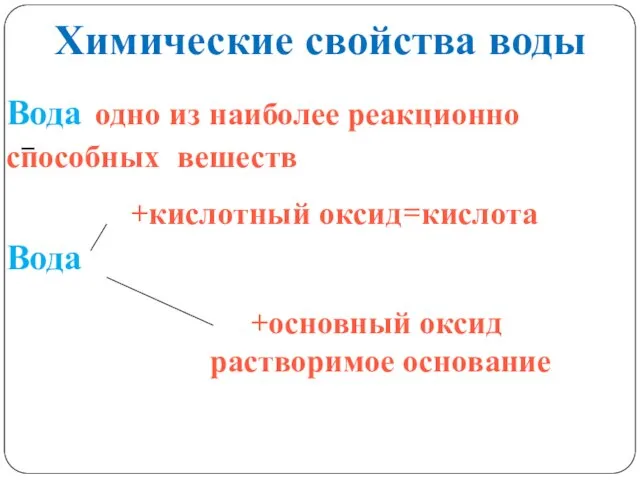
- 22. – +кислотный оксид=кислота Вода одно из наиболее реакционно способных вешеств Вода +основный оксид растворимое основание Химические
- 24. Скачать презентацию


















 Рівняння характеристики крупності
Рівняння характеристики крупності Химическая связь
Химическая связь Красители для волос. Первая группа
Красители для волос. Первая группа Комплексонометрическое титрование. 5 лекция. Часть 2
Комплексонометрическое титрование. 5 лекция. Часть 2 Металлы
Металлы Кислоты
Кислоты Карбоксилденген этоксилаттар
Карбоксилденген этоксилаттар Сухой лёд
Сухой лёд Органические реагенты
Органические реагенты Относительная молекулярная масса вещества
Относительная молекулярная масса вещества Судың диссоциациясы
Судың диссоциациясы Презентация на тему Биополимеры
Презентация на тему Биополимеры  Презентация на тему Классификация химических реакций 11 класс
Презентация на тему Классификация химических реакций 11 класс  Бытовая химия
Бытовая химия Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы
Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы Резиновые материалы и клеи. Тема 7.5
Резиновые материалы и клеи. Тема 7.5 Пористые стекла
Пористые стекла Разбор контрольной работы. Химия (9 класс)
Разбор контрольной работы. Химия (9 класс) Идеальный газ
Идеальный газ Электролитическая диссоциация
Электролитическая диссоциация Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических
Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических Строение атома. Периодический закон
Строение атома. Периодический закон Соединения щелочноземельных металлов
Соединения щелочноземельных металлов Химические реакции. Классификация
Химические реакции. Классификация Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5)
Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5) Золото
Золото Пластмассы
Пластмассы Изучение основного солевого состава брендов бутилированной воды, присутствующих на рынке России
Изучение основного солевого состава брендов бутилированной воды, присутствующих на рынке России