Слайд 2СЛОЖНЫЕ ВЕЩЕСТВА:
ОКСИДЫ
ОСНОВАНИЯ
КИСЛОТЫ
АМФОТЕРНЫЕ ГИДРОКСИДЫ
СОЛИ

Слайд 5ЗНАЧЕНИЕ КИСЛОТ В ЖИЗНИ ЧЕЛОВЕКА
Пищевкусовые добавки
Консервирование
Производство
лекарственных средств, красителей, полимеров,
взрывчатых веществ,

удобрений,
пищевых продуктов.
Слайд 6ТЕМА УРОКА: КИСЛОТЫ
ЦЕЛЬ:
СИСТЕМАТИЗИРОВАТЬ И ОБОБЩИТЬ ЗНАНИЯ О НЕОРГАНИЧЕСКИХ И ОРГАНИЧЕСКИХ КИСЛОТАХ
ЗАДАЧИ:
УГЛУБИТЬ

ЗНАНИЯ О НОМЕНКЛАТУРЕ И ПРИНЦИПАХ КЛАССИФИКАЦИИ КИСЛОТ
РАССМОТРЕТЬ ЗАВИСИМОСТЬ ИЗМЕНЕНИЯ СВОЙСТВ КИСЛОТ ОТ СОСТАВА ИХ МОЛЕКУЛ
ОБОБЩИТЬ ЗНАНИЯ ОБ ОБЩИХ ХИМИЧЕСКИХ СВОЙСТВАХ КИСЛОТ
РАЗВИВАТЬ УМЕНИЯ НАПИСАНИЯ УРАВНЕНИЙ ХИМИЧЕСКИХ РЕАКЦИЙ С УЧАСТИЕМ КИСЛОТ
РАССМОТРЕТЬ НАХОЖДЕНИЕ КИСЛОТ В ПРИРОДЕ ИХ РОЛЬ В ЖИЗНИ ЧЕЛОВЕКА
Слайд 7 Кислоты – это соединения,
состоящие из кислотных остатков
и атомов водорода,

способных замещаться атомами металлов
с образованием солей.
Слайд 8КЛАССИФИКАЦИЯ КИСЛОТ
ПО СОДЕРЖАНИЮ АТОМОВ КИСЛОРОДА В МОЛЕКУЛЕ
КИСЛОТЫ
КИСЛОРОДСОДЕРЖАЩИЕ БЕСКИСЛОРОДНЫЕ
Слайд 9КЛАССИФИКАЦИЯ КИСЛОТ
ПО КОЛИЧЕСТВУ АТОМОВ ВОДОРОДАВ МОЛЕКУЛЕ
КИСЛОТЫ
ОДНООСНОВНЫЕ ТРЕХОСНОВНЫЕ
ДВУХОСНОВНЫЕ
Слайд 10КЛАССИФИКАЦИЯ КИСЛОТ
ПО РАСТВОРИМОСТИ В ВОДЕ
КИСЛОТЫ
РАСТВОРИМЫЕ НЕРАСТВОРИМЫЕ
Слайд 11КЛАССИФИКАЦИЯ КИСЛОТ
ПО ЛЕТУЧЕСТИ
КИСЛОТЫ
ЛЕТУЧИЕ НЕЛЕТУЧИЕ
Слайд 12КЛАССИФИКАЦИЯ КИСЛОТ
ПО СТЕПЕНИ ДИССОЦИАЦИИ
КИСЛОТЫ
СИЛЬНЫЕ СЛАБЫЕ
Слайд 13КЛАССИФИКАЦИЯ КИСЛОТ
ПО СТАБИЛЬНОСТИ (УСТОЙЧИВОСТИ)
КИСЛОТЫ
СТАБИЛЬНЫЕ НЕСТАБИЛЬНЫЕ
Слайд 14НОМЕНКЛАТУРА КИСЛОТ
Бескислородные кислоты:
К названию кислотообразующего элемента добавляют гласную «о» и слова

«водородная кислота»
H2S – сероводородная кислота
Кислородсодержащие кислоты:
К русскому названию кислотообразующего элемента добавляют суффикс.
+5
Если элемент проявляет высшую СО – «-ная»: HNO3
+3
Если СО элемента ниже высшей – «-истая»: HNO2
Слайд 15ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ
ДИССОЦИАЦИЯ КИСЛОТ
Какие кислоты диссоциируют ступенчато?
Какова окраска лакмуса в растворах кислот?
Наличием

каких ионов обусловлена окраска лакмуса?
Когда в повседневной жизни мы встречаемся с процессом диссоциации кислот?
Слайд 16ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ
ВЗАИМОДЕЙСТВИЕ КИСЛОТ С МЕТАЛЛАМИ
И ОСНОВНЫМИ ОКСИДАМИ
ВСЕ ЛИ МЕТАЛЛЫ РЕАГИРУЮТ С

КИСЛОТАМИ?
ПОЧЕМУ ХИМИЧЕСКАЯ РЕАКЦИЯ АЛЮМИНИЯ С КИСЛОТОЙ НАЧИНАЕТСЯ ТОЛЬКО ПОСЛЕ НАГРЕВАНИЯ?
МОЖНО ЛИ В АЛЮМИНИЕВОЙ ПОСУДЕ ГОТОВИТЬ КИСЛЫЕ ЩИ?
МОЖНО ЛИ В ОЦИНКОВАННОМ ВЕДРЕ ХРАНИТЬ ЯГОДУ, КВАСИТЬ КАПУСТУ?
Слайд 17ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ
ВЗАИМОДЕЙСТВИЕ КИСЛОТ
С ОСНОВАНИЯМИ
В ЧЕМ СУТЬ ВЗАИМОДЕЙСТВИЯ КИСЛОТ С ОСНОВАНИЯМИ?
КАК

НАЗЫВАЮТСЯ ДАННЫЕ РЕАКЦИИ? ПОЧЕМУ?
КАК В ПОВСЕДНЕВНОЙ ЖИЗНИ МЫ МОЖЕМ ИСПОЛЬЗОВАТЬ ДАННОЕ СВОЙСТВО КИСЛОТ?
Слайд 18ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ
ВЗАИМОДЕЙСТВИЕ КИСЛОТ
С СОЛЯМИ
В ЧЕМ ОПАСНОСТЬ КИСЛОТНЫХ ДОЖДЕЙ ДЛЯ АРХИТЕКТУРНЫХ

ПАМЯТНИКОВ?
КОГДА В ПОВСЕДНЕВНОЙ ЖИЗНИ МЫ ВСТРЕЧАЕМСЯ С РЕАКЦИЕЙ ВЗАИМОДЕЙСТВИЯ ГИДРОКАРБОНАТА НАТРИЯ С УКСУСНОЙ КИСЛОТОЙ?
ВСЕ ЛИ СОЛИ И КИСЛОТЫ БУДУТ ВЗАИМОДЕЙСТВОВАТЬ МЕЖДУ СОБОЙ?
Слайд 19Кислотные свойства кислот, образованных элементами одного периода:
H3BO3 - H2CO3 - H2SO4
усиливаются

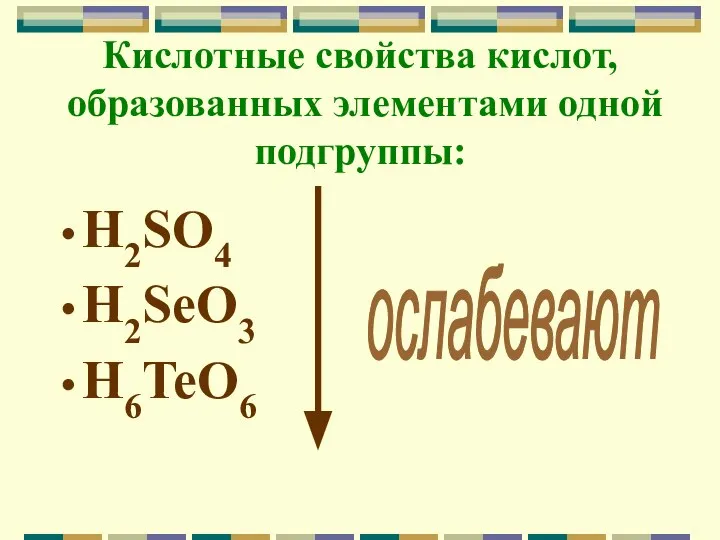
Слайд 20Кислотные свойства кислот, образованных элементами одной подгруппы:
H2SO4
H2SeO3
H6TeO6
ослабевают
Слайд 21Кислотные свойства кислот, образованных элементом
в различных СО:
+5 +6
HNO3 H2SO4

+3 +4
HNO2 H2SO3
усиливаются




















 Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Химия и сельское хозяйство
Химия и сельское хозяйство Оксидтер мен негіздердің реакциялары
Оксидтер мен негіздердің реакциялары Алгоритмы при изучении химии
Алгоритмы при изучении химии Презентация на тему Витамины. Урок химии 10 класс
Презентация на тему Витамины. Урок химии 10 класс  Алкины и их свойства
Алкины и их свойства Химия и автомобиль
Химия и автомобиль Углеводороды: изомерия
Углеводороды: изомерия Амилаза. Строение амилазы
Амилаза. Строение амилазы Минеральные кислоты. Взаимодействие с простыми веществами
Минеральные кислоты. Взаимодействие с простыми веществами Энергетические уровни
Энергетические уровни Углеводороды (УВ)
Углеводороды (УВ) Олеиновая кислота
Олеиновая кислота Химия һәм сәламәт яшәү рәвеше
Химия һәм сәламәт яшәү рәвеше Презентация на тему Кальций
Презентация на тему Кальций  Арены. Бензол
Арены. Бензол Задания для подготовки к ЕГЭ по химии
Задания для подготовки к ЕГЭ по химии Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Любовь и химия
Любовь и химия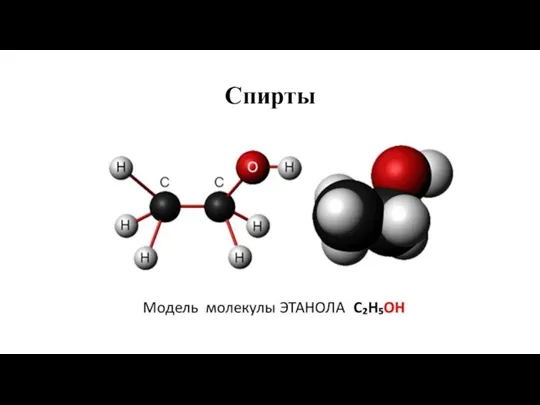 Спирты
Спирты Алкены. Этилен C2H4
Алкены. Этилен C2H4 Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Окисление этанола оксидом меди
Окисление этанола оксидом меди Смачивание и не смачивание жидкости. Капилляры
Смачивание и не смачивание жидкости. Капилляры Карбоновые кислоты
Карбоновые кислоты Предмет органической химии. Урок №1
Предмет органической химии. Урок №1 Характеристика кислорода и серы
Характеристика кислорода и серы Свойства ртути
Свойства ртути