Содержание
- 2. Серная кислота H2SO4 — сильная двухосновная кислота. При обычных условиях концентрированная серная кислота — тяжёлая маслянистая
- 3. Ее используют как гигроскопическое средство во многих химических реакциях, особенно при получении органических веществ, для осушки
- 4. Кроме того, благодаря этой способности, концентрированная серная кислота обугливает органические вещества (сахар, древесину), вызывает сильные ожоги
- 6. Свойства разбавленной серной кислоты Разбавленная H2SO4 - вступает в реакции замещения, за счет окисления катионов Н+:
- 7. Качественной реакцией на серную кислоту и её растворимые соли является их взаимодействие с растворимыми солями бария,
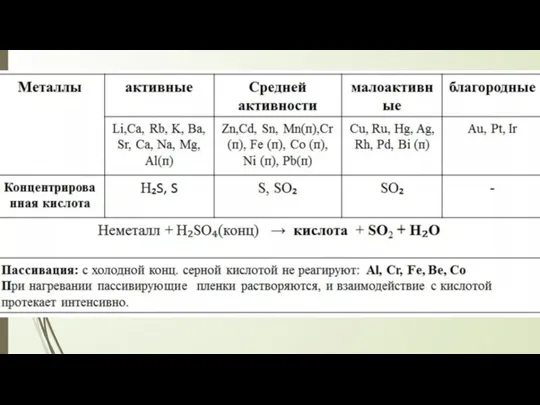
- 8. Свойства концентрированной серной кислоты Al, Cr, Fe пассивируются в конц.H2SO4, но реагируют с ней при нагревании:
- 10. Взаимодействие серной кислоты с неметаллами Взаимодействие серной кислоты с неметаллами происходит с выделением SO2 и окислением
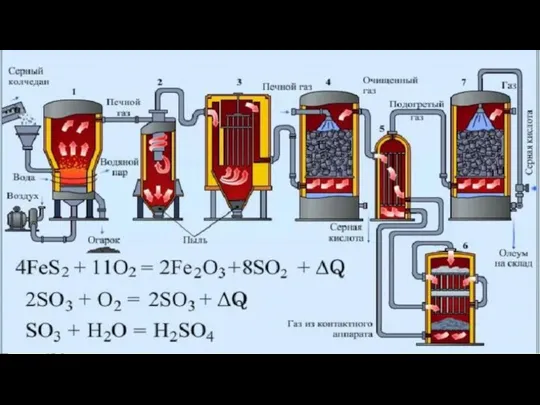
- 11. Производство серной кислоты Видео - https://www.youtube.com/watch?v=uHtmnGjSTNE
- 13. Общие научные принципы химического производства: Непрерывность. Противоток Катализ Увеличение площади соприкосновения реагирующих веществ. Теплообмен Рациональное использование
- 14. 1. Печь для обжига «в кипящем слое»: Пирит подвергают обжигу кислородом воздуха 4FeS2 + 11 O2
- 15. 6. Контактный аппарат: Обжиговый газ в присутствии катализатора при 450 °С окисляется до оксида серы (VI)
- 16. Экологические проблемы: Производство серной кислоты создает немало экологических проблем – на I стадии это потери сырья
- 18. Скачать презентацию













 Химическая кинетика и равновесие
Химическая кинетика и равновесие Окислительно-восстановительные реакции, 9 класс
Окислительно-восстановительные реакции, 9 класс Твердые электролиты
Твердые электролиты Nanofibers of aluminum oxide
Nanofibers of aluminum oxide Введение в хроматографию. Хроматографические методы анализа
Введение в хроматографию. Хроматографические методы анализа Металлы
Металлы Составление формул оксидов, оснований, солей
Составление формул оксидов, оснований, солей 10 класс Алкадиены более совершенная (2)
10 класс Алкадиены более совершенная (2) Химическая связь
Химическая связь Презентация на тему Типы химических реакций (8 класс)
Презентация на тему Типы химических реакций (8 класс)  Экстракционное разделение радионуклидов
Экстракционное разделение радионуклидов Проточные реакторы непрерывного действия. (Лекция 5)
Проточные реакторы непрерывного действия. (Лекция 5) Алкены
Алкены Презентация на тему Альдегиды и их свойства
Презентация на тему Альдегиды и их свойства  Арены. Бензол
Арены. Бензол Изменения, происходящие с веществами
Изменения, происходящие с веществами Железо
Железо Диффузия и осмос
Диффузия и осмос Соли как производные кислот и оснований. Их состав и названия
Соли как производные кислот и оснований. Их состав и названия Занимательная химия Программу составил
Занимательная химия Программу составил  Строение атома
Строение атома Кислоты, их классификация и свойства
Кислоты, их классификация и свойства Соли. Классификация солей
Соли. Классификация солей Геохимический барьер
Геохимический барьер 5 Нефть. Нефтепереработка. Конверсия метана
5 Нефть. Нефтепереработка. Конверсия метана Ліпіди
Ліпіди Электролиз растворов и расплавов неорганических и органических электролитов
Электролиз растворов и расплавов неорганических и органических электролитов Строение и номенклатура карбонильных соединений
Строение и номенклатура карбонильных соединений