Содержание
- 2. Положение металлов в Периодической системе Строение атомов Кристаллические решётки Общие физические свойства Металлы в природе Способы
- 4. К металлам относятся простые вещества, которые образуют:
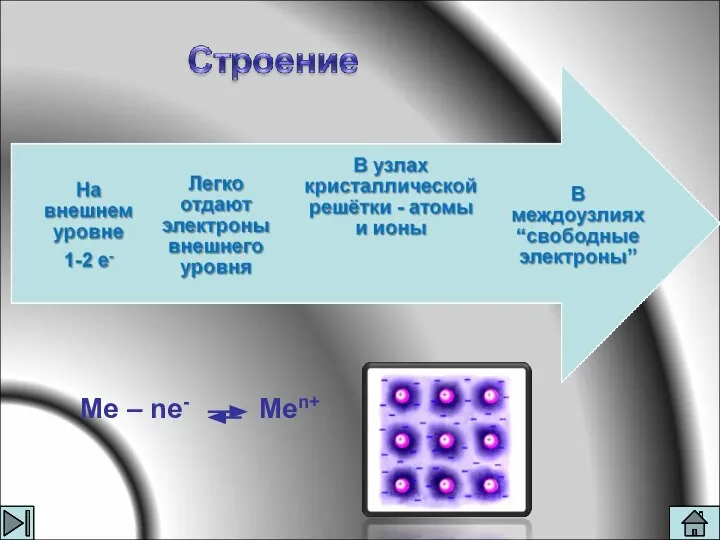
- 5. Ме – ne- Men+
- 7. Все твердые, кроме ртути Металлический блеск Пластичность, ковкость Электропроводность Теплопроводность Высокие температуры плавления
- 8. Самый распространённый металл в природе - алюминий - более 8% от земной коры
- 11. Получение металлов из руд их восстановлением. Восстановители:
- 12. Получение металлов электролизом:
- 13. Получение металлов восстановлением из растворов солей:
- 14. Металлы - восстановители Ме0 – ne- = Men+ процесс окисления С простыми веществами-неметаллами С водой С
- 16. 2K + 2H2O = 2KOH + H2↑ Zn + 2H2O = ZnO + H2↑ 3Fe +
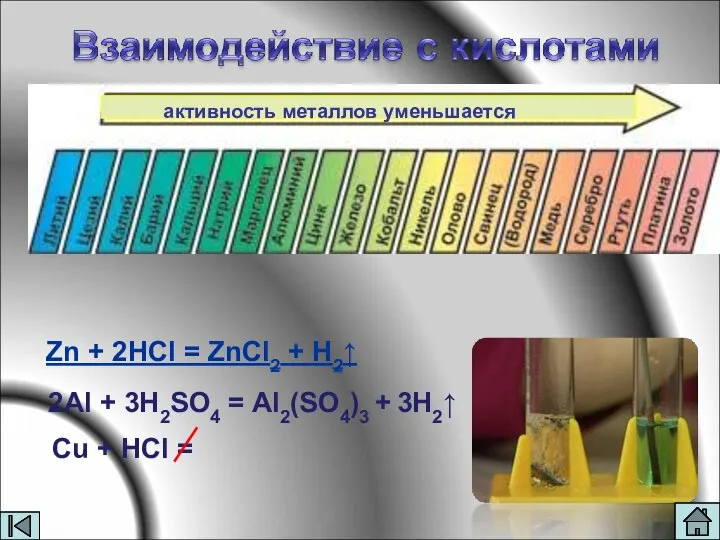
- 17. Zn + 2HCl = ZnCl2 + H2↑ 2Al + 3H2SO4 = Al2(SO4)3 + 3H2↑ Cu +
- 20. Скачать презентацию














 Научные принципы химического производства
Научные принципы химического производства Лаборатория мечты
Лаборатория мечты Введение в общую теорию поверхностных явлений. Лекция 1
Введение в общую теорию поверхностных явлений. Лекция 1 3 Серная кислота
3 Серная кислота Презентация на тему Классификация кислот
Презентация на тему Классификация кислот  Технологические процессы получения кислорода
Технологические процессы получения кислорода Строение вещества. Виды химической связи
Строение вещества. Виды химической связи Алканы 10-класс
Алканы 10-класс Способы получения металлов
Способы получения металлов Карбонаты. Лекция 12
Карбонаты. Лекция 12 Органическая химия. Центр дистанционного обучения
Органическая химия. Центр дистанционного обучения Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Понятие электродного потенциала и методы его измерения
Понятие электродного потенциала и методы его измерения Полиморфизм. Аллотропия
Полиморфизм. Аллотропия Сода. Что я знаю о ней!?
Сода. Что я знаю о ней!? Неорганические молекулы живого вещества: вода; химические свойства и биологическая роль
Неорганические молекулы живого вещества: вода; химические свойства и биологическая роль Скорость химической реакции
Скорость химической реакции Масляная кислота
Масляная кислота Презентация 3. Теория ЕГЭ
Презентация 3. Теория ЕГЭ Химия металлов. Влияние металлов на организм человека
Химия металлов. Влияние металлов на организм человека Происхождения названий химических элементов
Происхождения названий химических элементов Металлы. Контрольная работа
Металлы. Контрольная работа Неорганическая и органическая химия
Неорганическая и органическая химия Растворы. Лекция 7
Растворы. Лекция 7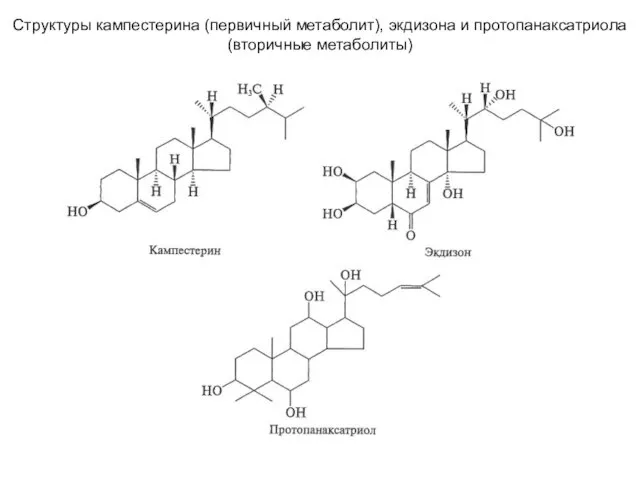 Структуры кампестерина (первичный метаболит), экдизона и протопанаксатриола (вторичные метаболиты)
Структуры кампестерина (первичный метаболит), экдизона и протопанаксатриола (вторичные метаболиты) Коррозия металлов
Коррозия металлов Химия функциональных материалов. Адсорбция
Химия функциональных материалов. Адсорбция Чистые вещества и смеси
Чистые вещества и смеси