Содержание
- 2. Что такое ГИДРОКСИДЫ и как их классифицируют?
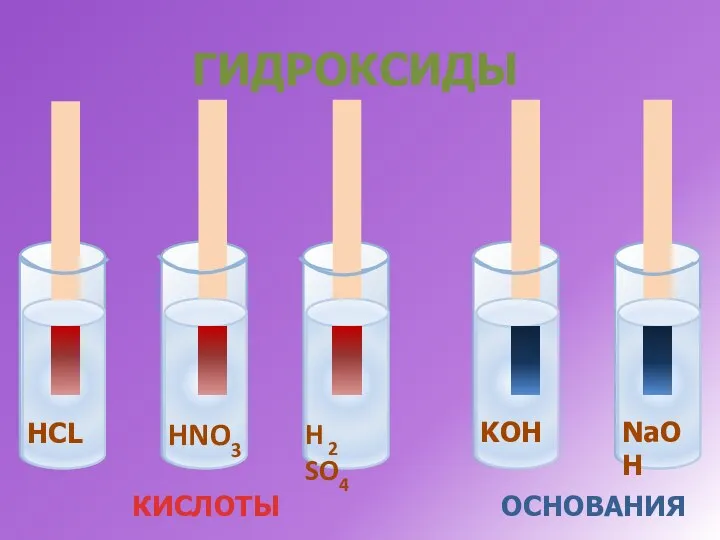
- 3. Индикатор ЛАКМУС в разных средах: ЩЕЛОЧЬ КИСЛОТА ВОДА
- 4. ГИДРОКСИДЫ КИСЛОТЫ ОСНОВАНИЯ HCL NaOH KOH H 2 SO4 HNO3
- 5. Приведите примеры ОСНОВАНИЙ
- 6. ПРИМЕРЫ ОСНОВАНИЙ: Na OH K OH Ca (OH)2 Ba (OH)2 Al (OH)3
- 7. Что общего в этих формулах? Гидроксильная группа -OH I и металлы
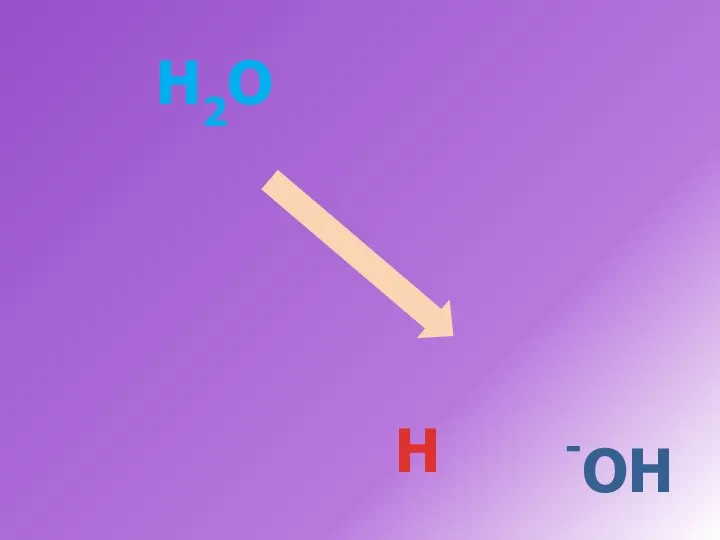
- 8. H2O H -OH
- 9. ОСНОВАНИЯ – ЭТО СЛОЖНЫЕ ВЕЩЕСТВА, В СОСТАВ КОТОРЫХ ВХОДЯТ АТОМЫ МЕТАЛЛОВ, СВЯЗАННЫЕ С ОДНОЙ ИЛИ НЕСКОЛЬКИМИ
- 10. Общая формула ОСНОВАНИЙ : (OH)n Me
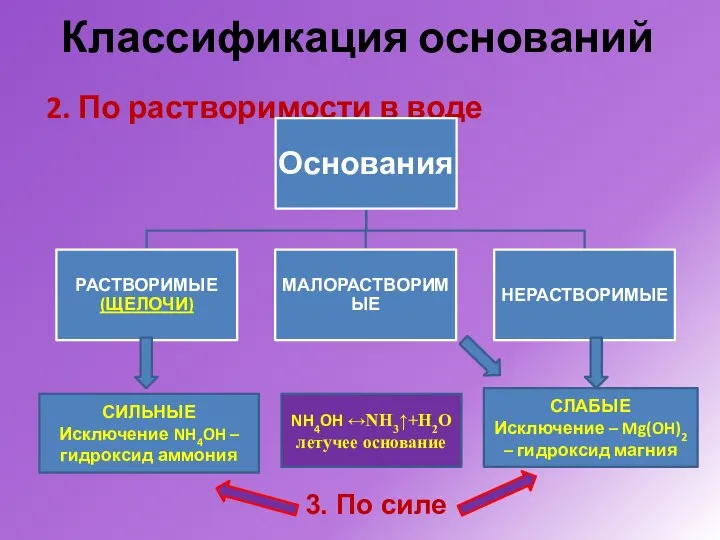
- 11. Как можно классифицировать ОСНОВАНИЯ ?
- 12. Классификация оснований 2. По растворимости в воде СЛАБЫЕ Исключение – Mg(OH)2 – гидроксид магния СИЛЬНЫЕ Исключение
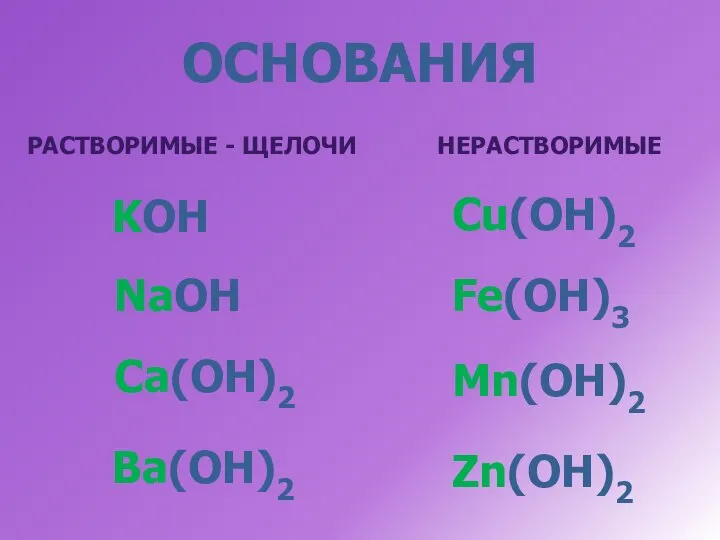
- 13. ОСНОВАНИЯ РАСТВОРИМЫЕ - ЩЕЛОЧИ НЕРАСТВОРИМЫЕ KOH NaOH Ca(OH)2 Ba(OH)2 Cu(OH)2 Fe(OH)3 Mn(OH)2 Zn(OH)2
- 14. Физические свойства ОСНОВАНИЙ
- 15. Твердое бесцветное вещество
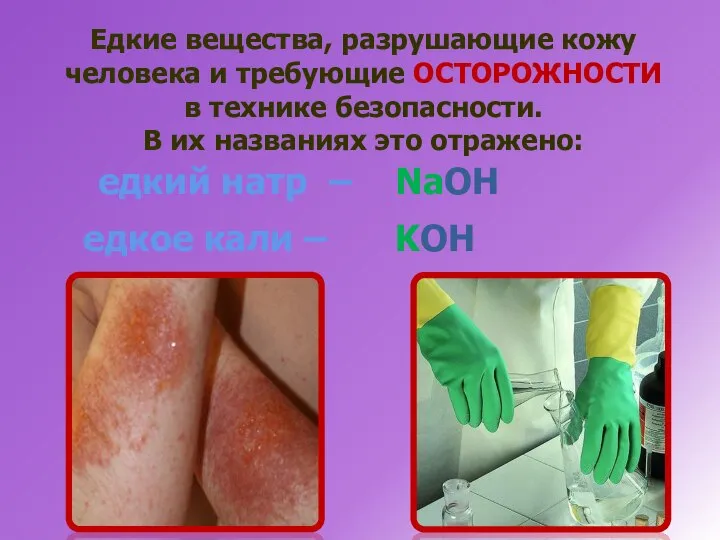
- 16. Едкие вещества, разрушающие кожу человека и требующие ОСТОРОЖНОСТИ в технике безопасности. В их названиях это отражено:
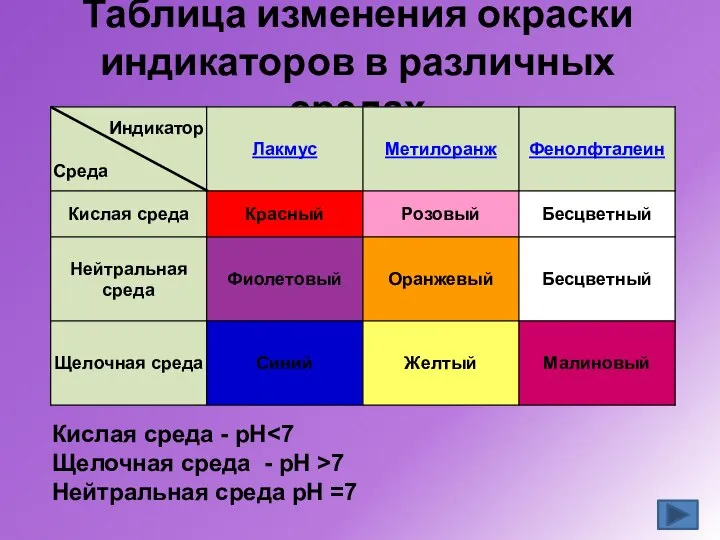
- 17. Таблица изменения окраски индикаторов в различных средах Кислая среда - рН Щелочная среда - рН >7
- 18. Химические свойства ЩЕЛОЧЕЙ: Взаимодействие с индикаторами. Взаимодействие с кислотами. + NaOH HCl = NaOH + HCl
- 19. РЕАКЦИЯ НЕЙТРАЛИЗАЦИИ – ЭТО ВЗАИМОДЕЙСТВИЕ МЕЖДУ КИСЛОТАМИ И ОСНОВАНИЯМИ С ОБРАЗОВАНИЕМ СОЛИ И ВОДЫ
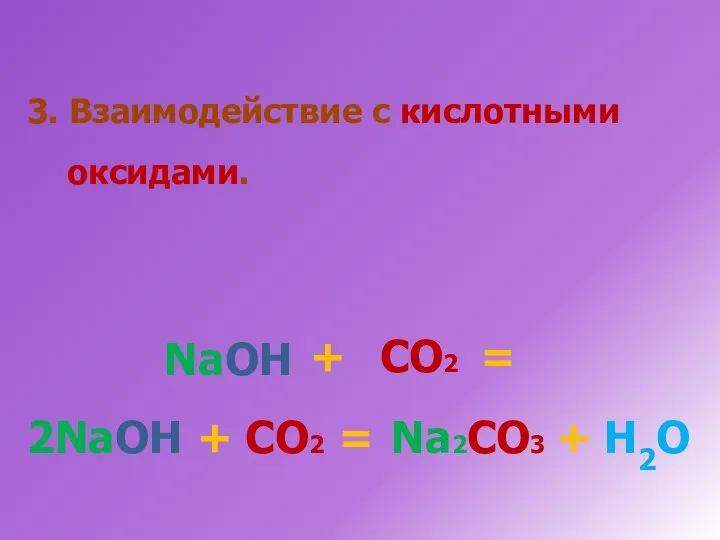
- 20. 3. Взаимодействие с кислотными оксидами. + NaOH СО2 = 2NaOH + СО2 = Na2CО3 + H2O
- 21. Качественное определение веществ Известковая вода – качественный реагент на углекислый газ Гидрокси́д ка́льция ( Ca(OH)2 ,
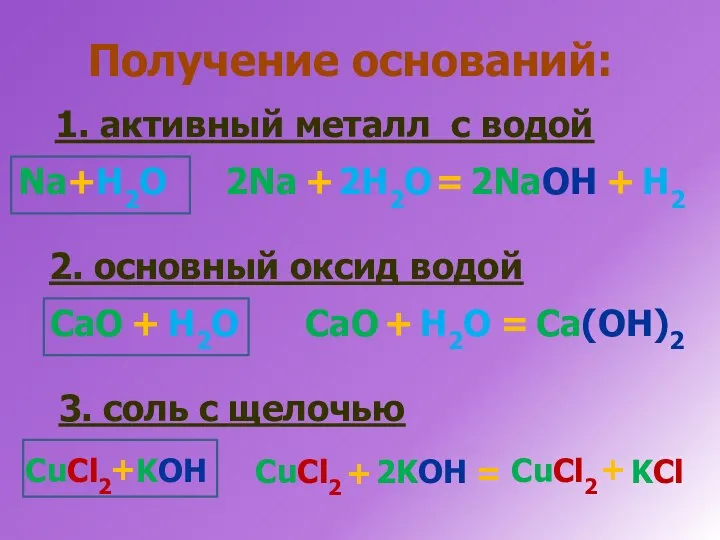
- 22. Получение оснований: 1. активный металл с водой Na + H2O 2Na + 2H2O = 2NaOH +
- 23. Едкий натр применяется во множестве отраслей промышленности и для бытовых нужд: в целлюлозно-бумажной промышленности для делигнификации
- 24. Гидроксид калия «калиевый щёлок» — KOH. Тривиальные названия: едкое кали, каустический поташ. Бесцветные, очень гигроскопичные кристаллы,
- 26. Скачать презентацию















 Титриметрический анализ. Основные понятия
Титриметрический анализ. Основные понятия Структура периодической системы химических элементов
Структура периодической системы химических элементов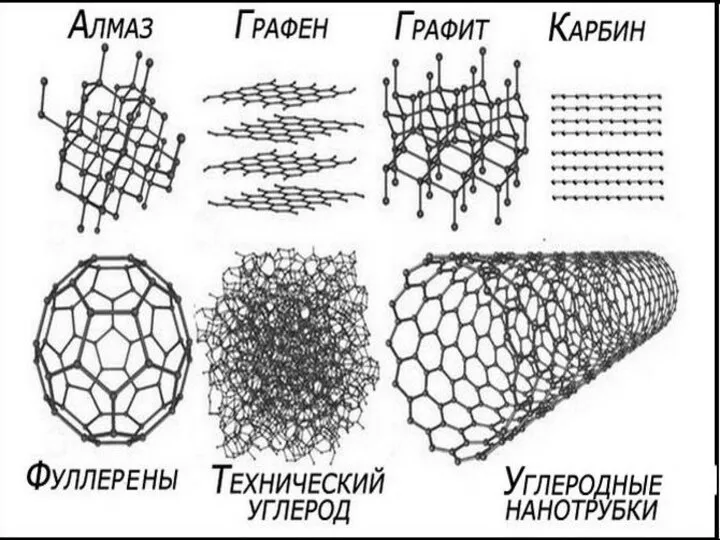 Углеродные нанотрубки
Углеродные нанотрубки Химическая промышленность
Химическая промышленность Производные кислородсодержащих гетероциклов - пиранов
Производные кислородсодержащих гетероциклов - пиранов Пентоза - відновлювальна сировина для синтезу фуранових сполук
Пентоза - відновлювальна сировина для синтезу фуранових сполук Stereoselective total syntheses of guanacastepenes N and O
Stereoselective total syntheses of guanacastepenes N and O Химические свойства основных оксидов. 9 класс
Химические свойства основных оксидов. 9 класс Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Узоры на молоке. Опыт
Узоры на молоке. Опыт Дидактическое сопровождение курса Мир органических соединений
Дидактическое сопровождение курса Мир органических соединений Строение молекулы воды
Строение молекулы воды Коррозия металлов
Коррозия металлов Общая характеристика неметаллов. 9 класс
Общая характеристика неметаллов. 9 класс Вода H2O
Вода H2O Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Карбоновые кислоты
Карбоновые кислоты Презентация на тему Химические свойства бензола. Получение, применение
Презентация на тему Химические свойства бензола. Получение, применение  Элементы химической термодинамики и биоэнергетики. Химическая кинетика
Элементы химической термодинамики и биоэнергетики. Химическая кинетика Соединения азота
Соединения азота Альдегиды и кетоны
Альдегиды и кетоны Презентация на тему Применение кислорода
Презентация на тему Применение кислорода  user_file_562b6f7f7ae4e
user_file_562b6f7f7ae4e Пространственное строение. Стереоизомерия. Структура и функции биолекул
Пространственное строение. Стереоизомерия. Структура и функции биолекул Занимательные задачи по химии
Занимательные задачи по химии Кремний и его соединения
Кремний и его соединения Непредельные углеводороды (алкены)
Непредельные углеводороды (алкены) Магний - активный, но под защитой
Магний - активный, но под защитой