Содержание
- 2. Родоначальниками соединений в органической химии являются углеводороды. Если рассматривать строение углеродного скелета органических веществ, то все
- 3. Рис. 1. Примеры ациклических и циклических углеводородовК ним относятся предельные углеводороды, где все связи в молекуле
- 4. Классификация органических веществ по наличию функциональной группы Если за основу классификации взять наличие в молекуле функциональных
- 5. Сравнение свойств предельных и непредельных углеводородов Предельные углеводороды. Простейшим представителем предельных углеводородов является метан. Его формула
- 6. Свойства веществ, содержащих функциональные группы Свойства производных углеводородов Основные свойства каждого класса органических веществ, производных углеводородов,
- 7. Спирты. Атом водорода в составе функциональной группы спиртов способен замещаться на атомы металла, поэтому спирты могут
- 8. Реакция серебряного зеркала В этой окислительно-восстановительной реакции альдегид превращается в кислоту, а серебро выделяется в свободном
- 9. Карбоновые кислоты Для карбоновых кислот характерны реакции со спиртами, а также общие свойства кислот. Это взаимодействие
- 10. Аминокислоты Аминокислоты – это бифункциональные соединения. Аминокислоты – это вещества, в молекулах которых содержатся одновременно аминогруппа
- 11. Аминокислоты Аминокислоты можно рассматривать как карбоновые кислоты, в молекулах которых атом водорода в радикале замещен аминогруппой.
- 12. Углеводы Глюкоза C6H12O6 относится к классу углеводов. Это тоже бифункциональное соединение, так как в ее молекуле
- 13. Генетическая связь Между классами органических веществ существует генетическая связь. Рис. 3. Генетическая связь кислородсодержащих органических соединений
- 14. Список рекомендованной литературы 1. Рудзитис Г.Е. Неорганическая и органическая химия. 9 класс: Учебник для общеобразовательных учреждений:
- 15. Рекомендованные ссылки на интернет-ресурсы 1. http://interneturok.ru/ru/school/chemistry/11-klass/bstroenie-atoma-periodicheskij-zakonb/periodicheskij-zakon-i-periodicheskaya-sistema-himicheskih-elementov-di-mendeleeva 2. http://www.hemi.nsu.ru/ucheb134.htm 3. http://chemport.ru/pertable/ 4. http://www.xumuk.ru/encyklopedia/2/5324.html
- 17. Скачать презентацию














 Практическая работа по теме Получение и свойства соединений металлов
Практическая работа по теме Получение и свойства соединений металлов Соли в природе. Реакции с участием солей. Модуль 2. Лекция 2.1
Соли в природе. Реакции с участием солей. Модуль 2. Лекция 2.1 Её величество – вода Интегрированный урок химии в 8 классе
Её величество – вода Интегрированный урок химии в 8 классе Zirconium Dioxide
Zirconium Dioxide Неорганическая химия 1 семестра. Растворы
Неорганическая химия 1 семестра. Растворы Ацилирование. Лекция 4
Ацилирование. Лекция 4 Химический диктант как метод формирующего оценивания
Химический диктант как метод формирующего оценивания Теория валентных связей
Теория валентных связей Презентация на тему Изотопы
Презентация на тему Изотопы  Министерство сельского хозяйства Российской Федерации. Поляграфия и фотоэлектронная спектроскопия
Министерство сельского хозяйства Российской Федерации. Поляграфия и фотоэлектронная спектроскопия Закономерности изменения свойств галогенов
Закономерности изменения свойств галогенов Презентация на тему Характеристика щелочных металлов 9 класс
Презентация на тему Характеристика щелочных металлов 9 класс  Поделочный камень родонит
Поделочный камень родонит Лабораторное оборудование. Тесты
Лабораторное оборудование. Тесты G12 - класс антифризов
G12 - класс антифризов Взвешивание. Аналитические весы
Взвешивание. Аналитические весы Презентация на тему Химические реакции 11 класс
Презентация на тему Химические реакции 11 класс 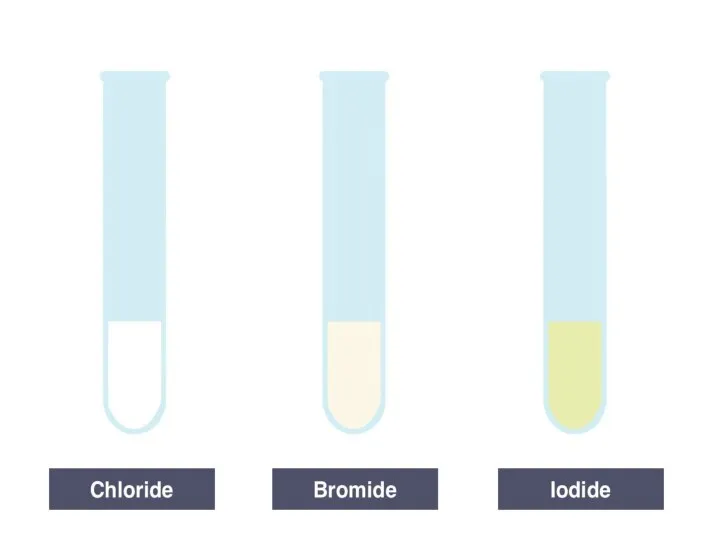 Определение галогенид-ионов в водном растворе. Лабораторный опыт
Определение галогенид-ионов в водном растворе. Лабораторный опыт Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения! Количество теплоты, для получения углекислого газа. Химическое равновесие. Примеры. (Лекция 4)
Количество теплоты, для получения углекислого газа. Химическое равновесие. Примеры. (Лекция 4) Алкадиены. Строение. Изомерия. Свойства
Алкадиены. Строение. Изомерия. Свойства Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Степень окисления. Составление формул бинарных соединений. 8 класс
Степень окисления. Составление формул бинарных соединений. 8 класс Сложные эфиры и жиры
Сложные эфиры и жиры Алканы и алкены
Алканы и алкены Карбоновые кислоты
Карбоновые кислоты Металлы и их соединения. Решение экспериментальных задач
Металлы и их соединения. Решение экспериментальных задач Анилин как органическое основание
Анилин как органическое основание