Слайд 2Что можно и нужно узнать?
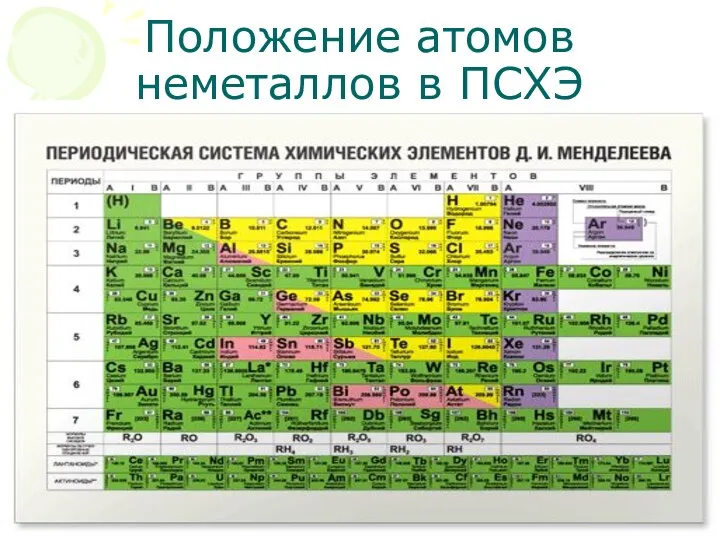
Положение х.э. неМе в ПСХЭ
Особенности строения их атомов
Окислительно-восстановительные

способности
Как выглядят неМе простые вещества
Причины их многообразия
Слайд 3Положение атомов неметаллов в ПСХЭ
Слайд 4Особенности строения атомов неметаллов
Электронов на внешнем уровне атома
Радиус атома
Электроотрицательность
В химических реакциях

восстановители или окислители
Как изменяются окислительные свойства
Самый сильный окислитель
Слайд 6Докажем, что это так!
Определите окислитель.
Cl2 + Na =
Cl2 + Cu =

O2 + S =
O2 + Fe =
F2 + S =
F2 + Pt =
Слайд 7Физические свойства (стр.89-90)
Агрегатное состояние
Цвет, запах
Температура плавления
кристаллические решетки
Причина многообразия простых веществ при небольшом

разнообразии атомов неметаллов
Слайд 10Подведем итог урока
неметаллы- это простые вещества, не обладающие свойствами…
х.э неМе располагаются в

… ПСХЭ
на внешнем уровне у их атомов от… до… электронов
отсюда следует а) радиус атомов… б)электроотрицательность…в) в химических реакциях в основном проявляют… свойства.
самый сильный окислитель-…, затем …
простых веществ неМе больше, чем неМе х.э, потому,что…
Слайд 11 Проверим себя (ТПО стр 142 №2-7 и25, 27 (1,2)
4)фтор
2) 16 и

18
3) 2,8,4
4) 2,8,6
2)F,Cl,I
1)3)
2) S S
+4
+6










 Алкины. Строение, номенклатура, изометрия, физические свойства
Алкины. Строение, номенклатура, изометрия, физические свойства Электроотрицательность (ЭО)
Электроотрицательность (ЭО) Химическае препараты
Химическае препараты Туф вулканический
Туф вулканический 9_OSNOVY_KOLANALIZA
9_OSNOVY_KOLANALIZA получение Ме презентация
получение Ме презентация Ионообменные материалы для сорбции биологически активных веществ
Ионообменные материалы для сорбции биологически активных веществ Селективная экстракция отдельных групп БАВ сверхкритическими флюидами
Селективная экстракция отдельных групп БАВ сверхкритическими флюидами Обобщение. Неметаллы
Обобщение. Неметаллы Опыты по теме Свойства основных классов неорганических соединений
Опыты по теме Свойства основных классов неорганических соединений Процессы переработки нефти
Процессы переработки нефти Аналитические методы в современных исследованиях химии
Аналитические методы в современных исследованиях химии Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Химия в нашей жизни
Химия в нашей жизни Соли
Соли Уравнения диссоциации
Уравнения диссоциации Сера. Физические и химические свойства. Нахождение в природе
Сера. Физические и химические свойства. Нахождение в природе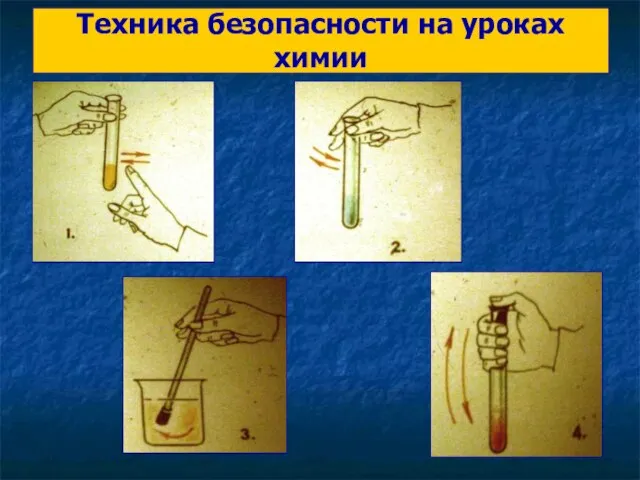 Техника безопасности на уроках химии
Техника безопасности на уроках химии История развития технологий термического крекинга в России и мире
История развития технологий термического крекинга в России и мире Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Вещество и тело. Чистые вещества и смеси
Вещество и тело. Чистые вещества и смеси Минералы
Минералы Газовые смеси. Способы задания газовых смесей. Лекция 5
Газовые смеси. Способы задания газовых смесей. Лекция 5 способы разделения смесей
способы разделения смесей (+)-Plumisclerin A. Плюмисклин А
(+)-Plumisclerin A. Плюмисклин А Растворы полимеров
Растворы полимеров Получение бутандиола, как способ переработки природного газа
Получение бутандиола, как способ переработки природного газа Основной органический синтез
Основной органический синтез