Слайд 2Оксиды азота
N2O NO N2O3 NO2 N2O5
Оксиды азота раздражающе воздействуют на слизистые
оболочки глаз, носа, разрушают легкие человека. Как правило, отравление организма человека NOx проявляется не сразу, а постепенно, причем каких либо нейтрализующих средств нет.
Слайд 4Получение кислот из оксидов азота
N2O3 + H2O = 2HNO2
2NO2 + H2O = HNO2 + HNO3
2NO
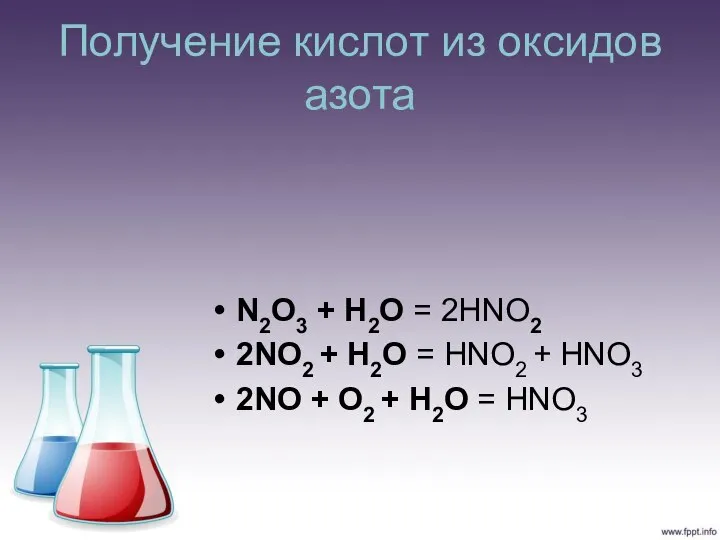
+ O2 + H2O = HNO3
Слайд 5Азотная кислота
Азотная кислота — бесцветная, дымящая на воздухе жидкость, температура плавления −41,59 °C, кипения

+82,6 °C с частичным разложением. Азотная кислота смешивается с водой во всех соотношениях. Водные растворы HNO3 с массовой долей 0,95-0,98 называют «дымящей азотной кислотой», с массовой долей 0,6-0,7 — концентрированной азотной кислотой.
Слайд 6Химические свойства
1. Полная диссоциация в водном растворе (запишите уравнение реакции)
HNO3 ↔ H+ + NO3-
2. Разложение

на оксид азота (IV), кислород и воду
Слайд 7 3. Реакция концентрированной азотной кислоты с металлами
4. Реакция разбавленной азотной кислоты с
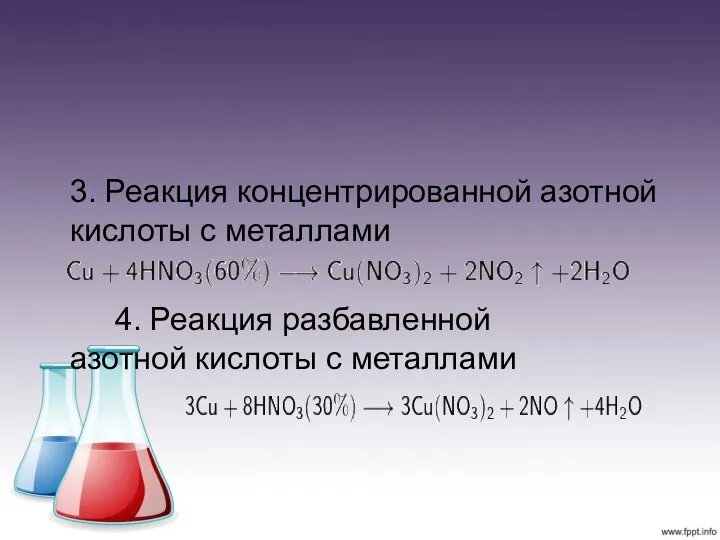
металлами
Слайд 10Самостоятельная работа
1. Причиной возникновения кислотных дождей являются массовые промышленные выбросы диоксида серы

и оксидов азота. Исходя из знаний, полученных на сегодняшнем уроке самостоятельно написать уравнения реакций на листочках.
2. Уравнять методом электронного баланса реакцию разбавленной азотной кислоты с медью.








 Производство серной кислоты
Производство серной кислоты Вода в природе. Состав, свойства и применение воды
Вода в природе. Состав, свойства и применение воды Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Вода. Растворы
Вода. Растворы Закон сохранения массы и химические уравнения
Закон сохранения массы и химические уравнения Соли
Соли Нефть. Способы переработки нефти
Нефть. Способы переработки нефти Металлы побочных подгрупп
Металлы побочных подгрупп Модель химического образования на основе технологического подхода. Методическая система учителя химии
Модель химического образования на основе технологического подхода. Методическая система учителя химии Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Химический элемент кислород
Химический элемент кислород Химическая география чудес природы
Химическая география чудес природы Материаловедение. Методы исследования в материаловедении (лекция 1)
Материаловедение. Методы исследования в материаловедении (лекция 1) Презентация по Химии "Схема получения моноизотопного кремния"
Презентация по Химии "Схема получения моноизотопного кремния"  Посвящение в химики
Посвящение в химики Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты)
Наша стирка по-байкальски. Синтетические моющие средства (СМС¸ детергенты) Презентация на тему Неметаллы, особенности строения
Презентация на тему Неметаллы, особенности строения  Схема монооксигеназной цепи микросом
Схема монооксигеназной цепи микросом Общая характеристика оксидов
Общая характеристика оксидов Серная кислота
Серная кислота Основные понятия химии
Основные понятия химии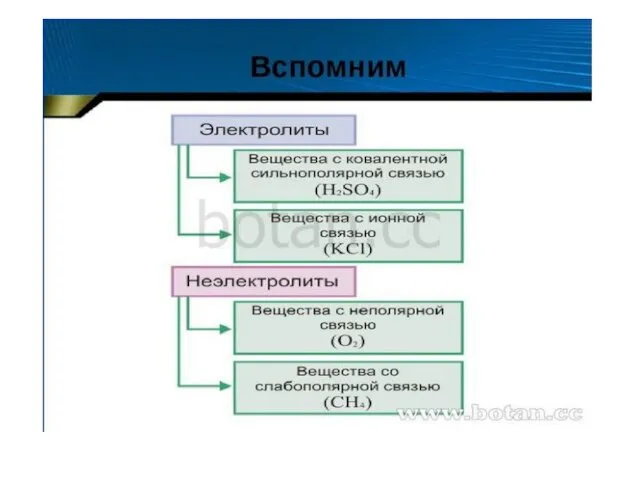 Диссоциация веществ
Диссоциация веществ Химическая связь и ее типы
Химическая связь и ее типы Соли. Химические свойства
Соли. Химические свойства Соль. Добыча соли
Соль. Добыча соли Металлы. Атомы металлов
Металлы. Атомы металлов Природные источники углеводорода
Природные источники углеводорода Кислоты. Кислоты, вокруг нас
Кислоты. Кислоты, вокруг нас