Содержание
- 2. Окислительно –восстановительные реакции ОВР 9класс
- 3. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ (ОВР) – реакции, протекающие с изменением степени окисления. ОВР – реакции, в результате которых
- 4. Два антипода парою ходят, Первый – теряет; второй - находит, Ролью меняясь при этом порой… Кто
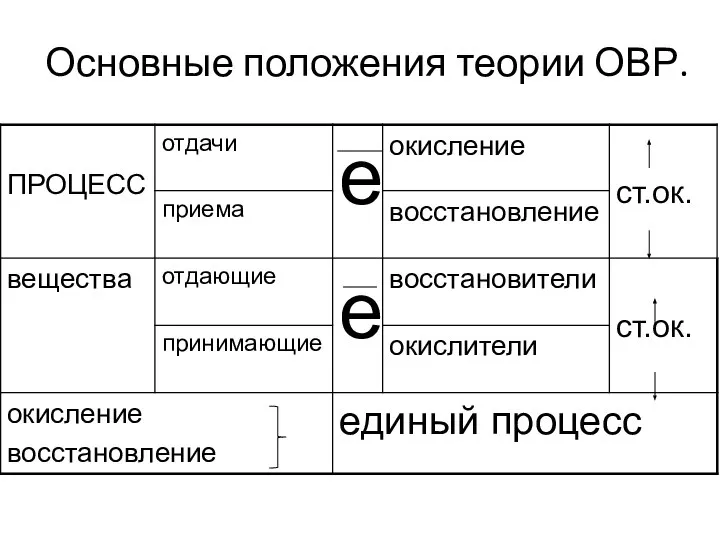
- 5. Основные положения теории ОВР.
- 6. Алгоритм составления ОВР Определить степени окисления элементов в соединениях, участвующих в реакции. Выявить элемент, степень окисления
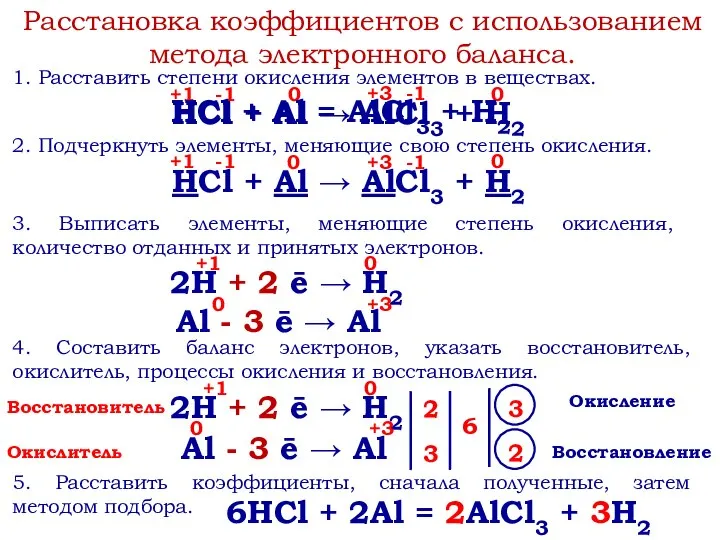
- 7. Расстановка коэффициентов с использованием метода электронного баланса. 1. Расставить степени окисления элементов в веществах. 2. Подчеркнуть
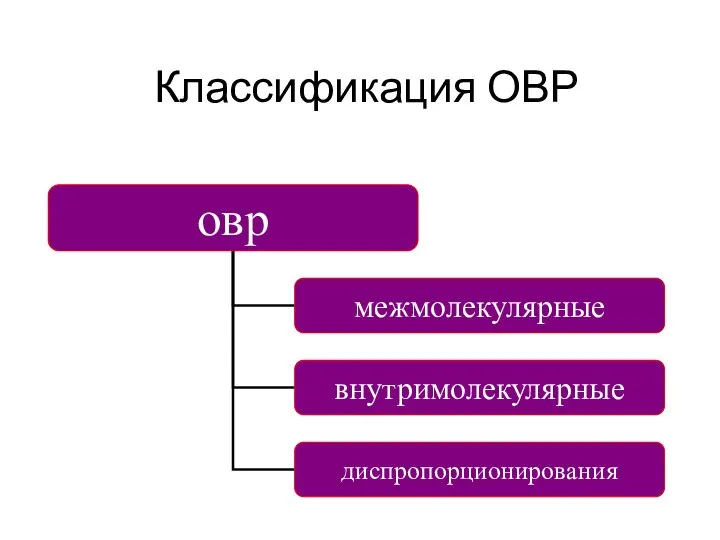
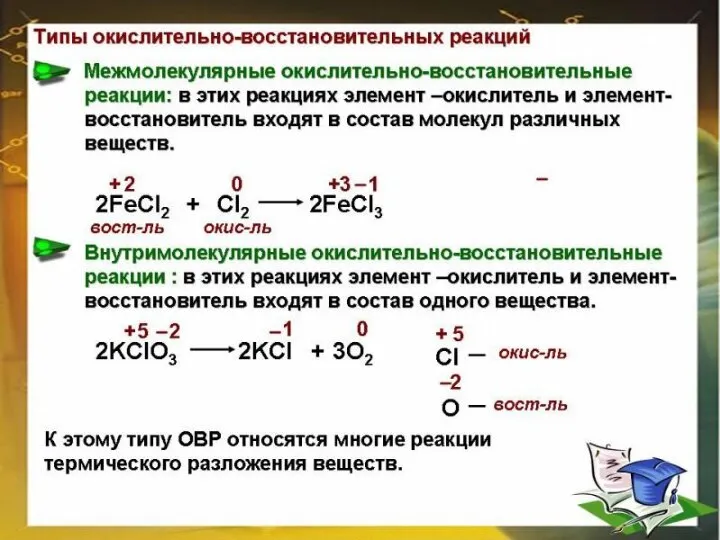
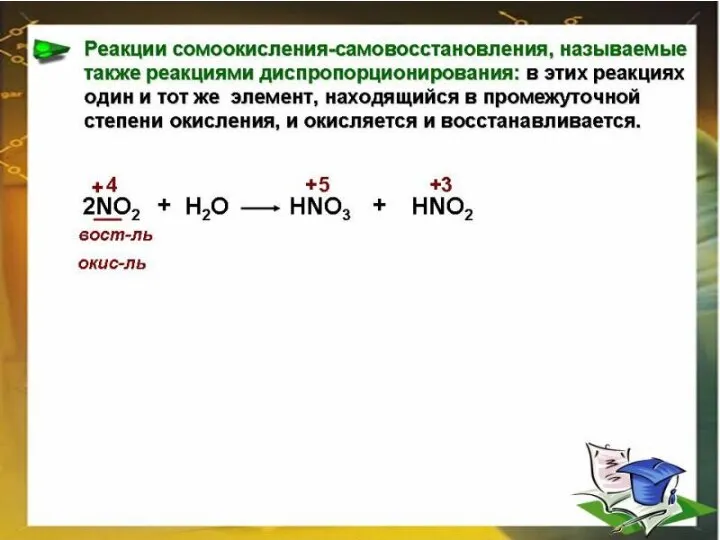
- 8. Классификация ОВР
- 11. Используя метод электронного баланса, преобразуйте схемы в уравнения реакций: а) V2O5 + Al → Al2O3 +
- 12. Т Е С Т Укажите ОВР: а) PH₃ + 2O₂ = H₃PO₄ б) KOH + HCl
- 14. Скачать презентацию






 Образование первичной структуры белка
Образование первичной структуры белка Железо
Железо Катаболизм пуриновых нуклеотидов
Катаболизм пуриновых нуклеотидов Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела
Кристаллическое строение металлов и сплавов. Аморфные и кристаллические тела Сплавы металлов (познавательная презентация)
Сплавы металлов (познавательная презентация) Предмет органической химии. Особенности органических веществ
Предмет органической химии. Особенности органических веществ Отжиг сталей (отжиг 2-го рода) Лекция 2
Отжиг сталей (отжиг 2-го рода) Лекция 2 Металлы II А подгруппы
Металлы II А подгруппы Презентация
Презентация Фосфор - светоносный
Фосфор - светоносный 1662922113131__olk9yp
1662922113131__olk9yp Соединения щелочных металлов
Соединения щелочных металлов Хлор. Химические свойства и применение. Лекция 5
Хлор. Химические свойства и применение. Лекция 5 Сложные неорганические вещества
Сложные неорганические вещества Презентация по Химии "Строение и физические свойства металлов"
Презентация по Химии "Строение и физические свойства металлов"  Основной закон радиоактивного распада и активность радионуклидов
Основной закон радиоактивного распада и активность радионуклидов Контроль качества лекарственных средств, производных аминокислот ароматического ряда. Лекция № 11
Контроль качества лекарственных средств, производных аминокислот ароматического ряда. Лекция № 11 Магматические породы
Магматические породы Строение металлов и их сплавов
Строение металлов и их сплавов Химическое равновесие и способы его смещения
Химическое равновесие и способы его смещения Материальный и тепловой балансы абсорбции
Материальный и тепловой балансы абсорбции Химия и сельское хозяйство
Химия и сельское хозяйство Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов Vielu īpašības
Vielu īpašības Обмен белков и аминокислот. Синтез заменимых аминокислот
Обмен белков и аминокислот. Синтез заменимых аминокислот Молярный объем газов. Закон Авогадро
Молярный объем газов. Закон Авогадро Сульфиты. Виды сульфидов
Сульфиты. Виды сульфидов Нафтены и арены
Нафтены и арены