Содержание
- 2. Повторим!!! Какие соединения мы называем оксидами?. Назовите и запишите общую формулу оксидов. Назвать известные оксиды…. В
- 3. КЛАССИФИКАЦИЯ ОКСИДОВ №1 Несолеобразующие -не взаимодействуют ни с кислотами, ни с щелочами и не образуют солей;
- 4. Классификация оксидов № 2 Основные –это такие оксиды, которым соответствуют основания. Оксиды металлов главных подгрупп 1
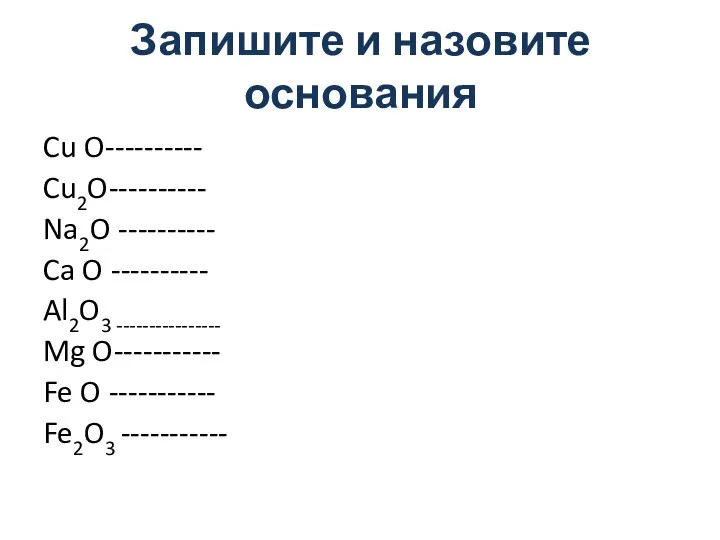
- 5. Запишите и назовите основания Cu O---------- Cu2O---------- Na2O ---------- Ca O ---------- Al2O3 ---------------- Mg O-----------
- 6. Запишите и назовите основания Cu O--------------- Cu (OH)2 Cu2O---------- -----Cu OH Na2O ---------------- Na OH Ca
- 7. Типичные реакции основных оксидов 1.Основный оксид + кислота = соль + вода ? 3Na2O +2H3PO4 =
- 8. Типичные реакции основных оксидов 1.Основный оксид + кислота = соль + вода ( обмена) 3Na2O +2H3PO4
- 9. Классификация оксидов № 2 Кислотные - это такие оксиды, которым соответствуют кислоты. Оксиды неметаллов. Оксиды металлов
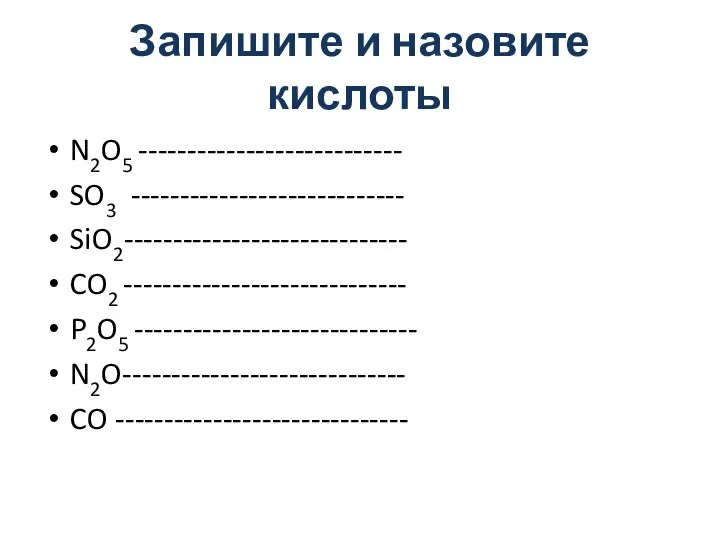
- 10. Запишите и назовите кислоты N2O5 --------------------------- SO3 ---------------------------- SiO2----------------------------- CO2 ----------------------------- P2O5 ----------------------------- N2O----------------------------- CO ------------------------------
- 11. Запишите и назовите кислоты N2O5 -----------------------------HNO3 SO3 -----------------------------H2SO4 SiO2----------------------------- H2SiO3 CO2 ----------------------------- H2CO3 P2O5 -----------------------------H3PO4 N2O-----------------------------
- 12. Типичные реакции кислотных оксидов 1.Кислотный оксид + основание = соль + вода ? SO2 + 2NaOH
- 13. Типичные реакции кислотных оксидов 1.Кислотный оксид + основание = соль + вода (обмена) SO2 + 2NaOH
- 14. Классификация оксидов № 2 Основные –это такие оксиды, которым соответствуют основания. Оксиды металлов главных подгрупп 1
- 16. Скачать презентацию











 Сложные эфиры. Жиры
Сложные эфиры. Жиры Кинетика катодного выделения водорода на дисилициде хрома в щелочном и кислом электролитах
Кинетика катодного выделения водорода на дисилициде хрома в щелочном и кислом электролитах Электролиз расплавов и растворов электролитов
Электролиз расплавов и растворов электролитов Презентация на тему Гормоны
Презентация на тему Гормоны  Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Альдегиды, строение и свойства
Альдегиды, строение и свойства Водородная химическая связь
Водородная химическая связь Природный и попутный газы, их состав и использование
Природный и попутный газы, их состав и использование Описание молекул
Описание молекул Роль металлов в искусстве
Роль металлов в искусстве Диаграмма состояния BaO-Al2O3-SiO2
Диаграмма состояния BaO-Al2O3-SiO2 Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы
Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы Приключение кислорода
Приключение кислорода Презентация на тему Самородки
Презентация на тему Самородки  Мышьяк. Висмут. Сурьма
Мышьяк. Висмут. Сурьма Лекарственные растения содержащие флавоноиды
Лекарственные растения содержащие флавоноиды Алкины. Строение
Алкины. Строение Химия вокруг нас и для нас
Химия вокруг нас и для нас Алюминий
Алюминий Строение, свойства и функции аминокислот и белков
Строение, свойства и функции аминокислот и белков Сода. Что я знаю о ней!?
Сода. Что я знаю о ней!? Равновесия в растворах электролитов. Окислительно-восстановительные реакции
Равновесия в растворах электролитов. Окислительно-восстановительные реакции Кислотные оксиды
Кислотные оксиды Презентация на тему Анализ качества питьевой воды
Презентация на тему Анализ качества питьевой воды  Презентация на тему Алхимики
Презентация на тему Алхимики  Растворение. Экспериментальная работа с веществами
Растворение. Экспериментальная работа с веществами Презентация на тему Основные законы науки химии
Презентация на тему Основные законы науки химии  Химическая связь
Химическая связь