Содержание
- 2. Основаниями называются сложные неорганические соединения состоящие из атома металла и одной или нескольких гидроксильных групп ОН
- 3. Основания Растворимые в воде -ЩЕЛОЧИ NaOH Ba(OH) 2 Нерастворимые Fe(OH) 3 Cu(OH) 2
- 4. Задание: Выпишите формулы оснований К2О, НСl, СuSО4, МgСl2, NaOH Аl203, SO2, НN3, Сu(ОН)2, МgО, SО3, ZnSО4,
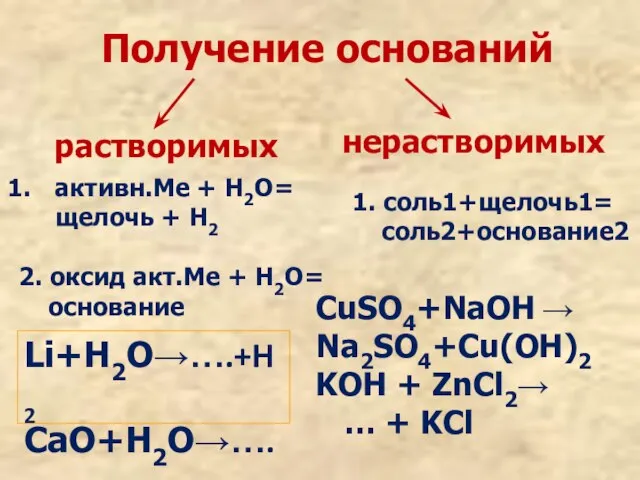
- 5. Получение оснований растворимых нерастворимых активн.Ме + Н2О= щелочь + Н2 2. оксид акт.Ме + Н2О= основание
- 6. Осуществите превращения Na→Na2O→NaOH Cu→CuO→CuCl2→Cu(OH)2
- 7. Решите задачу (р/т с. 94 №5) ω (Mn)= 61,8% ω(O)= 36% ω (H)=2,3% Пусть масса образца
- 8. Вычислите массу гидроксида кальция, который образовался при взаимодействии 11,2г оксида кальция с водой. CaO+H2O=Ca(OH)2
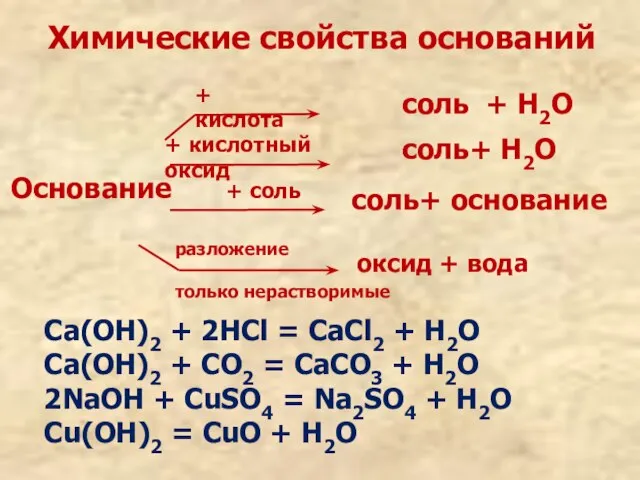
- 9. Химические свойства оснований
- 10. Щёлочи 1.Щёлочи изменяют окраску индикаторов: Лакмус - синий Метилоранж - жёлтый Фенолфталеин - малиновый
- 11. Химические свойства оснований Основание + кислота соль + Н2О + кислотный оксид соль+ Н2О + соль
- 12. 2.Реакция нейтрализации 2NaOH+H2SO4=Na2SO4+2H2O Основание + кислота = соль + вода ! Осторожно ! Едкие вещества !
- 13. 3. с оксидами неметаллов Ca(OH)2+CO2=CaCO3+H2O 4. с солями Ba(OH)2+CuSO4=Cu(OH)2+BaSO4 Щёлочи разъедают кожу, ткани, бумагу. Осторожно! Смыть
- 15. Скачать презентацию










 Презентация на тему Воздух. Кислород. Горение
Презентация на тему Воздух. Кислород. Горение  Альдегиды. Строение молекул
Альдегиды. Строение молекул 8_ANIONY_2_3_angr
8_ANIONY_2_3_angr Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты Реакции по направлению процесса
Реакции по направлению процесса Характеристика щелочных металлов (9 класс)
Характеристика щелочных металлов (9 класс) Калий. Общая информация
Калий. Общая информация Алгебраический метод решения задач В-9 – элемент решения задач С4
Алгебраический метод решения задач В-9 – элемент решения задач С4 Применение серы, хлора, углерода
Применение серы, хлора, углерода Ocena zawartości mikotoksyn w wybranych produktach spożywczych
Ocena zawartości mikotoksyn w wybranych produktach spożywczych Предельные углеводороды. Тест 19
Предельные углеводороды. Тест 19 Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса
Введение в химию. Вещества. Факультатив по химии для учащихся 7 класса Квест Секретная лаборатория. Первоначальные химические понятия. 8 класс
Квест Секретная лаборатория. Первоначальные химические понятия. 8 класс Растворы электролитов
Растворы электролитов Аналитический обзор по теме Процесс разложения аммиака
Аналитический обзор по теме Процесс разложения аммиака О некоторых удивительных удивительных свойствах свойствах веществ
О некоторых удивительных удивительных свойствах свойствах веществ Интерактивный плакат Алканы
Интерактивный плакат Алканы Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Ð¥ÐÐÐЧÐСÐÐÐ Ð ÐÐÐÐÐÐСÐÐ1
Ð¥ÐÐÐЧÐСÐÐÐ Ð ÐÐÐÐÐÐСÐÐ1 prezentatsia_lektsia_1_LF_Rastvory_Kolligativnye_svoi_774_stva_rastvorov_Osmos
prezentatsia_lektsia_1_LF_Rastvory_Kolligativnye_svoi_774_stva_rastvorov_Osmos Набор для выращивания монокристалла. Защита проекта
Набор для выращивания монокристалла. Защита проекта Протолитические буферные системы. Буферные системы организма, их взаимодействие
Протолитические буферные системы. Буферные системы организма, их взаимодействие Использование информационных технологий на уроках химии Радченко Н.В. учитель химии МОУ ПСОШ №3
Использование информационных технологий на уроках химии Радченко Н.В. учитель химии МОУ ПСОШ №3 Методика измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера
Методика измерений массовой концентрации ионов аммония в природных и сточных водах фотометрическим методом с реактивом Несслера Красители для волос. Первая группа
Красители для волос. Первая группа Ионные уравнения
Ионные уравнения Презентация на тему Основные классы неорганических соединений
Презентация на тему Основные классы неорганических соединений  Фосфорні добрива. Технології збагачення фосфоровмісної сировини
Фосфорні добрива. Технології збагачення фосфоровмісної сировини