Содержание
- 2. Основные обозначения m – масса (кг); F – сила (Н); s – площадь (м2); V- объём
- 3. Содержание Основные понятия Физическое тело (тело) – любой отдельно взятый предмет. Рабочее тело – вещество, используемое
- 4. Моль – количество вещества, число структурных частиц которого равно числу атомов, содержащихся в углероде массой 0,012
- 5. Температура – мера средней кинетической энергии молекул. t - температура по термодинамической шкале Цельсия (0С); Т
- 6. Молярная доля компонента смеси х – это величина, равная отношению количества вещества данного компонента к количеству
- 7. или единице, делённой на сумму отношений массовых долей компонентов к их молярным массам. М=1/Σ(ωi/Мi) Закон Дальтона.
- 8. Для газовой смеси по закону Дальтона справедливо: 1) каждый компонент газовой смеси, имеет температуру, равную температуре
- 9. Варианты практической работы №2
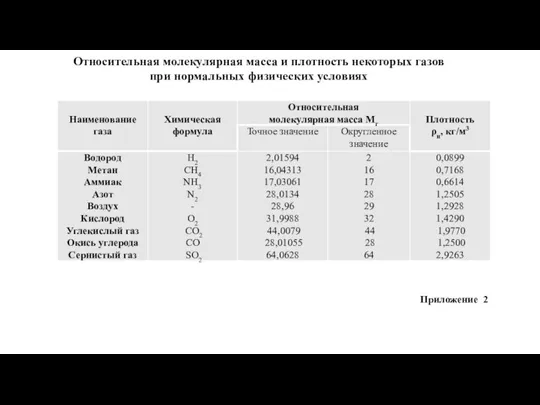
- 11. Относительная молекулярная масса и плотность некоторых газов при нормальных физических условиях Приложение 2
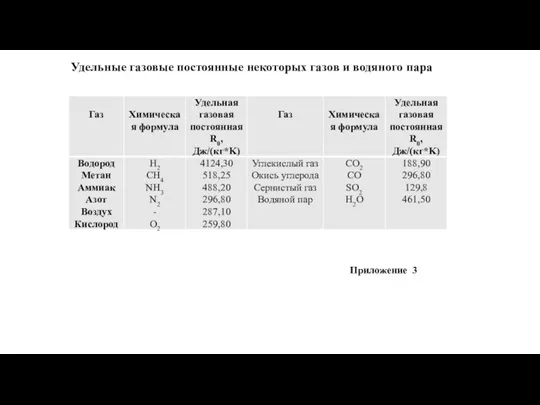
- 12. Удельные газовые постоянные некоторых газов и водяного пара Приложение 3
- 13. Исходные данные. Газ 1 CH4. Газ 2 CО . Приведенный объем V1 V1 =0,2 м3 .
- 14. Контрольное уравнение: х1+х2=0,181+0,819=1 Молярная масса смеси M=x1M1+ x2M2=(0,181·28,01+ 0,819·16,04) ·10-3 =5,29389 + 13,13676 · 10-3 Удельная
- 15. 1) состав смесей переменный 2.Вещества смесей сохраняют свои свойства:( Например:-кислород и водород газы: -кислород поддерживает горение
- 16. 2) Парциальное давление в газовой смеси. Мольная доля газов. Закон Дальтона (закон парциальных давлений). Парциальное давление
- 17. 3)Объeмной долей ri данного газа называется отношение объема, который занимал бы данный газ при температуре и
- 18. 4)В состав воздуха входит несколько различных газов: кислород, азот, углекислый газ, благородные газы, водяные пары и
- 20. Скачать презентацию















 Строение атома
Строение атома Уравнение состояния
Уравнение состояния Общая характеристика металлов
Общая характеристика металлов Углеводороды. Предельные (насыщенные) углеводороды
Углеводороды. Предельные (насыщенные) углеводороды Водород
Водород ОВР в гетерогенных системах
ОВР в гетерогенных системах Каскадный синтез пептидов
Каскадный синтез пептидов Синтез.Малахит
Синтез.Малахит Презентация на тему: Подгруппа азота
Презентация на тему: Подгруппа азота Минералы
Минералы Серная кислота
Серная кислота Сложные эфиры
Сложные эфиры Своя игра. Химия и охрана почв
Своя игра. Химия и охрана почв АЛКИНЫ (ацетиленовые углеводороды)
АЛКИНЫ (ацетиленовые углеводороды) Связь между основными классами неорганических соединений
Связь между основными классами неорганических соединений Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Уравнения химических реакций
Уравнения химических реакций Органическая химия
Органическая химия Исследование физико-химических свойств растворов сахарозы
Исследование физико-химических свойств растворов сахарозы Презентация на тему Фосфор. Соединения фосфора
Презентация на тему Фосфор. Соединения фосфора  Вычисление массовой доли химического элемента в веществе
Вычисление массовой доли химического элемента в веществе Бирюза. Характеристики минерала
Бирюза. Характеристики минерала Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Простые вещества – металлы и неметаллы
Простые вещества – металлы и неметаллы Белки. Структуры белков
Белки. Структуры белков Сложные реакции
Сложные реакции Моделирование состава биоплёночного материала
Моделирование состава биоплёночного материала Химическое равновесие
Химическое равновесие