Содержание
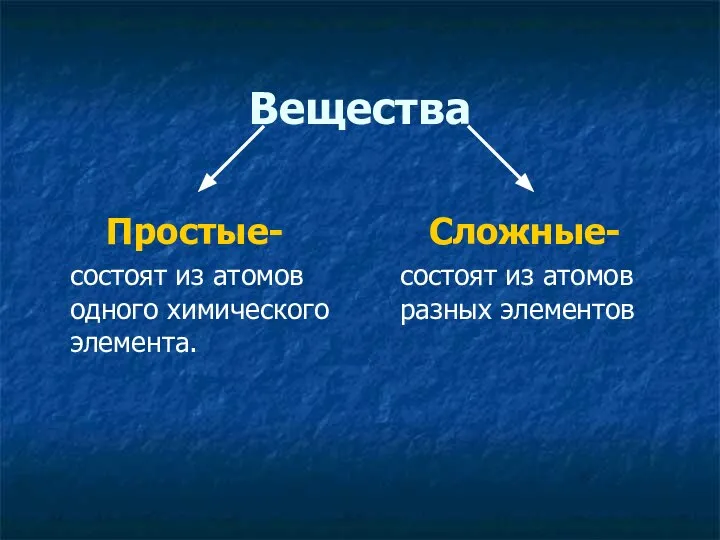
- 2. Вещества Простые- состоят из атомов одного химического элемента. Сложные- состоят из атомов разных элементов
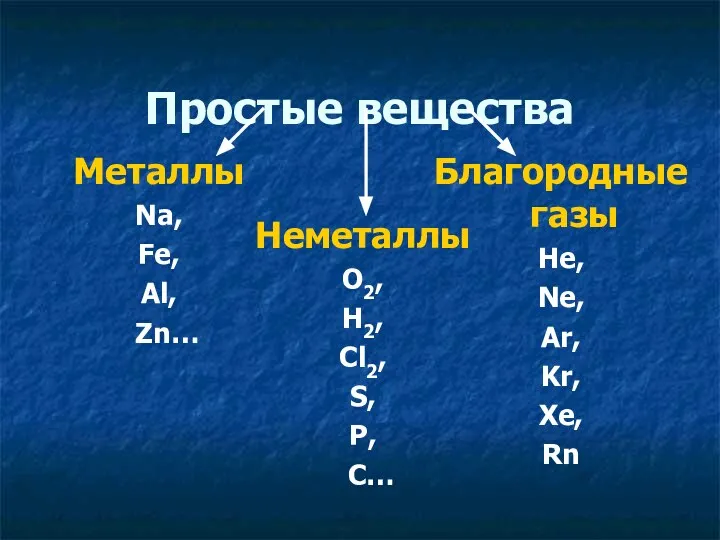
- 3. Благородные газы He, Ne, Ar, Kr, Xe, Rn Простые вещества Металлы Na, Fe, Al, Zn… Неметаллы
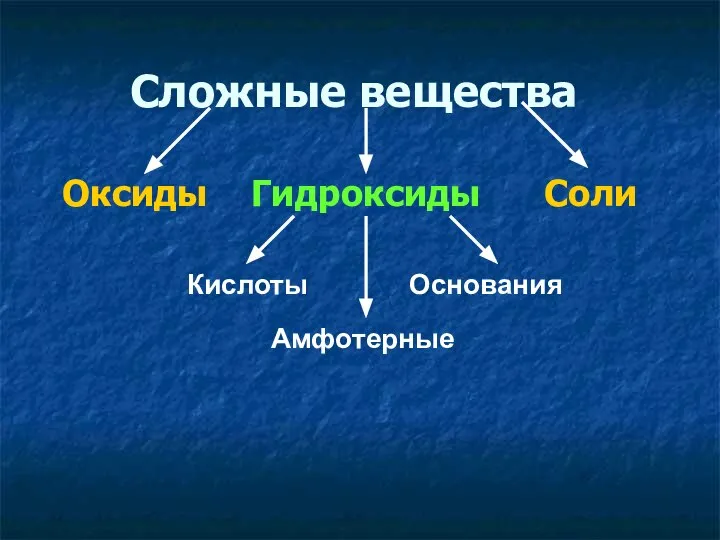
- 4. Сложные вещества Оксиды Гидроксиды Соли Кислоты Основания Амфотерные
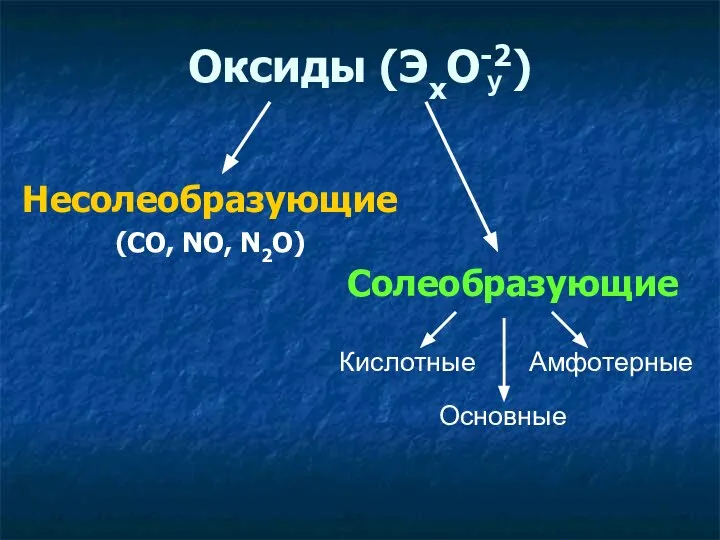
- 5. Несолеобразующие (СO, NO, N2O) Солеобразующие Кислотные Основные Амфотерные Оксиды (ЭхО-2) y
- 6. Кислотные оксиды Оксиды неметаллов: SO2 SO3 CO2 P2O5 SiO2 N2O3 N2O5 Оксиды металлов со степенью окисления
- 7. Основные оксиды- оксиды металлов со степенью окисления +1, +2 Na2O Li2O K2O MgO CaO BaO CrO
- 8. Амфотерные оксиды ZnO Al2O3 Fe2O3 Cr2O3 CuO BeO
- 9. Кислоты (НхR) HCl – соляная HNO3 – азотная HNO2 – азотистая H2SO4 – серная H2SO3 –
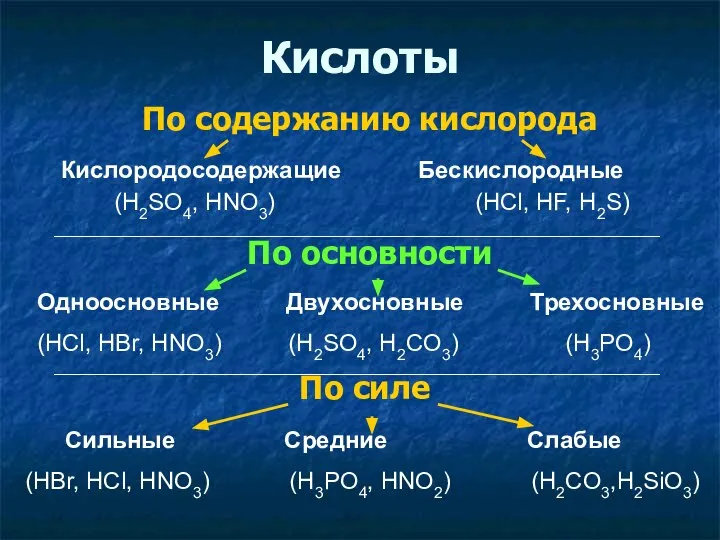
- 10. Кислоты По содержанию кислорода По основности По силе Кислородосодержащие Бескислородные (H2SO4, HNO3) (HCl, HF, H2S) Одноосновные
- 11. Соответствие кислот и оксидов SO2 – H2SO3 SO3 – H2SO4 CO2 – H2CO3 P2O5 – H3PO4
- 12. Основания (Ме(ОН)x) По растворимости в воде По силе Растворимые – щелочи Нерастворимые (NaOH, KOH, Ba(OH)2 )
- 13. Соответствие оснований и оксидов Na2O – NaOH Li2O – LiOH K2O – KOH MgO – Mg(OH)2
- 14. Амфотерные гидроксиды Zn(OH)2 H2ZnO2 Al(OH)3 H3AlO3 HAlO2 Cr(OH)3 HCrO2 Метаалюминиевая кислота Метахромистая кислота
- 16. Скачать презентацию








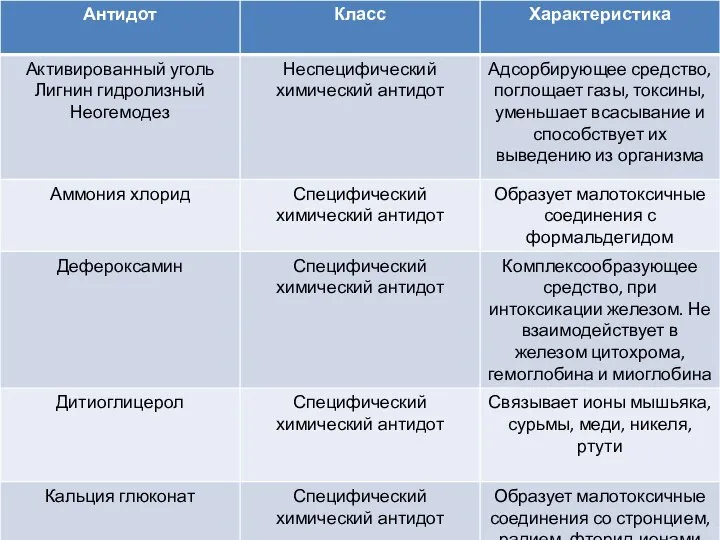 Антидоты. Класс. Характеристика
Антидоты. Класс. Характеристика valentnost
valentnost Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах
Обобщить и систематизировать знания учащихся о кислотах неорганических и органических, о их составе и свойствах Презентации 1 строение атома
Презентации 1 строение атома Наноматеріали. Тіт Лукрецій Кар
Наноматеріали. Тіт Лукрецій Кар Решение задач
Решение задач Bioenergetyka syntezy glutaminy
Bioenergetyka syntezy glutaminy Белки-1 2020
Белки-1 2020 Презентация на тему Коррозия
Презентация на тему Коррозия  Классификация и номенклатура ОС
Классификация и номенклатура ОС Электролитическая диссоциация
Электролитическая диссоциация Изменение химмотологических свойств цетанповышающей присадки в процессе хранения
Изменение химмотологических свойств цетанповышающей присадки в процессе хранения Homecredit Bank. Показатели и зоны роста
Homecredit Bank. Показатели и зоны роста Типы кристаллических решёток
Типы кристаллических решёток Алюминий
Алюминий Натрий, свойства атома, химические и физические свойства
Натрий, свойства атома, химические и физические свойства Определение Кофеина в Кофе
Определение Кофеина в Кофе Углеводороды. Алканы
Углеводороды. Алканы Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН
Изучение адсорбции аминокислот на поверхности гидроксилапатита при варьировании рН Каучук негізіндегі материалдар
Каучук негізіндегі материалдар минералы_4_блеск
минералы_4_блеск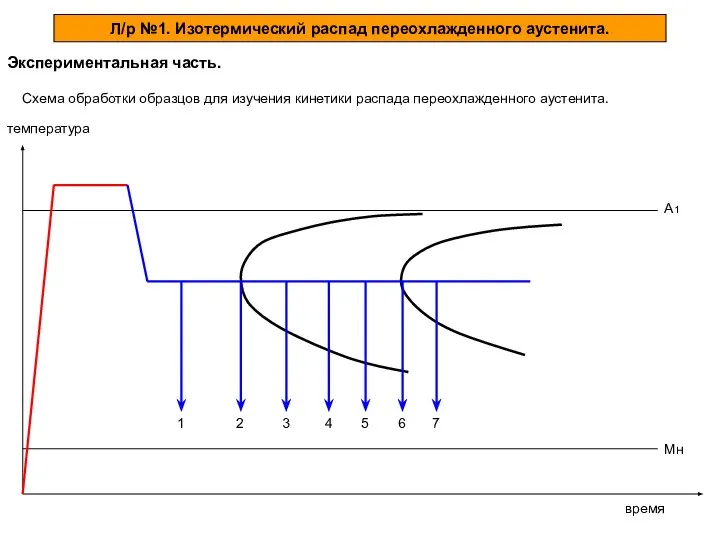 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Скорость протекания химических реакций
Скорость протекания химических реакций Составление формул по валентности. Понятие
Составление формул по валентности. Понятие Презентация на тему Гидролиз солей
Презентация на тему Гидролиз солей  Металлы
Металлы Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5
Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5 Вода-растворитель. Растворы
Вода-растворитель. Растворы