Слайд 2Лекция №7
Основные положения
качественного анализа
Дисциплина: «Физико- химические методы исследований и техника лабораторных

работ»
1 курс 2 семестр
Слайд 31. Классификация
методов аналитической химии
Аналитическая химия– наука о методах идентификации и определения

химического состава веществ и материалов и их химической структуры.
Слайд 4В зависимости от измеряемого свойства вещества применяют следующие методы:
Химические- проведение химических

реакций (гравиметрический и титриметрические методы)
Физико-химические- измерение каких-либо физических параметров химической системы, (величины потенциалов, оптических плотностей и т.д.)
Физические- состав вещества устанавливается изменением физических свойств объекта (плотности, вязкости, интенсивности излучения и т.д.).
В зависимости от аналитической задачи различают качественный и количественный анализ.
Слайд 52. Понятие о качественном анализе
Цель проведения- определение качественного состава вещества (из каких

элементов или ионов состоит вещество).
Для этого необходимо изучить свойства:
вещества как такового:
- физическое состояние (твёрдое, жидкость, газ)
- структура его в твердом состоянии (аморфное или кристаллическое вещество),
- цвет, запах, вкус и др.
вещества в химических превращениях в какое-либо новое с ясно выраженными характерными свойствами;
Слайд 6Химические реакции, применяемые в качественном анализе, называются качественными.
Проводят в пробирках, капельным путем

или под микроскопом (микрокристаллоскопические реакции).
Проводят «сухим» или «мокрым» путем (в раство-рах).
Слайд 72.1. Сухой путь анализа
Реакции, проводимые сухим путем (не в растворах), применяются как

вспомогательные, при предваритель-ном испытании.
Важнейшие реакции «сухой химии:
способность окрашивать несветящееся пламя газовой горелки:
- пробу на петле платиновой проволоки вносят в пламя горелки.
- образец окрашивает пламя в определенный цвет (например, ионы калия- в фиолетовый, ионы меди – в зеленый и т. д.)
Слайд 8летучесть при нагревании (разложением или возгонкой):
- пробу нагревают в пробирном цилиндре или

в запаянной с одного конца стеклянной трубочке
- летучие вещества превращаются в пары, которые затем конденсируются в более холодной части
способность к образованию «перлов»:
- при сплавлении вещества с тетраборатом натрия (бурой), в петле платиновой проволоки образуются стекловидные шарики- «перлы», имеющие определенный цвет (например, ионы хрома окрашивают «перлы» в зеленый цвет).
Слайд 92.2. «Мокрый путь» анализа
Анализ вещества, проводимый в растворах.
Это основной путь полного определения

состава вещества.
Исследуемое вещество должно переводится в раствор (растворитель- дистиллированная вода, кислоты - HCl, HNO3 и др.)
Слайд 10Не все химические реакции пригодны для качественного анализа.
Требования, предъявляемые к проводимой качественной

реакции:
1. Должна сопровождаться внешними изменения-ми:
изменение окраски раствора- цветные реакции
выпадение нерастворимого в воде осадка- осадочные
образование кристаллов определенной формы- микро-кристаллоскопические,
специфический запах, выделение газов- газообразую-щие.
Слайд 112. Должна протекать быстро и быть простой по выполнению.
3. Реакция должна быть:
-

специфична для данного иона- чем меньшее количество ионов вступает в реакцию с данным реактивом, тем более специфична данная реакция
- чувствительна- чем меньшее количество вещества может быть определено с помощью данного реактива, тем более чувствительна эта реакция.
Слайд 12Вещества, с помощью которых выполняется открытие ионов, называются реактивами на соответст-вующие ионы.

Реакции, характерные для какого-либо иона, назы-ваются частными реакциями этого иона.
Выполнение качественной реакции требует соблюдения определенных условий ее проведения:
1) концентрация реагирующих веществ- при выполнении частной качественной реакции добавляют избыток реактива
Слайд 132) среда раствора- реактив образует с данным ионом осадок или окрашивание в

строго определенной среде
3) соблюдение определённых температурных условий:
- труднорастворимые соли, выпадают в осадок только при охлаждении;
- некоторые реакции необходимо проводить при нагревании, так как на холоде они протекают слишком медленно, а иногда и в другом направлении;
- при проведении реакций сухим путем, окрашивание пламени в характерный для данного иона цвет удается лишь при нагревании в определенной части пламени.
Слайд 14Методы «мокрой химии» обладают относительно низкой точностью, не требуют высокой квалификации, почти

полностью вытеснены современными инструментальными физико- химическими методами (оптическими, хроматографическими и др. методами).
Слайд 153. Порядок проведения качественного химического анализа
При проведении качественного анализа, необходимо определить не

только какие элементы входят в состав данного вещества, но и, примерно, в каких количествах они находятся.
Слайд 16Для этого необходимо:
всегда брать на исследование определённое количества анализируемого вещества (около 0,5-

1 грамм) и при проведении анализа сравнивать величину отдельных осадков между собой
применять растворы определенной концентрации (нормальные (1н), полунормальные (0,5 н), в одну десятую нормального (0,1 н)).
Слайд 17Качественный химический анализ проводится в 3 этапа:
1) предварительное испытание
2) открытие металлов (катионов)
3)
открытие неметаллов (металлоидов) или кислот (анионов).
Слайд 18Особенности проведения качественного анализа в зависимости от вида анализируемых веществ:
1. Твердое неметаллическое

вещество:
1) производится внешний осмотр, микроскопическое исследование и предварительное испытание методами «сухого анализа»
2) проба растворяется в растворителях
Вещества, не растворяющиеся в растворителе, пере-водятся в раствор некоторыми специальными приемами:
сплавлением с содой,
кипячением с раствором соды,
нагреванием с некоторыми кислотами и др.
Слайд 19Полученный раствор подвергается систематическому анализу с предварительным выделением металлов и кислот по

группам и дальнейшим разделением их на отдельные элементы, пользуясь свойственными им частными реакциями.
Слайд 202. Твердое вещество в виде металла или сплава металлов:
1) проба металла растворяется

в азотной кислоте
2) полученный раствор выпаривается досуха
3) твёрдый остаток растворяется в воде и подвергается систематическому анализу.
Слайд 213. Жидкость (раствор).
1) определяется его цвет, запах и реакцию на лакмус

(кислотная, щелочная, нейтральная).
2) небольшую порцию жидкости выпаривают на платиновой пластинке или часовом стекле, чтобы удостовериться в присутствии в растворе каких-либо твёрдых веществ
После этих предварительных испытаний жидкость анализируется обычными методами.
4.Газ.
Производится различными специальными методами.
Слайд 22Итак, результат качественного химического анализа- принятие решения о наличии или отсутствии искомого

компонента в веществе.
Если необходимо определить количество искомого компонента в общем объёме вещества, далее проводят качественный анализ.





















 Презентация на тему Подготовка к ЕГЭ. Полезно знать
Презентация на тему Подготовка к ЕГЭ. Полезно знать  Лаборатория гидрометаллургических процессов
Лаборатория гидрометаллургических процессов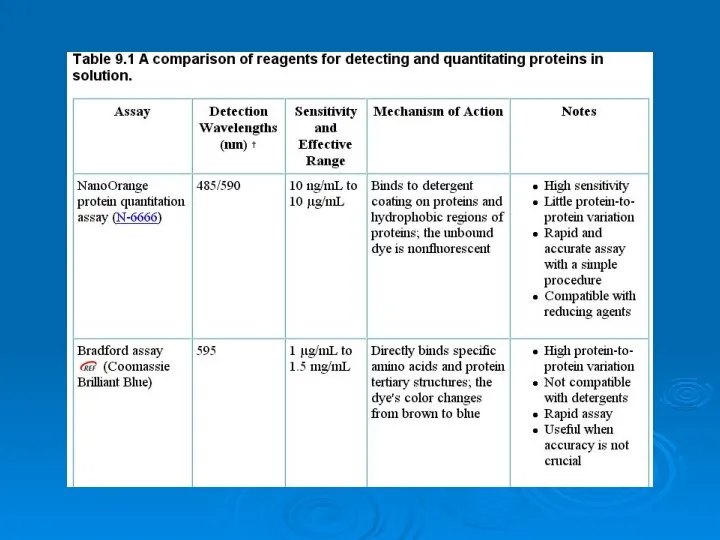 Analysis of proteins
Analysis of proteins Относительный вклад % буферных систем крови в поддержание в ней протолитического гомеостаза
Относительный вклад % буферных систем крови в поддержание в ней протолитического гомеостаза Фенол
Фенол Альдегиды, гомология, изомерия, номенклатура
Альдегиды, гомология, изомерия, номенклатура Вещество и тело. Чистые вещества и смеси
Вещество и тело. Чистые вещества и смеси Кремнийорганические каучуки
Кремнийорганические каучуки Удивительные кристаллы Выполнена учеником 8 а класса Савиным Анатолием Учитель: Звёздочкина С.А.
Удивительные кристаллы Выполнена учеником 8 а класса Савиным Анатолием Учитель: Звёздочкина С.А. Конструирование макромолекул методом ATRP
Конструирование макромолекул методом ATRP Генетич_связь_Проявление_периодического_закона
Генетич_связь_Проявление_периодического_закона Растворы. Типы растворов. Способы выражения концентрации растворов
Растворы. Типы растворов. Способы выражения концентрации растворов Тепловой эффект
Тепловой эффект Алкины. Строение алкинов
Алкины. Строение алкинов Презентация на тему Водородная связь (11 класс)
Презентация на тему Водородная связь (11 класс)  Карбонильные соединения
Карбонильные соединения Основные понятия химии
Основные понятия химии Транспорт веществ
Транспорт веществ Техника безопасности на уроках химии
Техника безопасности на уроках химии Образование химических связей
Образование химических связей Валентность
Валентность Kyseliny. Vlastnosti
Kyseliny. Vlastnosti Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5
Адсорбция. Механизмы адсорбции. Термодинамика адсорбции. Лекция 5 Пластмассы. Классификация
Пластмассы. Классификация Окислительные свойства концентрированной серной кислоты
Окислительные свойства концентрированной серной кислоты Дисперсные системы с твёрдой средой и газообразной фазой
Дисперсные системы с твёрдой средой и газообразной фазой Натуральный каучук
Натуральный каучук Электрохимия. Экзаменационные вопросы
Электрохимия. Экзаменационные вопросы