Содержание
- 2. ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ, ПРОТЕКАЮЩИЕ НА ЭЛЕКТРОДАХ ПРИ ПРОПУСКАНИИ ПОСТОЯННОГО ЭЛЕКТРИЧЕСКОГО ТОКА ЧЕРЕЗ РАСТВОРЫ ИЛИ РАСПЛАВЫ ЭЛЕКТРОЛИТОВ, НАЗЫВАЮТ
- 3. ЭЛЕКТРОЛИЗ ВОДНЫХ РАСТВОРОВ ЭЛЕКТРОЛИТОВ Катодные процессы в водных растворах электролитов :катионы или молекулы воды принимают электронов
- 4. Cu2+ + 2e– = Cu0, E0=0,337 В 2H2O + 2e– = H2 + 2OH–, E0=–0,83 В
- 5. 2. Катионы металлов с малой величиной стандартного электродного потенциала (катионы металлов начала ряда напряжений Li+, Na+,
- 6. 3. Катионы металлов со стандартным электродным потенциалом меньшим, чем у ВОДОРОДА, но большим, чем у алюминия
- 7. 4. На катоде легче всего разряжаются катионы того металла, которому отвечает наиболее положительный потенциал. Так, например,
- 8. АНОДНЫЕ ПРОЦЕССЫ На аноде происходит окисление анионов или молекул воды ( частицы отдают электронов - окисляются)
- 9. НА АНОДЕ ОКИСЛЯЮТСЯ АНИОНЫ БЕСКИСЛОРОДНЫХ КИСЛОТ, OH– ИЛИ МОЛЕКУЛЫ ВОДЫ 2Cl– – 2e– = Cl2 2H2O
- 10. ПРАВИЛА ПРОЦЕССОВ ЭЛЕКТРОЛИЗА При электролизе водного раствора соли из активного металла и кислородосодержащей кислоты на катоде
- 11. При электролизе раствора соли из активного металла и бескислородной кислоты на катоде образуется - Н2, на
- 12. ПРАВИЛА ПРОЦЕССОВ ЭЛЕКТРОЛИЗА При электролизе водного раствора соли из малоактивного металла и кислородосодержащей кислоты на катоде
- 13. ПРАВИЛА ПРОЦЕССОВ ЭЛЕКТРОЛИЗА При электролизе катиона аммония NH4+ восстанавливается вода. При электролизе солей органических кислот на
- 14. ПРАВИЛА ПРОЦЕССОВ ЭЛЕКТРОЛИЗА Электролиз раствора щелочи – это электролиз воды. Электролиз раствора кислородосодержащей кислоты – это
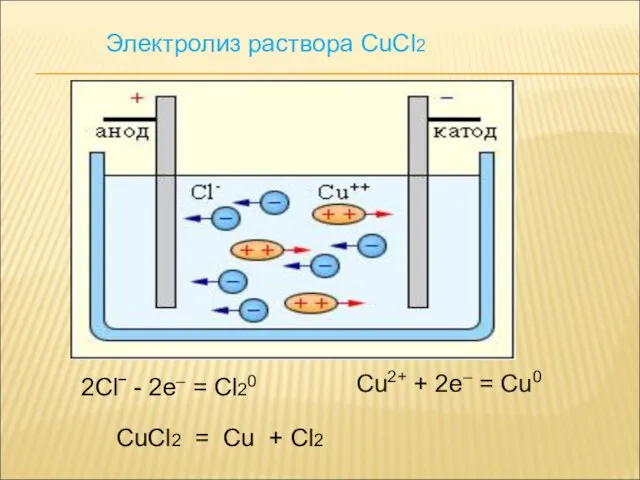
- 16. Электролиз раствора CuCl2 2Clˉ - 2e– = Cl20 Cu2+ + 2e– = Cu0 CuCl2 = Cu
- 18. Скачать презентацию














 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)