Слайд 21) Горение
При сжигании на воздухе алкены образуют углекислый газ и воду.

C2 H4 + 3O2 → 2CO2 + 2H2O + Q
Алкены применяют в качестве топлива и как добавку к топливу.
Слайд 3 2) Окисление
(растворы окислителей обесцвечиваются)
H2C=CH2 + [О] + НОН → CH2−CH2
![2) Окисление (растворы окислителей обесцвечиваются) H2C=CH2 + [О] + НОН → CH2−CH2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1141231/slide-2.jpg)
этилен
| | OH OH
этиленгликоль
Этиленгликоль идет на производство антифризов и тормозных жидкостей.
Слайд 43) Реакции присоединения.
а) Галогенирование. Алкены при обычных условиях присоединяют галогены.
Реакция

бромирования
С2Н4 + Br2 → С2Н4 Br2 дибромэтан
Дибромэтан - антидетонационная добавка в топливо и применяется для обработки бревен от термитов и жуков
Слайд 5 Реакция хлорирования
С2Н4 + CI2 → С2Н4 CI2 дихлорэтан
Дихлорэтан применяют как растворитель

и для обеззараживания зернохранилищ от вредителей
Слайд 6 б) Гидрирование. Алкены легко присоединяют водород в присутствии катализаторов (Pt, Pd, Ni)

образуя предельные углеводороды.
С2Н4 + H2 → C2 H6 этан
Алканы применяют в качестве топлива, для получения растворителей, хладагентов и многого другого.
Слайд 7в) Гидрогалогенирование.
С2Н4 + HCI → C2 H5 CI хлорэтан
С2Н4 + HBr →

C2 H5 Br бромэтан
Хлорэтан и бромэтан применяют для наркоза при легких операциях.
Слайд 8г) Гидратация – присоединение воды
С2Н4 + НОН → С2Н5ОН
этиловый

спирт
(этанол)
Этиловый спирт применяют как растворитель, антисептик в медицине, для производства синтетического каучука.
Слайд 94. Реакция полимеризации
n CH2 = CH2 → (- CH2 – CH2 -)n

ЭТИЛЕН ПОЛИЭТИЛЕН
Полиэтилен применяется для получения пленки, тары, труб, сантехники, изоляции проводов, каркасов катушек, бронепанелей в бронежилетах, предметов быта, игрушек, канцелярских товаров и многого другого.

![2) Окисление (растворы окислителей обесцвечиваются) H2C=CH2 + [О] + НОН → CH2−CH2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1141231/slide-2.jpg)






 Электронное и пространственное строение молекулы метана Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ол
Электронное и пространственное строение молекулы метана Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ол Презентация на тему Лекарства
Презентация на тему Лекарства  Презентация в 8 классе к уроку по химии на тему__
Презентация в 8 классе к уроку по химии на тему__ Металлы и их соединения
Металлы и их соединения Органическая химия
Органическая химия Лабораторно-практическое занятие № 5. Неметаллические материалы
Лабораторно-практическое занятие № 5. Неметаллические материалы Основания и их свойства
Основания и их свойства Аммиак
Аммиак Кислоты в химии
Кислоты в химии Химические свойства оснований
Химические свойства оснований Железо как химический элемент
Железо как химический элемент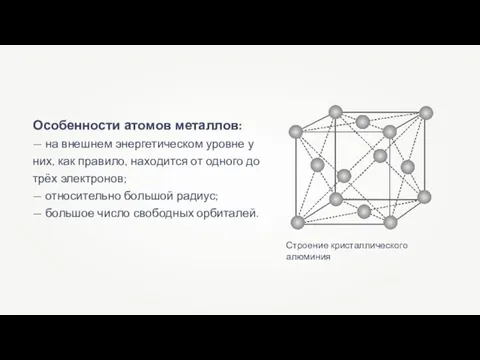 Металлическая химическая связь
Металлическая химическая связь Физическая химия растворов электролитов
Физическая химия растворов электролитов Окисники, відновники
Окисники, відновники Валентность
Валентность Сплавы, растворы, смеси
Сплавы, растворы, смеси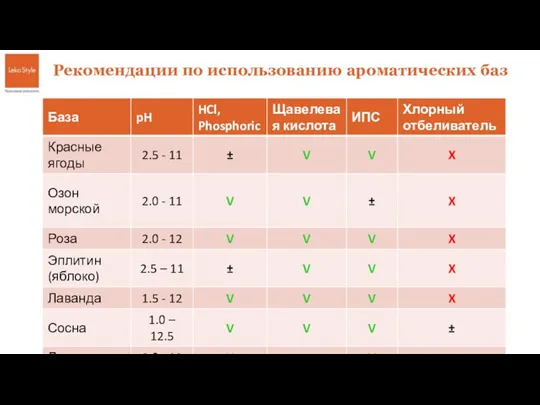 Базы для кислых и щелочных сред
Базы для кислых и щелочных сред Экстракция
Экстракция Презентация на тему Мусор
Презентация на тему Мусор  Химия и география. Викторина
Химия и география. Викторина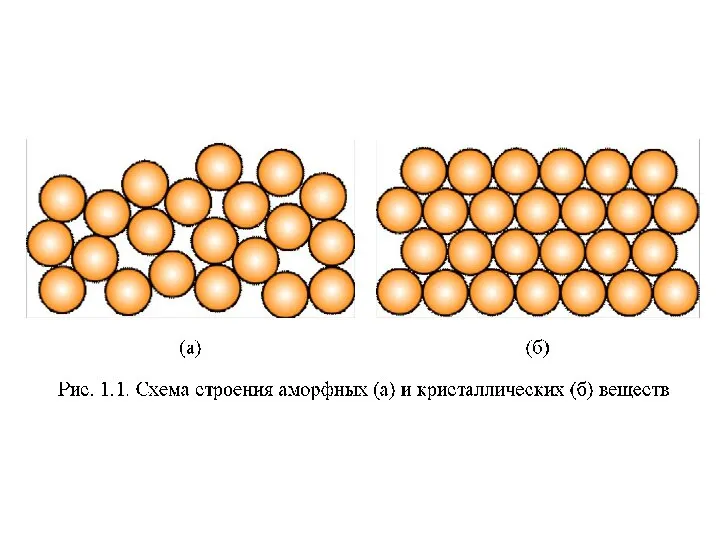 Материаловедение
Материаловедение Сероводород, сульфиды
Сероводород, сульфиды Пептиды, белки. Лабораторное занятие
Пептиды, белки. Лабораторное занятие Алкены
Алкены Получение и применение аренов
Получение и применение аренов Волокна
Волокна Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания
Электролитическая диссоциация веществ Реакции ионного обмена и условия их протекания Презентация на тему Химические свойства и применение алканов
Презентация на тему Химические свойства и применение алканов