Содержание
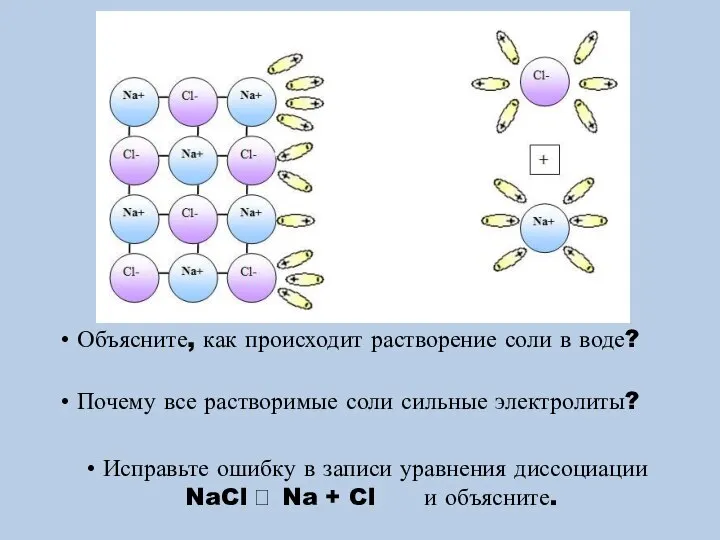
- 2. Объясните, как происходит растворение соли в воде? Почему все растворимые соли сильные электролиты? Исправьте ошибку в
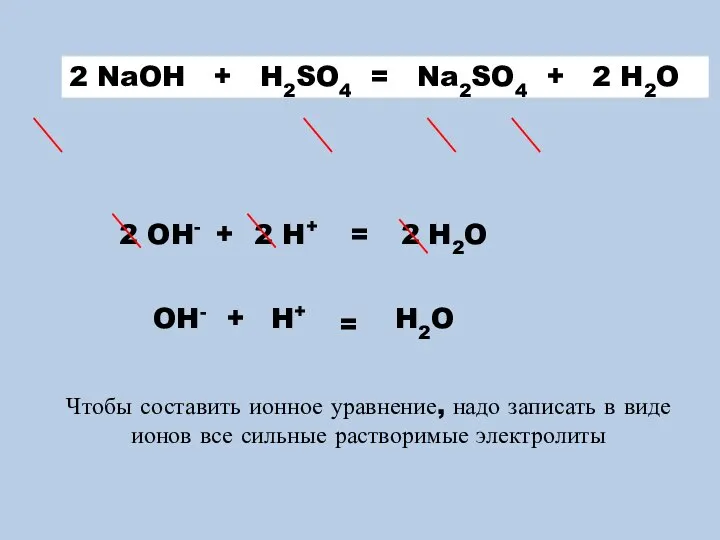
- 3. + 2 H2O = 2 Na++ SO42- 2 H++SO42- + 2 OH- + 2 Na+ 2
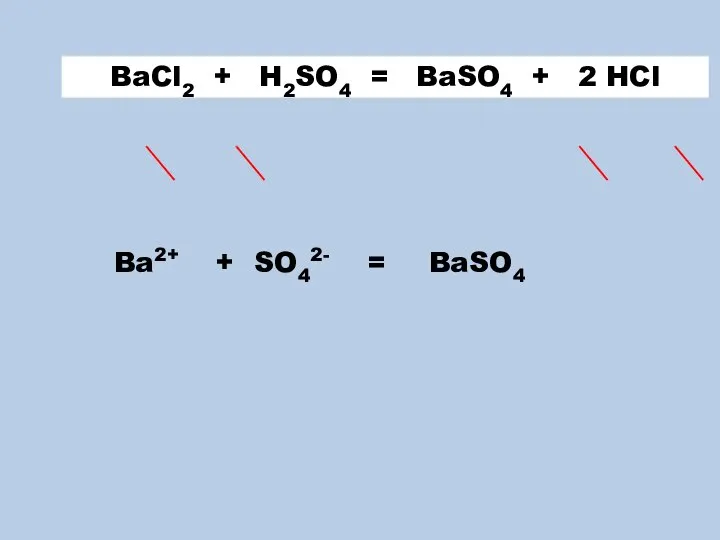
- 4. + 2 H++2 Cl- = Ba SO4 2 H++SO42- + 2 Cl- + Ba2+ BaCl2 +
- 5. Как составить ионное уравнение? Какие вещества нельзя расписывать на ионы? Надо ли записывать в виде ионов:
- 7. Скачать презентацию

 Получение меди
Получение меди Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла lll-l группы главные подгруппы. 11 класс
lll-l группы главные подгруппы. 11 класс Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9
Топология кристаллических структур. Топологические типы. Программы и базы данных для анализа топологии. Лекция 9 10_KhimiaKlassifikatsia_organicheskikh_soedieniy (1)
10_KhimiaKlassifikatsia_organicheskikh_soedieniy (1) Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов
Бензилиденкетоны в синтезе замещённых бензимидазолопиримидинов Презентация на тему Основания 8 класс
Презентация на тему Основания 8 класс  Основания
Основания Создание учебно-методических материалов по химии в современной форме (презентации уроков)
Создание учебно-методических материалов по химии в современной форме (презентации уроков) Определение формул органических веществ
Определение формул органических веществ Характеристика элемента по положению в таблице Д.И.Менделеева
Характеристика элемента по положению в таблице Д.И.Менделеева Веселый химический КВН
Веселый химический КВН Сферы применения CaCO3
Сферы применения CaCO3 Подготовка к контрольной работе химические реакции 8 класс
Подготовка к контрольной работе химические реакции 8 класс Виды металлов, сплавы металлов, применение в промышленности и в быту
Виды металлов, сплавы металлов, применение в промышленности и в быту Средства для борьбы с бытовыми насекомыми
Средства для борьбы с бытовыми насекомыми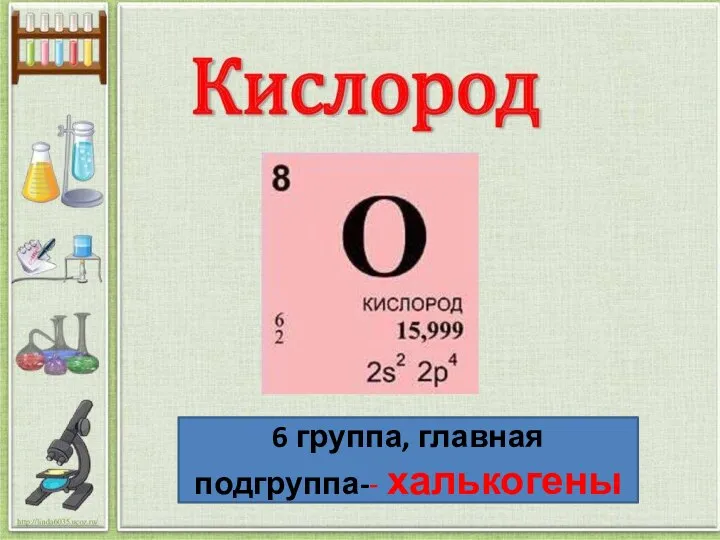 Кислород. Общая характеристика подгруппы на примере кислорода и серы
Кислород. Общая характеристика подгруппы на примере кислорода и серы Полимеры. Полиэтилен
Полимеры. Полиэтилен Презентация на тему Нефть. Переработка нефти
Презентация на тему Нефть. Переработка нефти  Свойства радиоактивных элементов
Свойства радиоактивных элементов Проектная деятельность учащихся по химии
Проектная деятельность учащихся по химии Физико-химия поверхностных явлений в функционировании живых систем
Физико-химия поверхностных явлений в функционировании живых систем Алкины
Алкины Химическая реакция в потоке в одномерном случае. Уравнение неразрывности
Химическая реакция в потоке в одномерном случае. Уравнение неразрывности Атомные спектры
Атомные спектры Литий
Литий Новейшие достижения в области высокомолекулярных соединений
Новейшие достижения в области высокомолекулярных соединений Хроматография
Хроматография