Слайд 2План:
Понятие о химическом равновесии.
Факторы, влияющие на смещение химического равновесия. Принцип Ле Шателье.
Смещение

химического равновесия (Пример).
Слайд 3Химическое равновесие
Когда скорость прямой реакции, равна скорости обратной реакции наступает химическое равновесие.
υпрям.р-ии=
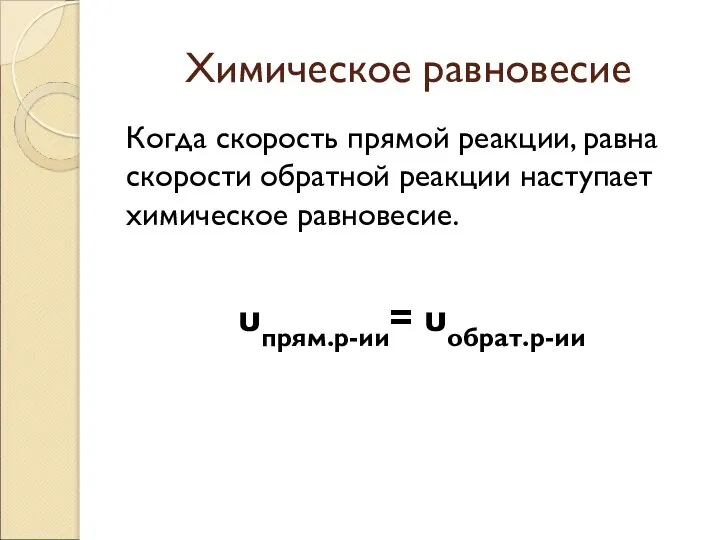
υобрат.р-ии
Слайд 4Анри Луи Ле Шателье (1850–1936)
Принцип
Ле Шателье (принцип смещения химического равновесия или принцип

противоложностей).
Был высказана в общем виде в 1884 году французским ученым Ле Шателье
Слайд 5ПРИНЦИП ЛЕ-ШАТЕЛЬЕ
Если на систему, находящуюся в равновесии оказывается воздействие (изменяется концентрация, давление,

температура), то равновесие смещается в ту сторону, которая ослабляет данное воздействие.
Слайд 6Факторы,
влияющие на смещение химического равновесия
Слайд 7
При повышении концентрации продуктов реакции или исходных веществ ( С ↑
), равновесие смещается в сторону их расходования.
При понижении концентрации продуктов реакции или исходных веществ ( С↓), равновесие смещается в сторону их образования.
Слайд 8Влияние изменения температуры
1. При повышении температуры (Т ↑ ) равновесие смещается в

сторону эндотермической реакции (- Q ).
2NH3 → N2 + 3H2 - Q
2. При понижении температуры (Т ↓ ) равновесие смещается в сторону экзотермической реакции (+ Q).
N2 + 3H2 → 2NH3 + Q
Слайд 9При повышении давления (Р ↑), равновесие смещается в сторону меньшего объема.
N2 (газ)
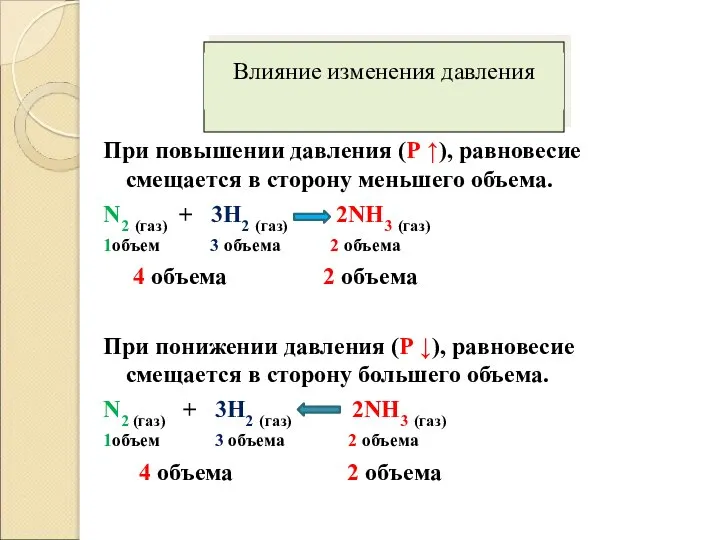
+ 3H2 (газ) 2NH3 (газ)
1объем 3 объема 2 объема
4 объема 2 объема
При понижении давления (Р ↓), равновесие смещается в сторону большего объема.
N2 (газ) + 3H2 (газ) 2NH3 (газ)
1объем 3 объема 2 объема
4 объема 2 объема
Слайд 10
ВЛИЯНИЕ КАТАЛИЗАТОРОВ НА РАВНОВЕСИЕ
КАТАЛИЗАТОРЫ В РАВНОЙ СТЕПЕНИ УСКОРЯЮТ И

ПРЯМУЮ И ОБРАТНУЮ , ИЗМЕНЯЯ ЭНЕРГИЮ АКТИВАЦИИ И ТОЙ И ДРУГОЙ НА ОДНУ И ТУЖЕ ВЕЛИЧИНУ.









 Спирты. Тест
Спирты. Тест Металлы. Общие свойства
Металлы. Общие свойства Презентация на тему Химические свойства алкенов
Презентация на тему Химические свойства алкенов  Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия
Презентация на тему Алкадиены: строение, номенклатура, гомологи, изомерия  Химия цвета
Химия цвета Зола. Свойства щёлока
Зола. Свойства щёлока Вещества в окружающей природе и в технике
Вещества в окружающей природе и в технике Относительная атомная масса элементов
Относительная атомная масса элементов Известняк. Разновидности известняка. Области применения
Известняк. Разновидности известняка. Области применения Полимерные материалы
Полимерные материалы Аммиак. Состав вещества
Аммиак. Состав вещества Подгруппа алюминия
Подгруппа алюминия Углеводороды
Углеводороды Опыты по теме Свойства основных классов неорганических соединений
Опыты по теме Свойства основных классов неорганических соединений Атомы, молекулы и ионы
Атомы, молекулы и ионы Алмазы
Алмазы Альдегиды, их химические и физические свойства. Получение и применение альдегидов
Альдегиды, их химические и физические свойства. Получение и применение альдегидов Описание молекул
Описание молекул Химия и повседневная жизнь человека
Химия и повседневная жизнь человека Химическое равновесие в гомогенных системах
Химическое равновесие в гомогенных системах Щелочные металлы
Щелочные металлы Составление ионных уравнений
Составление ионных уравнений Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения
Строение атома. Связь основных характеристик атома с его положением в таблице Д.И. Менделеева. Способы изображения строения teoriya_elektroliticheskoy_dissotsiatsii
teoriya_elektroliticheskoy_dissotsiatsii Семь доисторических металлов
Семь доисторических металлов Презентация на тему Применение спиртов
Презентация на тему Применение спиртов  Белки. Структуры белков
Белки. Структуры белков Обобщающий урок по теме «Соединения химических элементов» 8 класс.
Обобщающий урок по теме «Соединения химических элементов» 8 класс.