Слайд 2Соли – это химические соединения, состоящие из катионов и анионов. Могут быть получены

при взаимодействии кислот и оснований с выделением воды
Слайд 3КЛАССИФИКАЦИЯ СОЛЕЙ
Средние соли – продукты полного замещения атомов водорода в кислоте химическим

элементом металлом (состоят из катионов металла и анионов кислотного остатка)
Na2SO4, K3PO4
Кислые соли - продукты неполного замещения атомов водорода в кислоте химическим элементом металлом (в анион кислотного остатка входит водород)
NaHSO4, K2HPO4
Основные соли - продукты неполного замещения гидроксогрупп в гидроксиде металла кислотными остатками (катион содержит гироксогруппы)
CuOHCl, AlOH(NO3)2
Слайд 4КЛАССИФИКАЦИЯ СОЛЕЙ
Двойные соли – соли, содержащие два катиона
KAl(SO4)2
Смешанные соли – соли,

содержащие два аниона
CaOCl2
Комплексные соли – соли, содержащие ион комплексообразователя, связанный с лигандами
Na[Al(OH)4]
Слайд 5ЗАДАНИЕ 1 ( ПИСЬМЕННО)
К средним солям относится каждое из двух веществ
Fe(OH)2Cl и

Fe(HSO4)2
MgCl2 и Mg(OH)NO3
KHCO3 и NaHSiO3
K3PO4 и BaSiO3
Слайд 6ЗАДАНИЕ 2 (ПИСЬМЕННО)
Установите соответствие между формулой соли и её принадлежностью к определённой

группе.
А) ZnSO4 1) кислая
Б) Cu2(OH)2CO3 2) средняя
В) KAl(SO4)2 3)основная
Г) NaHSO4 4) двойная
5)комплексная
Слайд 7ЗАДАНИЕ 3 (ПИСЬМЕННО)
Установите соответствие между солью и классом (группой) солей, к которому

она принадлежит.
А) Сa(OCl)Cl 1) основные
Б) NaH2PO4 2) кислые
В) Al(OH)SO4 3) средние
Г) Fe(SCN)2 4) двойные
5) смешанные
Слайд 8ЗАДАНИЕ 4 (ПИСЬМЕННО)
Формулы только основных солей указаны в ряду,
KHCO3, Na2Cr2O7, (CUOH)2SO4
CuCl2,

NaHSO3, (AlOH)Cl2
Ca(HCO3)2, ZnS, (FeOH)Cl
(FeOH)NO3, (CuOH)2CO3, MgOHCl
Слайд 9СПОСОБЫ ПОЛУЧЕНИЯ СРЕДНИХ СОЛЕЙ
Основания + кислота:
3NaOH + H3PO4 = Na3PO4 + 3H2O
Основный

оксид + кислота:
MgO + H2SO4 = MgSO4 + H2O
Кислотный оксид + щелочь:
SO3 + 2NaOH = Na2SO4 + H2O
Кислотный оксид + основный оксид:
SO3 + Na2O = Na2SO4
Слайд 10СПОСОБЫ ПОЛУЧЕНИЯ СРЕДНИХ СОЛЕЙ
Соль + кислота:
BaCl2 + H2SO4 = BaSO4↓ + 2HCl
Раствор

соли + раствор соли:
BaCl2 + Na2SO4 = BaSO4↓ + 2NaCl
Раствор соли + раствор щелочи:
MgSO4 + 2NaOH = Mg(OH)2 + Na2SO4
Слайд 11СПОСОБЫ ПОЛУЧЕНИЯ СРЕДНИХ СОЛЕЙ
Металл + неметалл:
Mg + S = MgS
Металл + раствор

соли:
Mg + CuSO4 = MgSO4 + Cu
Металл + кислота:
Mg + H2SO4 = MgSO4 + H2
Слайд 12ЗАДАНИЕ 5 (ПИСЬМЕННО)
Нерастворимая соль образуется при взаимодействии
KOH(р-р) и H3PO4(р-р)
HCl(р-р) и Mg(NO3)2(р-р)

HNO3(р-р) и CuO
Ca(OH)2(р-р) и CO2
Слайд 13РАЗЛОЖЕНИЕ СРЕДНИХ СОЛЕЙ
Разложение карбонатов 2 группы главной подгруппы:
CaCO3 = CaO + CO2
Разложение

нитратов:
2NaNO3 = 2NaNO2 +O2
2Cu(NO3)2 = 2CuO + 4NO2 +O2
2AgNO3 = 2Ag + 2NO2 + O2
Разложение других солей:
2KMnO4 = K2MnO4 + MnO2 + O2
2KClO3 = 2KCl + 3O2
Слайд 14ПОЛУЧЕНИЕ КИСЛЫХ СОЛЕЙ
Взаимодействие избытка кислоты с основанием:
H3PO4 + NaOH = NaH2PO4 +

H2O
Взаимодействие избытка кислотного оксида с основанием:
CO2 + KOH = KHCO3
Слайд 15ЗАДАНИЕ 6 (ПИСЬМЕННО)
Установите соответствие между реагирующими веществами и продуктами из взаимодействия.
А) KOH

+ SO3(изб) → 1) KHSO4
Б) KOH + SO3(нед) → 2) K2SO3
В) KOH + CO2(изб) → 3) K2CO3 и H2O
Г) KOH + CO2(нед) → 4) K2SO4 и H2O
5) KHCO3
6) KHSO3
Слайд 16ПОЛУЧЕНИЕ ОСНОВНЫХ СОЛЕЙ
Взаимодействие кислоты с избытком основания:
Fe(OH)3 + HCl = Fe(OH)2Cl +

H2O
Взаимодействие избытка соли со щелочью:
Cu(NO3)2 +NaOH = CuOHNO3 + NaNO3
Слайд 17ПЕРЕХОД ОДНИХ СОЛЕЙ В ДРУГИЕ
Средние → кислые:
Na3PO4 + 2H3PO4 =
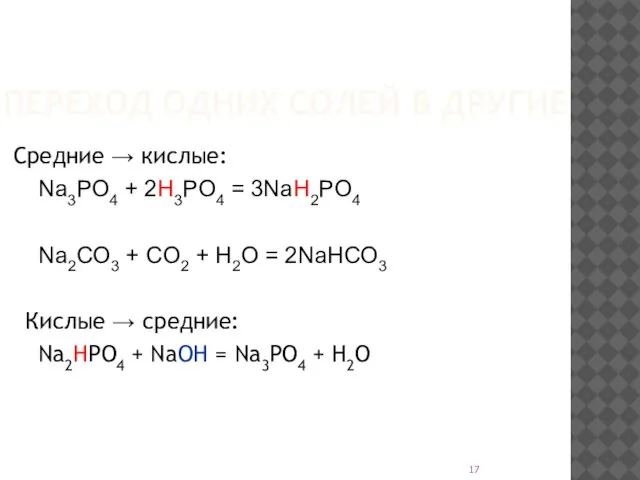
3NaH2PO4
Na2CO3 + CO2 + H2O = 2NaHCO3
Кислые → средние:
Na2HPO4 + NaOH = Na3PO4 + H2O
















 Фракционный состав нефти. Химический состав нефти
Фракционный состав нефти. Химический состав нефти Магний и кальций
Магний и кальций Свойства белков
Свойства белков Жидкая углекислота
Жидкая углекислота Презентация на тему Кристаллическая решетка
Презентация на тему Кристаллическая решетка  Электронное и пространственное строение алкенов. Гомология и изомерия алкенов
Электронное и пространственное строение алкенов. Гомология и изомерия алкенов Нитробактерии. Нитратное дыхание
Нитробактерии. Нитратное дыхание Про краски
Про краски Вероятность протекания химических реакций
Вероятность протекания химических реакций Природные источники углеводородов
Природные источники углеводородов Типы загрязнений биосферы
Типы загрязнений биосферы Степень окисления
Степень окисления Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Силикатная промышленность
Силикатная промышленность Аллотропия Аллотропные видоизменения (модификации)
Аллотропия Аллотропные видоизменения (модификации) Кислоты в химии
Кислоты в химии Состав и строение атома. Изотопы
Состав и строение атома. Изотопы Количество вещества. Моль
Количество вещества. Моль Методи визначення корозійної стійкості матеріалів (тема 11)
Методи визначення корозійної стійкості матеріалів (тема 11) Классификация органических соединений. 10 класс
Классификация органических соединений. 10 класс Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка
Аммиак. Состав. Строение. Химическая ковалентная полярная связь. Кристаллическая молекулярная решетка Характеристика элемента по Периодической системе Д.И. Менделеева
Характеристика элемента по Периодической системе Д.И. Менделеева Презентация на тему Химический состав клетки: ультрамикроэлементы
Презентация на тему Химический состав клетки: ультрамикроэлементы  Получение серной кислоты
Получение серной кислоты Искусство фотографии и химия
Искусство фотографии и химия Предмет органической химии
Предмет органической химии Химия и география. Викторина
Химия и география. Викторина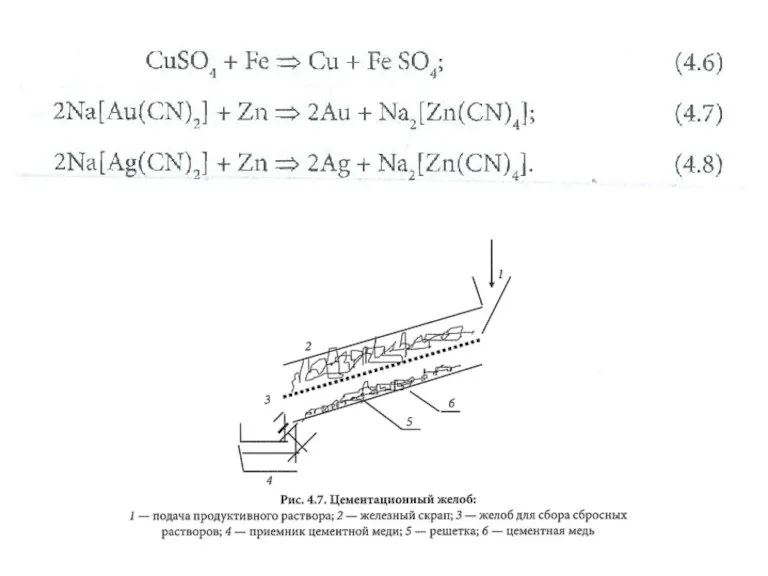 Гальванохимическая очистка. Сорбция
Гальванохимическая очистка. Сорбция