Слайд 2Классификация
Оксиды
(ЭхОу)
Кислоты
(Н+кисл.ост)
Соли
(Ме+кисл.ост)
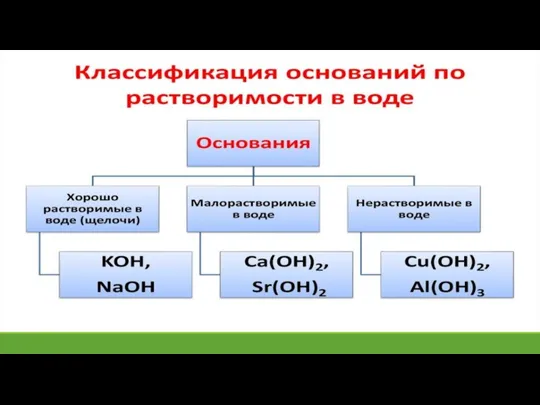
Основания
(Ме+ОН)

Слайд 3ОКСИДЫ
Кислотные
НемеО
Пример: СО2; SO3; N2O5
Основные
МеО
Пример: СаО; FeO.

Слайд 4Задание: Выпишите оксиды в столбик, напротив формулы запишите характер оксида, дайте ему

название:BaO, CaO, P2O5, SiO2, Li2O, CuO, MgO,SO2, WO3, ZnO,Br2O7
Слайд 5 Основным оксидам соответствуют основания: Na2O + H2O = 2NaOH
Кислотным оксидам соответствуют кислоты(кислородсодержащие):

SO3 + H2O → H2SO4
Слайд 6Задание: Составьте уравнения реакции взаимодействия следующих оксидов с водой. Дайте названия продуктам

реакции.
K2O+ H2O->
CO2+H2O->
Li2O+H2O->
P2O5+H2O->
N2O5+H2O->
MgO+H2O->
Слайд 8С помощью каких (не менее трех) химических реакций можно получить:
А) Оксид алюминия
Б)

Оксид кальция
В) Оксид углерода(IV)
Слайд 9Кислоты
По содержанию атомов кислорода
Бескислородные
Кислородсодержащие
По числу атомов водорода
* Одноосновные
* Двухосновные
* Трехосновные

Слайд 10Задание: В соответствии с классификацией охарактеризуйте следующие кислоты:
HNO3, HF ,HCl, HBr ,HI,

H2SO4, H2SO3, H2S ,H2CO3 , H2SiO3.
Дайте им названия.
Слайд 11Кислоты взаимодействуют с металлами. Для взаимодействия кислот с металлами должны выполнятся некоторые

условия:
металл должен быть достаточно активным по отношению к кислотам (в ряду активности металлов он должен располагаться до водорода). Чем левее находится металл в ряду активности, тем интенсивнее он взаимодействует с кислотами;
При протекании химических реакций кислоты с металлами образуется соль и выделяется водород
Слайд 12Составьте уравнения:
С какими металлами будет вступать в реакцию H2SO4, назовите продукты

реакции.
Ag, Ca, Mg, Sn, Cu, Hg, Au, Ni.
Слайд 13Кислоты вступают в реакцию нейтрализации
Реакция нейтрализа́ции (от лат. neuter — ни тот,

ни другой) — реакция взаимодействия кислоты и основания между собой с образованием соли и воды.
Реакция нейтрализации является разновидностью реакции обмена.
Пример: KOH+HCl ->KCl+H2O (образовались соль - хлорид калия и вода)
Слайд 14Составить уравнения реакции между:
Соляная кислота и гидроксид магния
Серная кислота и гидроксид натрия
Азотная

кислота и гидроксид цинка
Фосфорная кислота и гидроксид железа(II)
Угольная кислота и гидроксид кальция.
Дать название продуктам реакции
Слайд 16КОН- гидроксид калия. (валентность калия постоянная, поэтому в названии ее указывать не

нужно; валентность ОН – группы всегда равна 1)
Fe(OH)3 - гидроксид железа(III) –валентность железа 3, а ОН группы 1, поэтому ОН взяли в скобки и за ними поставили индекс 3. В названии указываем валентность, потому что у железа она переменная
Слайд 17Задание. Дать название следующим соединениям:
Fe(OH)2 ; Fe(OH)3 ; Al(OH)3; LiOH; NaOH; KOH;

RbOH; CsOH; Ca(OH)2; Sr(OH)2; Ba(OH)2.
Слайд 19Решить цепочки превращений, дать названия веществам, указать тип химической реакции:
Сa->CaO->Ca(OH)2->CaO
ZnO->ZnCl2->Zn(OH)2->ZnO

Слайд 21Назовите следующие соли:
NaNO3, K3PO4, CuSO4, Li3PO4, CaCO3, AgCl,
*Название солям дается от названия

кислотного остатка. Валентность металла указывается в скобках в том случае, если она переменная. Валентность кислотного остатка определяем по формуле соответствующей кислоты (число атомов водорода)
Слайд 22Составьте формулы солей по их названию:
Фосфат марганца(IV)
Сульфат магния
Нитрат цинка
Хлорид железа (III)
Сульфат хрома

(III)
Карбонат калия
Силикат калия
Фосфат меди(II)
Сульфид никеля (II)
Сульфит алюминия





















 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 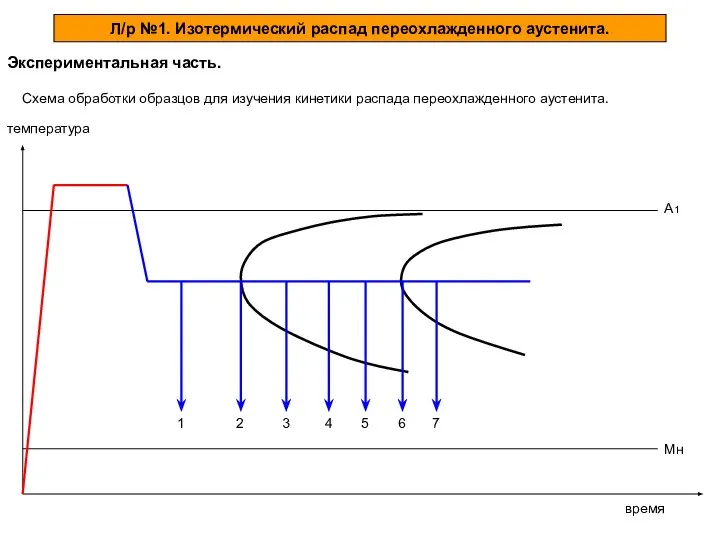 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций