Содержание
- 2. Кислоты сильные и слабые Все кислоты, независимо от их происхождения, объединяет общее свойство – они содержат
- 3. Основание сильное и слабое Основания – это сложные вещества, состоящие из ионов металлов и связанных с
- 4. Основание сильное и слабое Сильное основание - неорганическое химическое соединение, образованное гидроксильной группой -ОН и щелочным
- 5. Кислоты сильные и слабые Под их силой понимается способность отдавать ионы водорода. Если кислота легко отдает
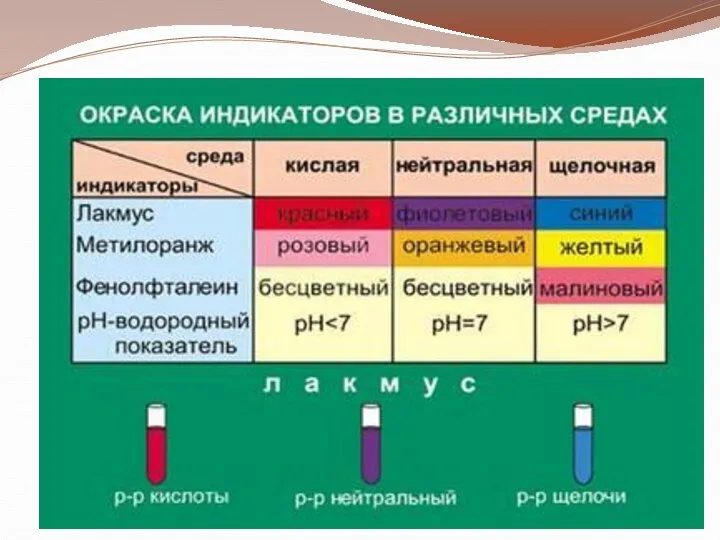
- 6. Кислоты сильные и слабые Самый простой и наглядный способ (хоть и не очень точный) – это
- 7. «Силачи» и «слабаки» в мире кислот и оснований Универсальная индикаторная бумага Изменение окраски в растворе щелочи
- 8. Полоску индикаторной бумаги обмакнуть в исследуемый раствор, затем быстро положить на белую подложку. Быстро нужно потому,
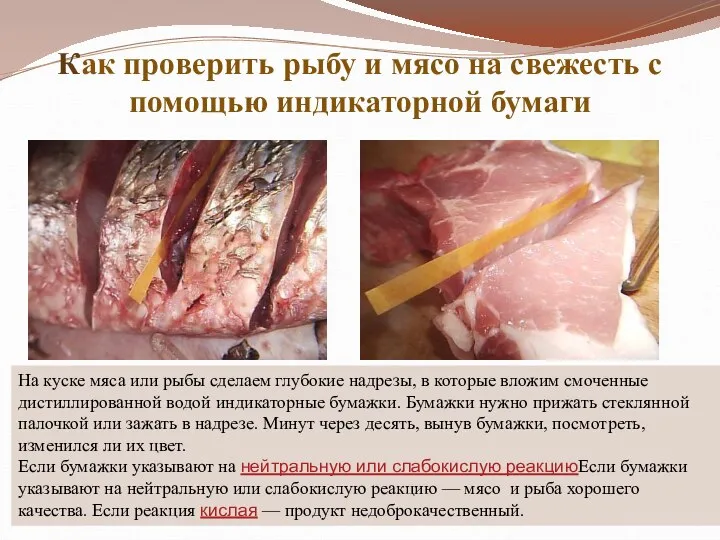
- 9. Как проверить рыбу и мясо на свежесть с помощью индикаторной бумаги На куске мяса или рыбы
- 10. В химии есть вещества, обладающие способностью менять свою окраску в присутствии кислот и щелочей. Эти вещества
- 12. Действие кислот и щелочей на металлы Молоток хранился в кладовке на одной полке с соляной кислотой.
- 13. Лабораторные опыты: Испытание растворов соляной, лимонной кислот, гидроксида натрия, соды, хлорида алюминия индикаторами. Взаимодействие соляной кислоты
- 15. Скачать презентацию










 Образование первичной структуры белка
Образование первичной структуры белка Кальций в океане: кораллы и жемчуг. Кальций в строительстве: гипс и алебастр
Кальций в океане: кораллы и жемчуг. Кальций в строительстве: гипс и алебастр Алканы: гомологический ряд, строение, номенклатура, физические свойства
Алканы: гомологический ряд, строение, номенклатура, физические свойства Основания. Физические и химические свойства оснований
Основания. Физические и химические свойства оснований Кинетическая устойчивость комплексов
Кинетическая устойчивость комплексов Геохимический барьер
Геохимический барьер Азот
Азот Простые вещества в стране Химляндии. 8 класс
Простые вещества в стране Химляндии. 8 класс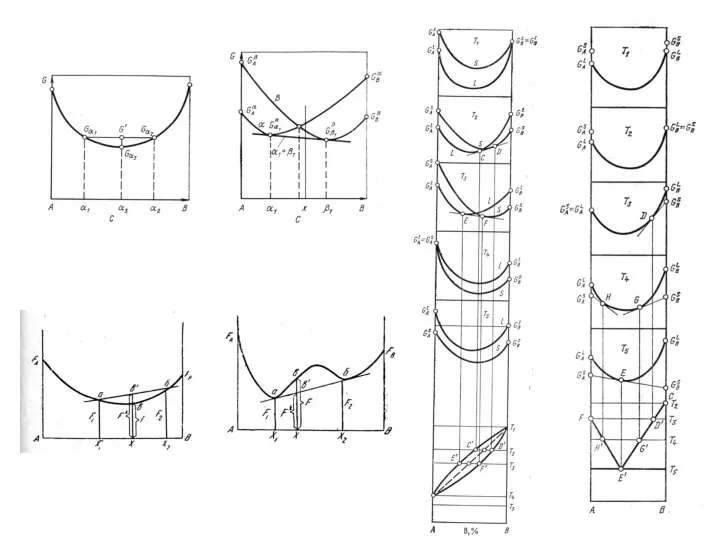 Кинетика кристаллизации сплавов
Кинетика кристаллизации сплавов Основания. 8 класс
Основания. 8 класс Цезий сверхактивный 1860 г
Цезий сверхактивный 1860 г Структура материалов. Введение в науку о материалах
Структура материалов. Введение в науку о материалах Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья
Стеклообразование, структура и свойства стекол системы Na2O – B2O3 – SiO2 на основе комплексного борсодержащего сырья Химические вещества парабены
Химические вещества парабены Бор и его соединения
Бор и его соединения Ковалентная полярная химическая связь
Ковалентная полярная химическая связь Классы неорганических веществ
Классы неорганических веществ Минеральные воды Старой Руссы
Минеральные воды Старой Руссы Физические и фазовые состояния полимеров
Физические и фазовые состояния полимеров Платина
Платина Застосування рідких кристалів
Застосування рідких кристалів Периодический закон Д. Менделеева с точки зрения строения атома. Часть 1
Периодический закон Д. Менделеева с точки зрения строения атома. Часть 1 Шаблон для презентации по химии
Шаблон для презентации по химии Стереоизомерия
Стереоизомерия Подгруппа кислорода. Решение экспериментальных задач
Подгруппа кислорода. Решение экспериментальных задач Аминокислоты. Общая формула
Аминокислоты. Общая формула Вода. Классы неорганических соединений. 8 класс
Вода. Классы неорганических соединений. 8 класс Растворы. 8 класс
Растворы. 8 класс