Содержание
- 2. Теплота растворения (ΔHраств.) – тепловой эффект образования любого не идеального раствора независимо от агрегатного состояния компонентов.
- 3. Теплота растворения зависит от агрегатного состояния растворителя и растворенных веществ; от концентрации раствора; от того, были
- 4. Зависимость теплоты растворения от агрегатного состояния компонентов раствора Теплота растворения твердых тел в жидкости складывается из
- 5. Тепловой эффект растворения газа в жидкости может быть представлен в виде суммы двух слагаемых – теплоты
- 6. Зависимость теплоты растворения от концентрации раствора
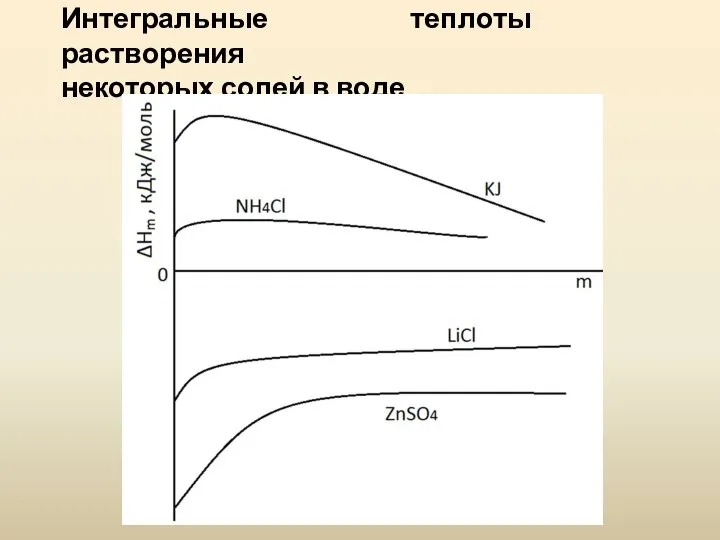
- 7. Интегральные теплоты растворения некоторых солей в воде
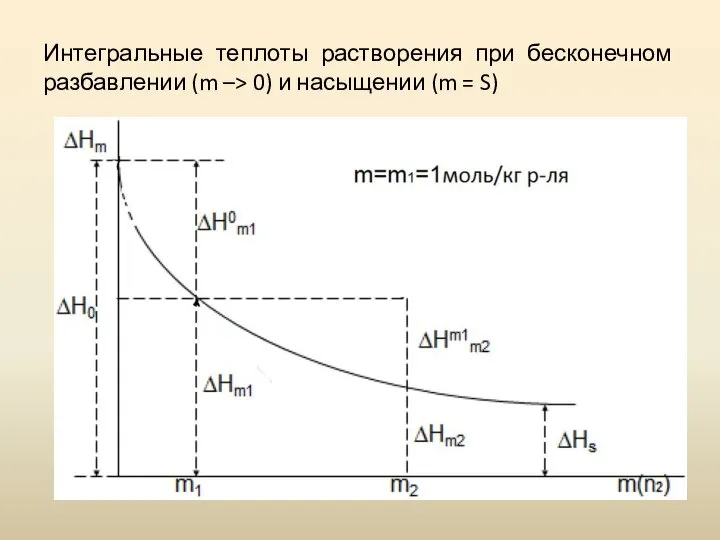
- 8. Первой интегральной теплотой растворения (ΔH0) называется тепловой эффект растворения 1 моль вещества в бесконечно большом количестве
- 9. Интегральные теплоты растворения при бесконечном разбавлении (m –> 0) и насыщении (m = S)
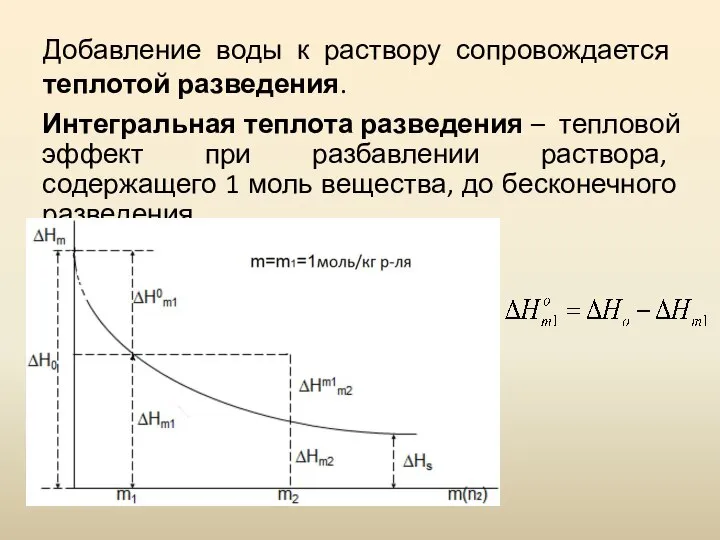
- 10. Добавление воды к раствору сопровождается теплотой разведения. Интегральная теплота разведения – тепловой эффект при разбавлении раствора,
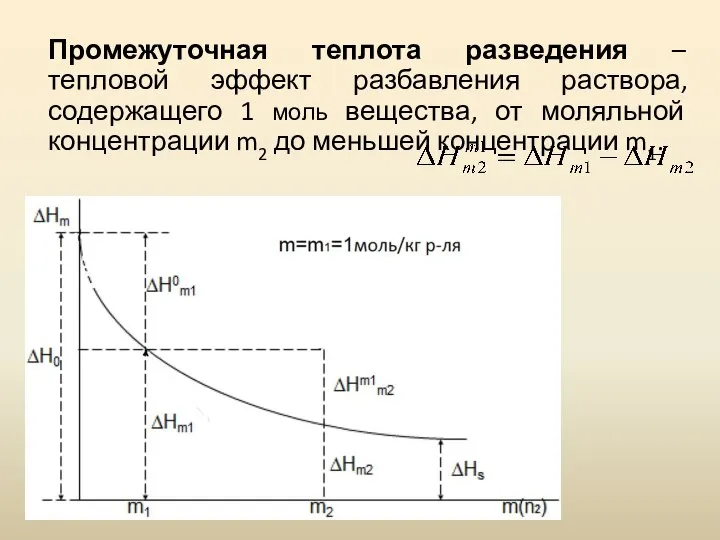
- 11. Промежуточная теплота разведения – тепловой эффект разбавления раствора, содержащего 1 моль вещества, от моляльной концентрации m2
- 12. Дифференциальная (парциальная) теплота растворения - тепловой эффект от растворения 1 моля вещества в бесконечно большом объеме
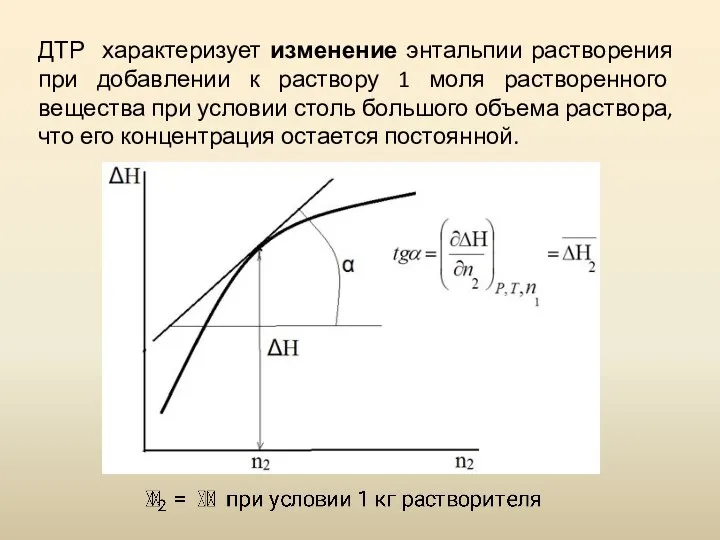
- 13. ДТР характеризует изменение энтальпии растворения при добавлении к раствору 1 моля растворенного вещества при условии столь
- 15. Скачать презентацию







 Учитель химии МАОУ СОШ № 61 города Тюмени Белова Н.В.
Учитель химии МАОУ СОШ № 61 города Тюмени Белова Н.В. Презентация на тему Неорганические и органические основания
Презентация на тему Неорганические и органические основания  Ионы. Ионная связь.
Ионы. Ионная связь. Якісні реакції органічних речовин
Якісні реакції органічних речовин Общие способы получения металлов
Общие способы получения металлов Основные классы неорганических соединений
Основные классы неорганических соединений СТРОЕНИЕ АТОМА ПРОТОНЫ ЭЛЕКТРОНЫ НЕЙТРОНЫ
СТРОЕНИЕ АТОМА ПРОТОНЫ ЭЛЕКТРОНЫ НЕЙТРОНЫ Презентация на тему Водород, его общая характеристика, нахождение в природе и его свойства
Презентация на тему Водород, его общая характеристика, нахождение в природе и его свойства  Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение Расчет энергетического профиля реакции N,N,N’,N’-тетраметилгуанидина с о-метиленхиноном
Расчет энергетического профиля реакции N,N,N’,N’-тетраметилгуанидина с о-метиленхиноном Стекло. Виды стекла
Стекло. Виды стекла Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера
Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера Действие активированного угля
Действие активированного угля 10 класс урок № 2 ТХС
10 класс урок № 2 ТХС Аэрозоли и аэродисперсии
Аэрозоли и аэродисперсии Сера и ее соединения
Сера и ее соединения Пористые стекла
Пористые стекла Количественный анализ. Методы количественного анализа
Количественный анализ. Методы количественного анализа Презентация на тему Неметаллы
Презентация на тему Неметаллы  Презентация по Химии "Стиральные порошки и их экологическое воздействие на окружающую среду"
Презентация по Химии "Стиральные порошки и их экологическое воздействие на окружающую среду"  Классификация органических веществ
Классификация органических веществ Химические свойства металлов
Химические свойства металлов Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb
Как меняется термическая устойчивость и реакционная способность связей Э-C и Э-O-Э в ряду Э=Si, Ge, Sn, Pb Высокомолекулярные соеденения
Высокомолекулярные соеденения Общая характеристика элементов подгруппы углерода. Углерод как простое вещество
Общая характеристика элементов подгруппы углерода. Углерод как простое вещество Аминокислоты и их применение
Аминокислоты и их применение Презентация на тему Жиры, их строение и свойства
Презентация на тему Жиры, их строение и свойства