Содержание
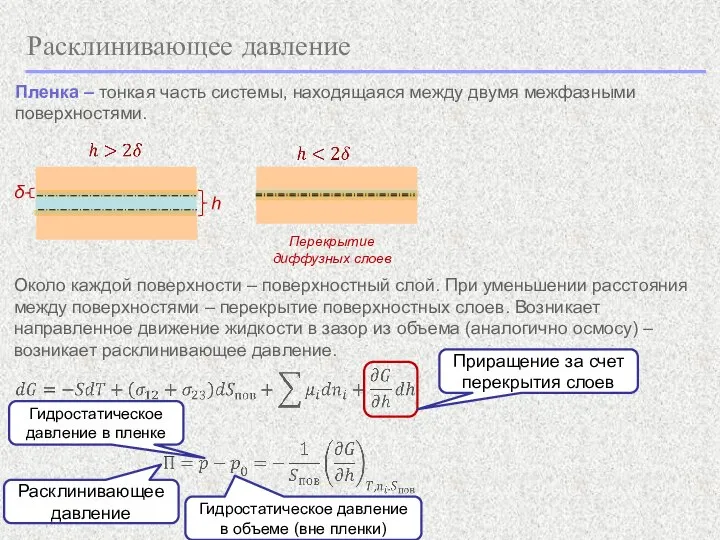
- 2. Расклинивающее давление Пленка – тонкая часть системы, находящаяся между двумя межфазными поверхностями.
- 3. Расклинивающее давление Расклинивающее давление – интегральный параметр, учитывающий как силы притяжения, так и силы отталкивания. Расклинивающее
- 4. Расклинивающее давление Составляющие расклинивающего давления: Молекулярные (силы Ван-дер-Ваальса); Электростатические (взаимодействие перекрывающихся ДЭС); Структурные (изменение структуры растворителя
- 5. Теория ДЛФО – общие положения Теория ДЛФО (DLVO) создана Дерягиным, Ландау, Фервеем и Овербеком Используется для
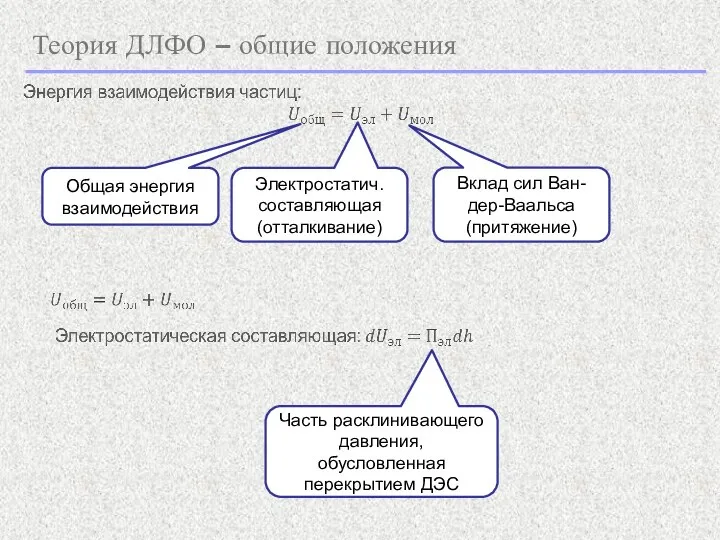
- 6. Теория ДЛФО – общие положения Общая энергия взаимодействия Электростатич. составляющая (отталкивание) Вклад сил Ван-дер-Ваальса (притяжение) Часть
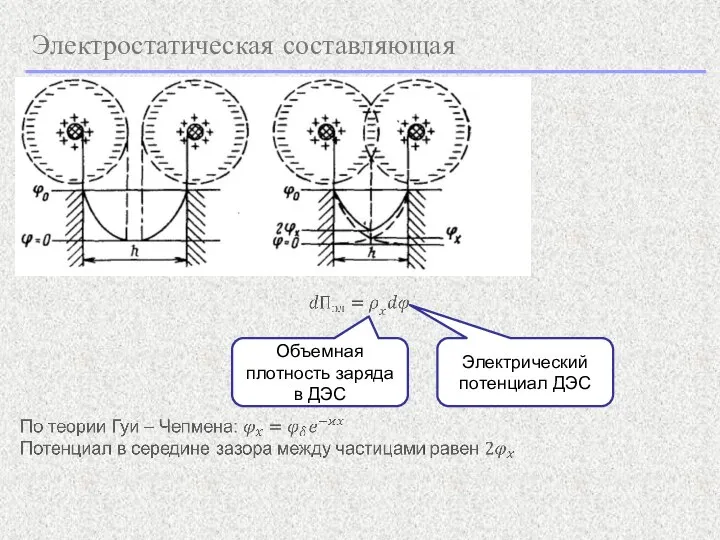
- 7. Электростатическая составляющая Объемная плотность заряда в ДЭС Электрический потенциал ДЭС
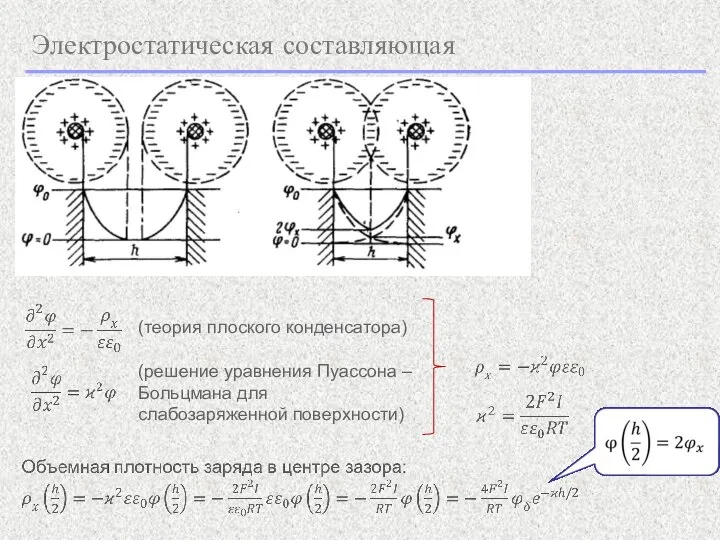
- 8. Электростатическая составляющая (теория плоского конденсатора) (решение уравнения Пуассона – Больцмана для слабозаряженной поверхности)
- 9. Электростатическая составляющая
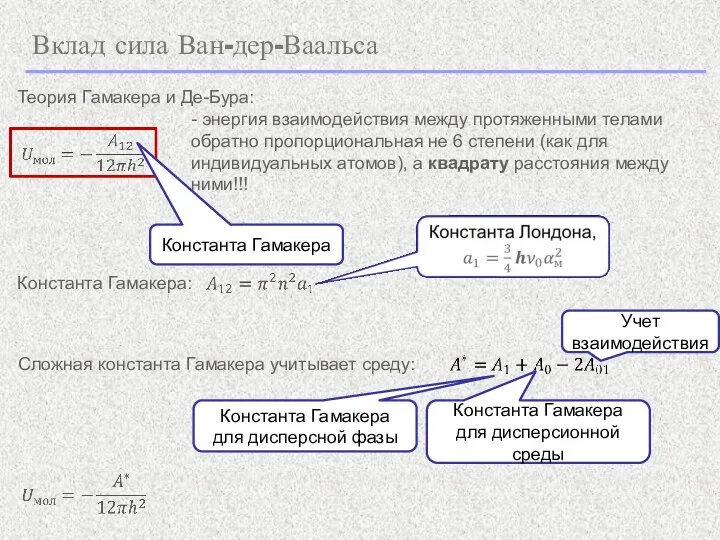
- 10. Вклад сила Ван-дер-Ваальса - энергия взаимодействия между протяженными телами обратно пропорциональная не 6 степени (как для
- 11. Потенциальные кривые I – непосредственное слипание частиц II – притяжение через прослойку среды Ортокинетическая коагуляция: взаимодействие
- 12. Потенциальные кривые 1 – силы притяжения на любом расстоянии преобладают - быстрая коагуляция с образованием агрегатов;
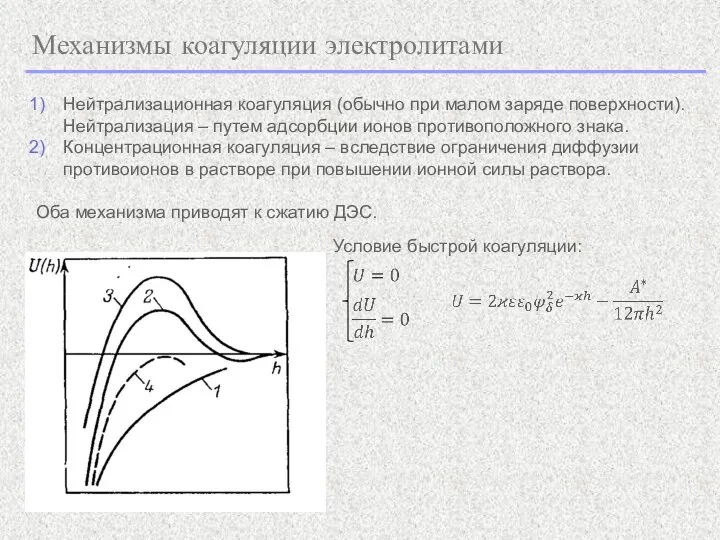
- 13. Механизмы коагуляции электролитами Нейтрализационная коагуляция (обычно при малом заряде поверхности). Нейтрализация – путем адсорбции ионов противоположного
- 14. Механизмы коагуляции электролитами (1) (2) Для слабозаряженных поверхностей (нейтрализационная коагуляция):
- 15. Закономерности коагуляции электролитами Коагуляция наступает при перекрытии ДЭС Коагуляцию вызывают ионы противоположного знака по отношению к
- 17. Скачать презентацию








 Игровые технологии на уроках химии как средство реализации системно-деятельного подхода в обучении
Игровые технологии на уроках химии как средство реализации системно-деятельного подхода в обучении Движение молекул
Движение молекул Ферменты
Ферменты Углеводы. Дисахариды. Полисахариды. Лекция 6
Углеводы. Дисахариды. Полисахариды. Лекция 6 Сухой спирт
Сухой спирт Алкины: получение и свойства
Алкины: получение и свойства Электролитическая диссоциация
Электролитическая диссоциация Анодное растворение mn5si3-электрода в сернокислом фторидсодержащем электролите
Анодное растворение mn5si3-электрода в сернокислом фторидсодержащем электролите Аллотропия. Аллотропные формы серы
Аллотропия. Аллотропные формы серы Разминка
Разминка Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера
Особенности строения ионных кристаллов. Постоянная Моделунга. Энергия кристаллической решётки. Цикл Борна-Габера Катализ
Катализ Проантоцианидины. Антиоксидантные и антирадикальные свойства
Проантоцианидины. Антиоксидантные и антирадикальные свойства Основные классы неорганических соединений. Мы едем, едем, едем…
Основные классы неорганических соединений. Мы едем, едем, едем… Технология производства органических лекарственных веществ. Препараты алифатического ряда: хлороформ, йодоформ, хлоральгидрат
Технология производства органических лекарственных веществ. Препараты алифатического ряда: хлороформ, йодоформ, хлоральгидрат Понятие о предельных углеводородах. Алканы
Понятие о предельных углеводородах. Алканы Алканы 10-класс
Алканы 10-класс Общие свойства растворов
Общие свойства растворов Классификация химических реакций
Классификация химических реакций Строение вещества. Химическая связь и кристаллическое строение. Урок 1: Ионная и ковалентная связи
Строение вещества. Химическая связь и кристаллическое строение. Урок 1: Ионная и ковалентная связи Классы неорганических веществ
Классы неорганических веществ Обобщение и систематизация знаний по теме Вещества и их классификация
Обобщение и систематизация знаний по теме Вещества и их классификация Классификация органических веществ
Классификация органических веществ Современная аналитическая химия.Учебная литература
Современная аналитическая химия.Учебная литература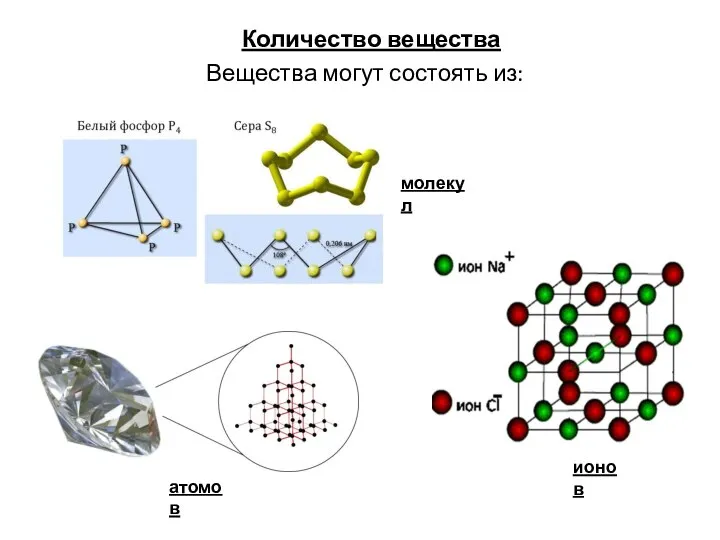 Количество вещества
Количество вещества Структура периодической таблицы элементов
Структура периодической таблицы элементов Подготовка газа к транспорту с применением процесса низкотемпературной сепарации
Подготовка газа к транспорту с применением процесса низкотемпературной сепарации Галогены
Галогены