Содержание
- 2. Аквариум Акватория Акваланг Акварель Аква (лат. aqua) — «вода» на латинском и итальянском языках Гидра (др.
- 3. ВОДА В ПРИРОДЕ. СОСТАВ, СВОЙСТВА И ПРИМЕНЕНИЕ ВОДЫ. Вода! Ты не просто необходима для жизни, ты
- 4. План: История открытия Химический элемент … как простое вещество Получение и собирание воды Физические свойства воды
- 5. ВОДА – ОТКРЫТИЕ XVII ВЕКА Получение сложных веществ из более простых называется синтезом (греч. синтез –
- 6. РАЗЛОЖЕНИЕ ВОДЫ А. Лавуазье Fe трубка Fe2O3 3Fe + 4H2O → Fe3O4 + 4H2↑
- 7. РАЗЛОЖЕНИЕ ВОДЫ Эвдиометр 1 л водорода (н.у.) 0,089 г 1 л кислорода (н.у.) 1, 429 г
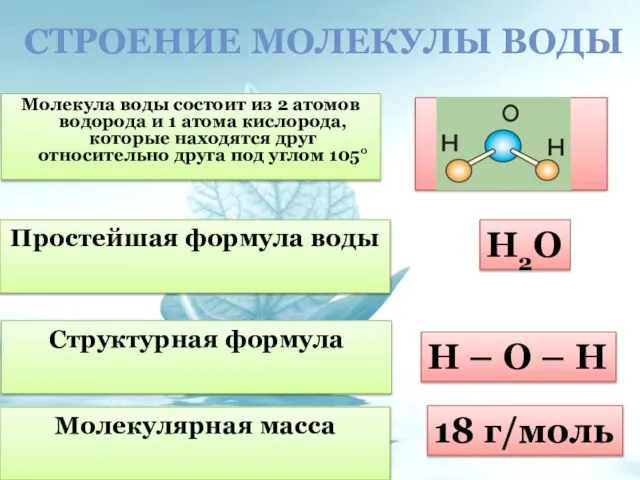
- 8. СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ Простейшая формула воды Структурная формула Молекулярная масса Н2О Н – О – Н
- 9. ФИЗИЧЕСКИЕ СВОЙСТВА ВОДЫ Жидкость Без вкуса Без запаха Без цвета ρ=1 г/см3 T0плав=00С(лед→вода) T0кип=1000С(вода →пар) Вода
- 10. АНОМАЛИИ ВОДЫ ВОДА - САМОЕ АНОМАЛЬНОЕ СОЕДИНЕНИЕ НА ЗЕМНОМ ШАРЕ Единственное вещество, которое на земле существует
- 12. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ I.Взаимодействие воды с простыми веществами: 1.Реакция с металлами, расположенными в ряду активности металлов
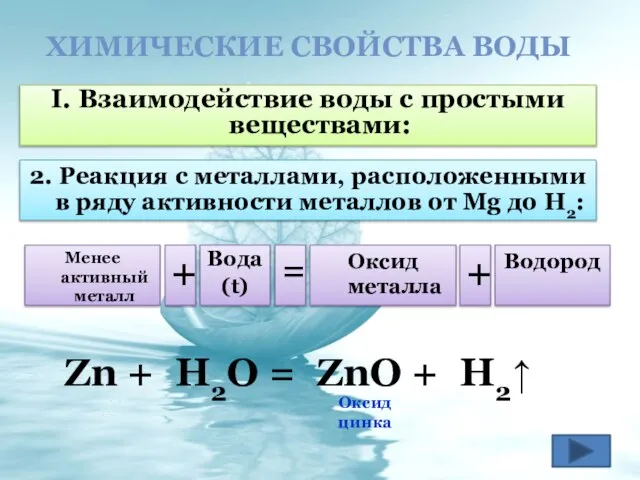
- 13. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ I. Взаимодействие воды с простыми веществами: 2. Реакция с металлами, расположенными в ряду
- 14. ХИМИЧЕСКИЕ СВОЙСТВА ВОДЫ I. Взаимодействие воды с простыми веществами: 3. Реакция с некоторыми неметаллами протекает при
- 15. Запишите: Слева направо по ряду химическая активность металлов убывает. Активные металлы (до алюминия включительно) Металлы средней
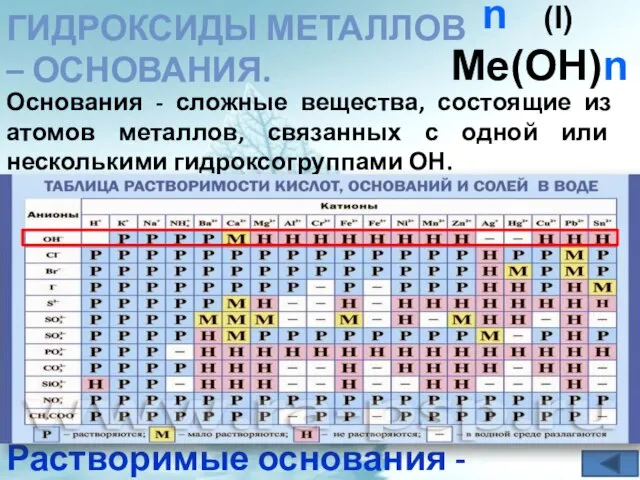
- 16. ГИДРОКСИДЫ МЕТАЛЛОВ – ОСНОВАНИЯ. Основания - сложные вещества, состоящие из атомов металлов, связанных с одной или
- 17. ГИДРОСФЕРА - ВОДНАЯ ОБОЛОЧКА ЗЕМЛИ
- 18. ГИДРОСФЕРА 97 % - морская вода 3% - пресная вода Ледники 79% Подземные воды 20% Реки,
- 19. Почти ¾ поверхности земного шара покрыты водой, образующей океаны, моря, реки и озёра. Много воды находится
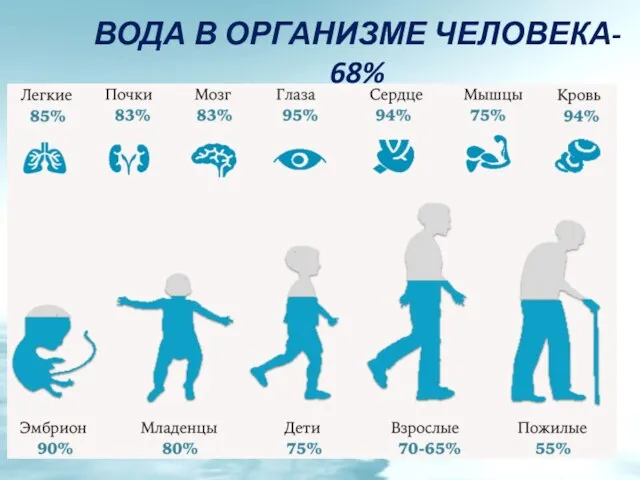
- 20. ВОДА В ОРГАНИЗМЕ ЧЕЛОВЕКА- 68%
- 21. ВОДООЧИСНЫЕ СООРУЖЕНИЯ
- 23. Скачать презентацию
















 Типы кристаллических решеток
Типы кристаллических решеток Судын оксидтермен реакциясы
Судын оксидтермен реакциясы Ионная химическая связь
Ионная химическая связь Классы неорганических соединений
Классы неорганических соединений Истина - дочь времени, а не авторитета
Истина - дочь времени, а не авторитета Презентация на тему Виды кристаллических решеток
Презентация на тему Виды кристаллических решеток 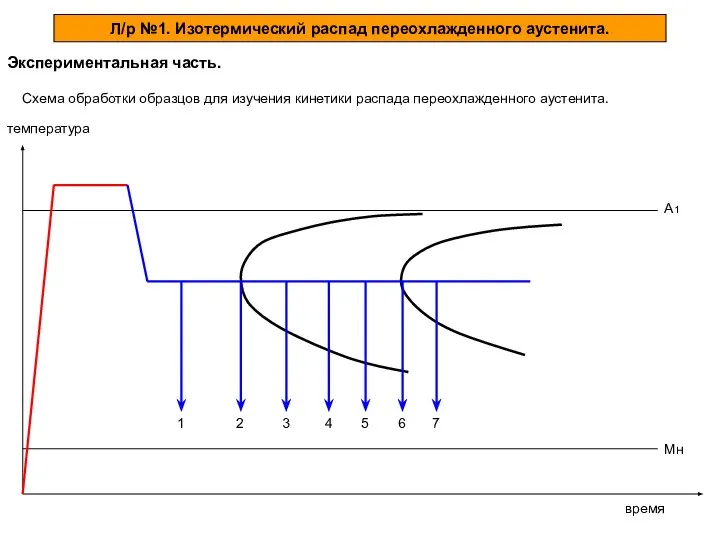 Изотермический распад переохлажденного аустенита. Экспериментальная часть
Изотермический распад переохлажденного аустенита. Экспериментальная часть Содержание варианта ЕГЭ
Содержание варианта ЕГЭ 11_.21
11_.21 Использование комплексно-ориентированных заданий на уроках
Использование комплексно-ориентированных заданий на уроках Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Реакции окисления-восстановления в химическом анализе. (Лекция 7.2)
Реакции окисления-восстановления в химическом анализе. (Лекция 7.2) Алканы
Алканы Химия и автомобиль
Химия и автомобиль Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства
Общая характеристика элементов подгруппы углерода. Углерод – его строение и свойства Природный каучук
Природный каучук Классификация оксидов
Классификация оксидов Химические реакции
Химические реакции Образование и получение веществ. 6 класс
Образование и получение веществ. 6 класс Металлы
Металлы Закон сохранения массы веществ. Уравнения химических реакций.
Закон сохранения массы веществ. Уравнения химических реакций. Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Валентность. Определение валентности по формулам
Валентность. Определение валентности по формулам Кроссворд. Плотность
Кроссворд. Плотность Алкены
Алкены Коррозия металлов
Коррозия металлов Вещества с атомной кристаллической решеткой
Вещества с атомной кристаллической решеткой Cкорость химических реакций
Cкорость химических реакций